
Kalorimetri hvilke studier og anvendelser
Det kalorimetri er en teknik, der bestemmer ændringer i kalorieindholdet i et system, der er forbundet med en kemisk eller fysisk proces. Det er baseret på måling af temperaturændringer, når et system absorberer eller udsender varme. Kalorimeteret er det udstyr, der anvendes i reaktioner, hvor en varmeveksling er involveret.
Hvad der kaldes en "kaffekop" er den enkleste form for denne type apparat. Ved dets anvendelse måles den mængde varme, der er involveret i reaktioner, der udføres ved konstant tryk i en vandig opløsning. En kaffekop kalorimeter består af en beholder af polystyren, der placeres i et bægerglas..

Vandet placeres i polystyrenbeholderen udstyret med et låg lavet af det samme materiale, der giver det en vis grad af varmeisolering. Derudover har beholderen et termometer og en mekanisk omrører..
Dette kalorimeter måler den mængde varme, der absorberes eller udsendes, afhængigt af om reaktionen er endoterm eller eksoterm, når en reaktion finder sted i en vandig opløsning. Systemet, der skal undersøges, består af reaktanterne og produkterne.
Artikelindeks
- 1 Hvad studerer kalorimetri?
- 2 Varmekapacitet på et kalorimeter
- 2.1 Eksempel på brug af kalorimeteret til beregning af specifik varme
- 3 Kalorimetrisk pumpe
- 4 typer kalorimeter
- 4.1 Isotermisk titreringskalorimeter (CTI)
- 4.2 Differential scanningskalorimeter
- 5 applikationer
- 5.1 Anvendelse af isotermisk titreringskalorimetri
- 5.2 Anvendelse af differentiel scanningskalorimetri
- 6 Referencer
Hvad studerer kalorimetri?
Kalorimetri studerer forholdet mellem varmeenergien forbundet med en kemisk reaktion, og hvordan den bruges til at bestemme dens variabler. Deres anvendelser inden for forskningsområder retfærdiggør omfanget af disse metoder.
Kalorimeters kalorikapacitet
Denne kapacitet beregnes ved at dividere den mængde varme, der absorberes af kalorimeteret, med temperaturændringen. Denne variation er produktet af varmen, der udsendes i en eksoterm reaktion, som er lig med:
Mængden af varme, der absorberes af kalorimeteret + mængden af varme, der absorberes af opløsningen
Variationen kan bestemmes ved at tilføje en kendt mængde varme ved at måle temperaturændringen. Til denne bestemmelse af kalorikapaciteten anvendes benzoesyre normalt, da dens forbrændingsvarme er kendt (3.227 kJ / mol).
Kalorikapacitet kan også bestemmes ved at tilføje varme ved hjælp af en elektrisk strøm.
Eksempel at bruge kalorimeteret til at beregne specifik varme
En 95 g bar af et metal opvarmes til 400 ° C, hvorefter det straks føres til et kalorimeter med 500 g vand, først ved 20 ° C. Systemets endelige temperatur er 24 ºC. Beregn metalets specifikke varme.
Δq = m x ce x Δt
I dette udtryk:
Δq = belastningsvariation.
m = masse.
ce = specifik varme.
Δt = temperaturvariation.
Varmen, som vandet vinder, er lig med varmen fra metalstangen.
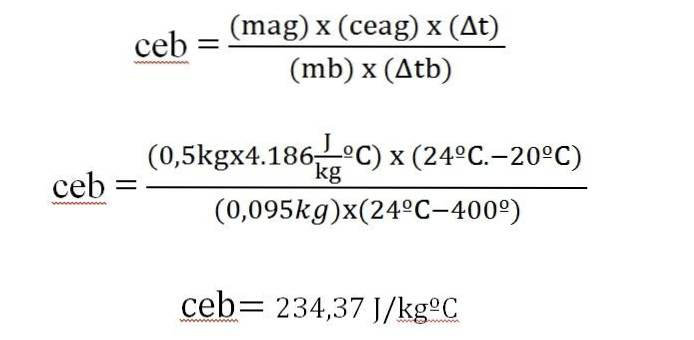
Denne værdi svarer til den, der vises i en tabel over den specifikke varme for sølv (234 J / kg ºC).
Så en af anvendelserne af kalorimetri er samarbejdet om identifikation af materialer.
Kalorimetrisk pumpe
Den består af en stålbeholder, kendt som pumpen, modstandsdygtig over for de høje tryk, der kan opstå under reaktionerne, der opstår i denne beholder. denne beholder er forbundet til et tændingskredsløb for at starte reaktionerne.
Pumpen nedsænkes i en stor beholder med vand, hvis funktion er at absorbere den varme, der genereres i pumpen under reaktionerne, hvilket gør temperaturvariationen lille. Vandbeholderen er udstyret med et termometer og en mekanisk omrører.
Energiforandringer måles med næsten konstant volumen og temperatur, så der arbejdes ikke med de reaktioner, der opstår i pumpen.
ΔE = q
ΔE er variationen af den interne energi i reaktionen og q den varme, der genereres i denne.
Typer af kalorimeter
Isotermisk titreringskalorimeter (CTI)
Kalorimeteret har to celler: i den ene placeres prøven, og i den anden placeres referencen generelt vand.
Den temperaturforskel, der genereres mellem cellerne - på grund af reaktionen, der forekommer i prøvecellen - annulleres af et feedback-system, der injicerer varme for at udligne temperaturerne i cellerne..
Denne type kalorimeter gør det muligt at følge interaktionen mellem makromolekyler og deres ligander..
Differential scanningskalorimeter
Dette kalorimeter har to celler, som CTI, men har en enhed, der gør det muligt at bestemme temperaturen og varmestrømmene forbundet med ændringer i et materiale som en funktion af tiden.
Denne teknik giver information om foldning af proteiner og nukleinsyrer såvel som deres stabilisering..
Ansøgninger

-Kalorimetri gør det muligt at bestemme varmeudvekslingen, der forekommer i en kemisk reaktion, hvilket giver en klarere forståelse af mekanismen for denne.
-Ved at bestemme et materiales specifikke varme giver kalorimetri data, der hjælper med at identificere det.
-Da der er en direkte proportionalitet mellem varmeændring af en reaktion og koncentrationen af reaktanterne kombineret med det faktum, at kalorimetri ikke kræver klare prøver, kan denne teknik bruges til at bestemme koncentrationen af stoffer, der er til stede i komplekse matricer..
-Inden for kemiteknik anvendes kalorimetri i sikkerhedsprocessen såvel som i forskellige områder af optimeringsprocessen, kemisk reaktion og i driftsenheden..
Anvendelse af isotermisk titreringskalorimetri
-Det samarbejder om etablering af enzymvirkningsmekanismen såvel som inden for dets kinetik. Denne teknik kan måle reaktioner mellem molekyler, bestemme bindingsaffinitet, støkiometri, entalpi og entropi i opløsning uden behov for markører..
-Vurderer interaktionen mellem nanopartikler og proteiner og er sammen med andre analysemetoder et vigtigt redskab til registrering af konformationsændringer i proteiner.
-Det har anvendelse til konservering af mad og afgrøder.
-Med hensyn til opbevaring af mad kan du bestemme dets forringelse og holdbarhed (mikrobiologisk aktivitet). Det kan sammenligne effektiviteten af forskellige fødevarekonserveringsmetoder og er i stand til at bestemme den optimale dosis konserveringsmidler såvel som nedbrydningen i emballagekontrollen.
-Hvad angår vegetabilske afgrøder, kan du studere frøets spiring. At være i vand og i nærvær af ilt frigiver de varme, der kan måles med et isotermisk kalorimeter. Undersøg alderen og forkert opbevaring af frøene og studer deres vækstrate i lyset af variationer i temperatur, pH eller forskellige kemikalier.
-Endelig kan du måle jordens biologiske aktivitet. Derudover kan det opdage sygdomme.
Anvendelse af differentiel scanningskalorimetri
-Sammen med isotermisk kalorimetri har det gjort det muligt at undersøge interaktion af proteiner med deres ligander, den allosteriske interaktion, foldning af proteiner og mekanismen for deres stabilisering..
-Varmen, der frigøres eller absorberes under en molekylær bindingshændelse, kan måles direkte.
-Differential scanningskalorimetri er et termodynamisk værktøj til direkte etablering af optagelsen af varmeenergi, der forekommer i en prøve. Dette gør det muligt at analysere de faktorer, der er involveret i proteinmolekylets stabilitet..
-Han studerer også termodynamikken i nukleinsyrefoldningsovergangen. Teknikken tillader bestemmelse af den oxidative stabilitet af linolsyre, der er isoleret og koblet til andre lipider.
-Teknikken anvendes i kvantificering af nanosolider til farmaceutisk brug og i den termiske karakterisering af nanostrukturerede lipidtransportører..
Referencer
- Whitten, K., Davis, R., Peck, M. og Stanley, G. Kemi. (2008). 8. udgave Cengage Learning Rediger.
- Rehak, N. N. og Young, D. S. (1978). Potentielle anvendelser af kalorimetri i det kliniske laboratorium. Clin. Chem. 24 (8): 1414-1419.
- Stossel, F. (1997). Anvendelser af reaktionskalorimetri inden for kemisk teknik. J. Therm. Anal. 49 (3): 1677-1688.
- Weber, P. C. og Salemme, F. R. (2003). Anvendelser af kalorimetriske metoder til lægemiddelopdagelse og undersøgelse af proteininteraktioner. Curr. Opin. Struktur. Biol. 13 (1): 115-121.
- Gill, P., Moghadem, T. og Ranjbar, B. (2010). Differential scanningskalorimetriske teknikker: anvendelser inden for biologi og nanovidenskab. J. Biol. Tech. 21 (4): 167-193.
- Omanovic-Miklicanin, E., Manfield, I. og Wilkins, T. (2017). Anvendelser af isotermisk titreringskalorimetri til evaluering af protein-nanopartikelinteraktioner. J. Therm. Anal. 127: 605-613.
- Community College Consortium for Bioscience Credentials. (7. juli 2014). Kaffekop kalorimeter. [Figur]. Hentet den 7. juni 2018 fra: commons.wikimedia.org



Endnu ingen kommentarer