
Enkel destillationsproces og eksempler
Det enkel destillation er en procedure, hvor dampene, der produceres fra en væske, føres direkte til en kondensator, inden for hvilken temperaturen på dampene falder, og deres kondens opstår.
Det bruges til at adskille en flygtig komponent fra de ikke-flygtige komponenter, der findes i en væske. Det bruges også til adskillelse af to væsker til stede i en opløsning med meget forskellige kogepunkter..
Enkel destillation er ikke en effektiv metode til adskillelse af to flygtige væsker, der er til stede i en opløsning. Når temperaturen på den stiger gennem varmetilførslen, stiger molekylernes kinetiske energi også, hvilket giver dem mulighed for at overvinde samhørighedskraften mellem dem..
Flygtige væsker begynder at koge, når deres damptryk er lig med det ydre tryk, der udøves på opløsningens overflade. Begge væsker bidrager til sammensætningen af den dannede damp, jo mere flygtig væske er større; det vil sige den med det laveste kogepunkt.
Derfor udgør den mere flygtige væske det meste af det dannede destillat. Processen gentages, indtil en ønsket renhed eller den højest mulige koncentration er nået..
Artikelindeks
- 1 Enkel destillationsproces
- 1.1 Udstyr
- 1.2 Kondensator
- 1.3 Opvarmning
- 2 Eksempler
- 2.1 Destillation af vand og alkohol
- 2.2 Separation af flydende fast stof
- 2.3 Alkohol og glycerin
- 3 Referencer
Enkel destillationsproces
Ved simpel destillation øges temperaturen på en opløsning, indtil den koger. I det øjeblik sker overgangen mellem flydende til luftformige tilstande. Dette observeres, når en konstant bobling begynder i opløsningen.
Hold
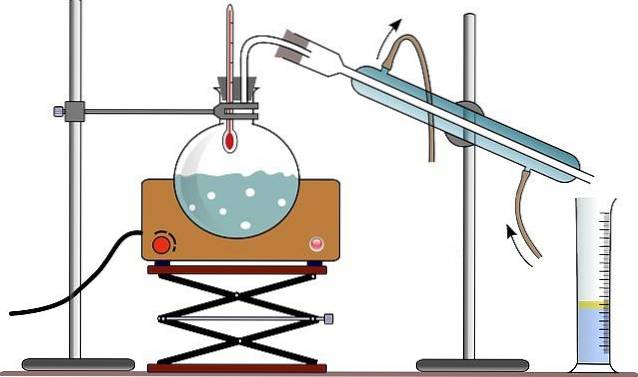
Udstyret til simpel destillation består normalt af en brænder eller et varmetæppe (se billede); en rund ildfast glasflaske med en formalet glasmunding, der muliggør kobling og nogle glasperler (nogle bruger en træpind) for at reducere størrelsen af de dannede bobler.
Glasperlerne fungerer som bobledannende kerner, som tillader væsken at koge langsomt og undgår overophedning, der resulterer i dannelsen af en slags kæmpe bobler; i stand til selv at uddrive en væskemasse ud af destillationskolben.
Fastgjort til kolbens munding er en ildfast glasadapter med tre mundinger, der er lavet af malet glas. Den ene hals er fastgjort til destillationskolben, en anden hals er fastgjort til kondensatoren, og den tredje hals lukkes ved hjælp af en gummiprop..
På billedet mangler holderen denne adapter; og i stedet placeres termometeret og en direkte forbindelse til kondensatoren gennem den samme gummiprop.
Kondensator
Kondensatoren er en enhed designet til at udføre den funktion, som navnet indikerer: at kondensere den damp, der bevæger sig gennem den. Gennem sin øvre mund er den koblet til adapteren, og gennem den nederste mund er den forbundet med en ballon, hvor destillationsprodukterne opsamles..
I tilfælde af billedet bruger de (skønt det ikke altid er korrekt) en gradueret cylinder til at måle det destillerede volumen på en gang.
Vandet, der cirkulerer gennem kondensatorens ydre kappe, trænger ind gennem den nederste del og kommer ud gennem den øvre del. Dette sikrer, at kondensatortemperaturen er lav nok til at tillade kondensering af dampene, der dannes i destillationskolben..
Alle de dele, der udgør destillationsapparatet, er fastgjort med klemmer forbundet til en metalstøtte.
Et volumen af opløsningen, der skal destilleres, anbringes i den runde kolbe med en passende kapacitet.
Korrekte forbindelser foretages ved hjælp af grafit eller fedt for at sikre effektiv forsegling, og opvarmning af opløsningen begynder. Samtidig begynder vandets passage gennem kondensatoren.
Opvarmning
Når destillationskolben opvarmes, observeres en stigning i temperaturen på termometeret, indtil et punkt nås, hvor temperaturen forbliver konstant. Dette forbliver sådan, selvom opvarmningen fortsætter; medmindre al flygtig væske er fordampet fuldstændigt.
Forklaringen på denne adfærd er, at kogepunktet for komponenten med den laveste kogepunkt for væskeblandingen er nået, hvor dens damptryk er lig med det ydre tryk (760 mm Hg).
På dette tidspunkt udnyttes al varmeenergien i skiftet fra flydende tilstand til gasform, der involverer udløbet af væskens intermolekylære samhørighedskraft. Derfor kan varmeforsyningen ikke oversættes til en stigning i temperaturen..
Destillationens flydende produkt opsamles i korrekt mærkede kolber, hvis volumen vil afhænge af det volumen, der oprindeligt var placeret i destillationskolben..
Eksempler
Destillation af vand og alkohol
Du har en 50% alkohol i vandopløsning. Når man ved, at alkoholens kogepunkt er 78,4 ° C, og vandets kogepunkt er ca. 100 ° C, kan man så opnå en ren alkohol med et simpelt destillationstrin? Svaret er nej.
Ved opvarmning af alkohol-vand-blandingen nås kogepunktet for den mest flygtige væske oprindeligt; i dette tilfælde alkohol. Den dannede damp vil have en højere andel af alkoholen, men der vil også være en høj tilstedeværelse af vand i dampen, da kogepunkterne er ens..
Væsken, der opsamles fra destillationen og kondensationen, har en alkoholprocent på over 50%. Hvis denne væske udsættes for successive destillationer, kan en koncentreret alkoholopløsning opnås; men ikke rent, da dampene fortsætter med at trække vand til en bestemt sammensætning og danne det, der er kendt som en azeotrop
Det flydende produkt ved gæring af sukker har en alkoholprocent på 10%. Denne koncentration, der kan bringes til 50%, som i tilfældet med whisky, ved simpel destillation.
Væske-faststof adskillelse
En opløsning af et salt i vand består af en væske, der kan fordampes, og en ikke-flygtig forbindelse med et højt kogepunkt: salt..
Ved destillation af opløsningen kan der fås rent vand i kondensationsvæsken. I mellemtiden vil saltene bundfældes i bunden af destillationskolben.
Alkohol og glycerin
Der er en blanding af ethylalkohol med et kogepunkt på 78,4 ° C og glycerin med et kogepunkt på 260 ° C. Når den udsættes for simpel destillation, vil den dannede damp have en meget høj procentdel alkohol tæt på 100%..
Derfor opnås en destilleret væske med en procentdel af alkohol svarende til dampens. Dette sker, fordi kogepunkterne for væsker er meget forskellige.
Referencer
- Claude Yoder. (2019). Destillation. Kablet kemi. Gendannet fra: wiredchemist.com
- Whitten, Davis, Peck & Stanley. (2008). Kemi. (8. udgave). CENGAGE Læring.
- Dragani, Rachelle. (17. maj 2018). Tre eksempler på simple destillationsblandinger. Videnskabelig. Gendannet fra: sciencing.com
- Helmenstine, Anne Marie, Ph.D. (2. januar 2019). Hvad er destillation? Kemidefinition. Gendannet fra: thoughtco.com
- Dr. Welder. (s.f.). Enkel destillation. Gendannet fra: dartmouth.edu
- University of Barcelona. (s.f.). Destillation. Gendannet fra: ub.edu



Endnu ingen kommentarer