
Dibenzalacetone egenskaber, reaktionsmekanisme, anvendelser, risici
Det dibenzalaceton (dba) er en organisk forbindelse, hvis molekylformel er C17H14O. Det er et gulligt fast stof, der afhængigt af dets renhed kan fremstå som krystaller. Det bruges i solcreme og organometalliske synteser, hvor palladium bruges som katalysator.
Selvom syntese er en relativt enkel proces, der er ganske tilbagevendende i undervisningslaboratorier for at forklare aldolkondensation, er dens mekanisme noget omfattende, og flere faktorer skal tages i betragtning. Det anvendte benzaldehyd, som kondenserer med acetone, skal destilleres frisk for at garantere dets lave oxidation i kontakt med luft..

Ligeledes anvendes et basisk ethanol-vandmedium til at opløse reagenserne og samtidig fremme den endelige udfældning af dibenzalacetone, en hydrofob og uopløselig forbindelse. Indtil videre vides det ikke, hvilke negative virkninger dibenzalaceton kan have på kroppen eller miljøet, bortset fra at være et irriterende stof.
Artikelindeks
- 1 egenskaber
- 1.1 Fysisk udseende
- 1.2 Molær masse
- 1.3 Isomerer
- 1.4 Smeltepunkt
- 1.5 Opløselighed i vand
- 1.6 Struktur
- 2 Reaktionsmekanisme af dibenzalaceton
- 3 Syntese
- 3.1 Reagenser
- 3.2 Fremgangsmåde
- 3.3 Omkrystallisering
- 4 anvendelser
- 5 risici
- 6 Referencer
Ejendomme
Fysisk fremtoning
Støvet eller krystallinsk udseende gulligt fast stof.
Molar masse
234,29 g / mol
Isomerer
Dibenzalacetone forekommer som tre geometriske isomerer: trans-trans, trans-cis og cis-cis. Trans-trans-isomeren er den mest stabile af alle, og derfor den, der produceres mest under syntese.
Smeltepunkt
110-111 ° C Dette område varierer afhængigt af graden af renhed af det syntetiserede faste stof..
Vandopløselighed
Uopløselig.
Struktur
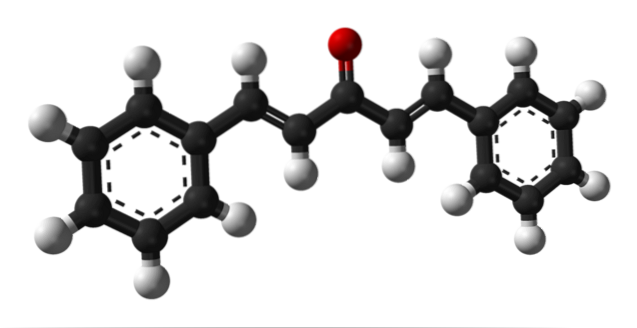
Det øverste billede viser molekylet af trans-trans dibenzalacetone-isomeren, repræsenteret af en model af kugler og søjler. I midten af den har vi carbonylgruppen og ved dens sider nogle dobbeltbindinger og to aromatiske benzenringe.
Dibenzalacetone er i det væsentlige apolar og hydrofob, da hele strukturen praktisk talt er sammensat af carbon- og hydrogenatomer. Carbonylgruppen giver den kun et lille dipolmoment.
Strukturen kan sammenlignes med den i et blad, da alle dets carbonatomer har SP-hybridiseringto; derfor hviler de på samme plan.
Lysfotoner interagerer med det π-konjugerede system af dibenzalacetone; især de af UV-stråling, der absorberes for at excitere delokaliserede elektroner. Denne egenskab gør dibenzalaceton til en fremragende absorber af ultraviolet lys..
Reaktionsmekanisme af dibenzalaceton
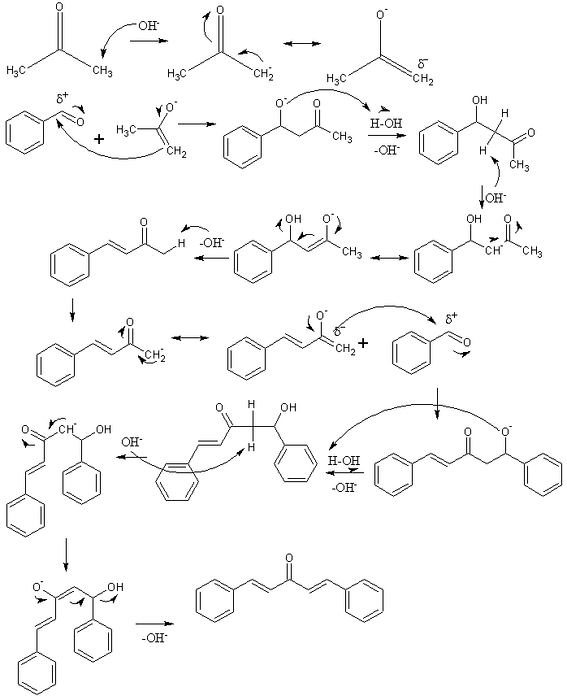
I det øverste billede har vi repræsenteret mekanismen for aldolkondensationen mellem benzaldehyd og acetone for således at stamme fra dibenzalacetone; specifikt dens trans-trans-isomer.
Reaktionen begynder med acetone i et basisk medium. OH- deprotonerer en sur proton af en af dens to methylgrupper, -CH3, giver anledning til en enolat: CH3C (O) CHto-, som aflokaliserer sin negative ladning ved resonans (første række i billedet).
Dette enolat fungerer derefter som et nukleofilt middel: det angriber carbonylgruppen i et benzaldehydmolekyle. Dens inkorporering i benzaldehyd genererer et alkoxid, der, fordi det er meget basisk, deprotonerer et vandmolekyle og bliver en aldol (anden række). Aldol eller β-hydroxyketon er kendetegnet ved at have grupperne C = O og OH.
Det basiske medium dehydrerer denne aldol, og der dannes en dobbeltbinding i dens struktur, som genererer benzylidenaceton (tredje række). Dernæst OH- det deprotonerer også et af dets sure hydrogener og gentager endnu et nukleofilt angreb på et andet benzaldehydmolekyle. Denne gang finder angrebet sted i en lavere hastighed (fjerde række).
Det dannede produkt deprotonerer et andet vandmolekyle og gennemgår dehydrering igen for at eliminere OH-gruppen og etablere en anden dobbeltbinding (femte og sjette række). Således og endelig produceres dibenzalacetone.
Syntese
Reagenser
Reagenserne til at udføre syntesen af dibenzalacetone er følgende:
- 95% ethanol.
- Frisk destilleret benzaldehyd fra bitter mandelolie.
- NaOH som basisk katalysator i destilleret vand.
De anvendte mængder afhænger af, hvor meget dibenzalacetone der skal syntetiseres. Det tilstræbes imidlertid, at der er et overskud af benzaldehyd, fordi en del af det oxideres til benzoesyre. Det garanteres også, at reaktionen tager kortere tid, og at den uønskede benzylidenaceton produceres i mindre grad..
Ethanol fungerer som et opløsningsmiddel for benzaldehyd, ellers ville det ikke opløses i det basiske NaOH-medium.
Behandle
I et stort bægerglas blandes ethanolen med benzaldehydet. Derefter tilsættes det basiske NaOH-medium under konstant magnetisk omrøring. I dette trin forekommer Cannizzaro-reaktionen i mindre grad; to molekyler benzaldehyd uforholdsmæssigt store i en af benzylalkohol og den anden af benzoesyre, let genkendelig ved sin karakteristiske søde lugt.
Til sidst tilsættes acetonen, og opløsningen ventes i en halv time for at blive uklar og gul-orange i farven. Dibenzalacetone vil udfældes på grund af vand, så der tilsættes et betydeligt volumen vand for at fremme dets komplette nedbør..
Dibenzalacetonen filtreres under vakuum, og dens gulagtige faste stof vaskes flere gange med destilleret vand..
Omkrystallisering

Til oprensning af dibenzalacetonen anvendes 95% ethanol eller varmt ethylacetat, således at krystaller med større renhed opnås hver gang omkrystallisationen gentages. Således vil det indledende gule pulver blive omdannet til små gule krystaller af dibenzalaceton..
Ansøgninger
Dibenzalacetone er en forbindelse, der ikke har mange anvendelser. På grund af dets evne til at absorbere ultraviolet lys bruges det til formulering af solcreme eller ethvert andet produkt, der søger at afbøde forekomsten af UV-stråler, det være sig belægninger eller maling..
På den anden side anvendes dibenzalacetone i de organometalliske synteser af palladium. Det fungerer som et bindemiddel, der koordinerer med palladiummetalatomer, Pd0, til dannelse af tris (dibenzylidenaceton) dipalladium-kompleks (0).
Denne organometalliske forbindelse tilvejebringer Pd-atomer0 i forskellige organiske synteser, så den opfører sig som en homogen katalysator, da den opløses i mange organiske opløsningsmidler.
Dibenzalaceton som bindemiddel er også let at erstatte med andre organiske bindemidler, hvilket gør det muligt for de organometalliske synteser af palladium at udvikle sig hurtigt..
Risici
Med hensyn til risiciene er der ikke meget information tilgængelig, der rapporterer om de mulige påvirkninger på sundheden eller miljøet, som dibenzalaceton kan forårsage. I sin rene tilstand er det et solidt irriterende stof ved indtagelse, vejrtrækning eller ved direkte kontakt med øjnene eller huden..
Imidlertid er det tilsyneladende ikke irriterende nok, at det ikke kan være en del af formuleringer til solcreme. På den anden side er det så uopløseligt i vand, at dets koncentration i det er ubetydeligt og præsenterer sig selv som et fast forurenende stof. I denne forstand er det ukendt, hvor skadelig den uklarhed, den forårsager, er for marine fauna eller jordbund..
Indtil andet er bevist, vil dibenzalacetone blive betragtet som en relativt sikker forbindelse, da dens lave reaktivitet ikke er en grund til risiko eller større forholdsregler..
Referencer
- Morrison, R. T. og Boyd, R, N. (1987). Organisk kemi. 5. udgave. Redaktionel Addison-Wesley Interamericana.
- Carey F. (2008). Organisk kemi. (Sjette udgave). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. (10. udgave.). Wiley plus.
- Wikipedia. (2020). Dibenzylidenaceton. Gendannet fra: en.wikipedia.org
- National Center for Biotechnology Information. (2020). Dibenzylidenaceton. PubChem Database. CID = 640180. Gendannet fra: pubchem.ncbi.nlm.nih.gov
- Organiske synteser. (2020). Dibenzalacetone. Gendannet fra: orgsyn.org
- Dibenzalacetone af Aldol Condensation. Gendannet fra: web.mnstate.edu



Endnu ingen kommentarer