
Sphingolipids egenskaber, funktioner, grupper, syntese

Det sphingolipider de repræsenterer en af de tre største familier af lipider til stede i biologiske membraner. Som glycerophospholipider og steroler er de amfipatiske molekyler med en hydrofil polær region og en hydrofob apolar region..
De blev først beskrevet i 1884 af Johann L. W. Thudichum, der beskrev tre sfingolipider (sphingomyelin, cerebrosider og cerebrosulfatid), der hører til de tre forskellige kendte klasser: phosphoesphingolipider, neutrale og sure glycosphingolipider..
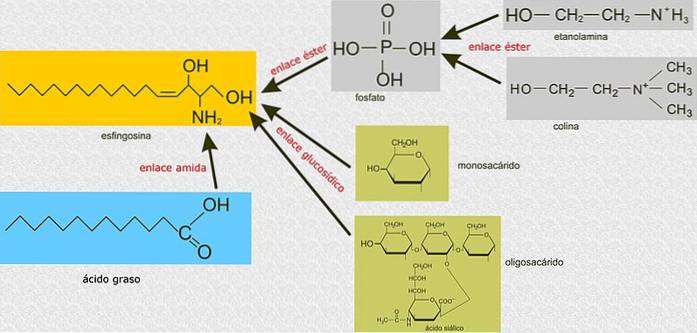
I modsætning til glycerophospholipider er sfingolipider ikke bygget på et glycerol-3-phosphatmolekyle som hovedskelet, men er forbindelser afledt af sphingosin, en aminoalkohol med en lang carbonhydridkæde bundet af en amidbinding..
Med hensyn til kompleksitet og mangfoldighed er mindst 5 forskellige basetyper kendt for sfingolipider i pattedyr. Disse baser kan forbindes med mere end 20 forskellige typer fedtsyrer med varierende længder og grader af mætning ud over de mange variationer i de polære grupper, der kan forekomme..
Biologiske membraner har ca. 20% sfingolipider. Disse har varierede og vigtige funktioner i celler, fra strukturel til signaltransduktion og kontrol af forskellige cellulære kommunikationsprocesser..
Fordelingen af disse molekyler varierer afhængigt af organellens funktion, hvor de findes, men normalt er koncentrationen af sfingolipider meget højere i det ydre monolag af plasmamembranen sammenlignet med det indre monolag og andre rum..
Hos mennesker er der mindst 60 arter af sfingolipider. Mange af dem er vigtige komponenter i membranerne i nerveceller, mens andre spiller vigtige strukturelle roller eller deltager i signaltransduktion, genkendelse, celledifferentiering, patogenese, programmeret celledød, blandt andre..
Artikelindeks
- 1 Struktur
- 2 funktioner
- 3 funktioner
- 3.1 -Strukturelle funktioner
- 3.2 -Signaleringsfunktioner
- 3.3 -Som receptorer i membranen
- 4 grupper af sfingolipider
- 4.1 Sphingomyelins
- 4.2 Neutrale glycolipider eller glycosphingolipider (gratis)
- 4.3 Sure gangliosider eller glycosphingolipider
- 5 Syntese
- 5.1 Syntese af ceramidskelettet
- 5.2 Dannelse af specifikke sfingolipider
- 6 Metabolisme
- 6.1 Regulering
- 7 Referencer
OGstruktur
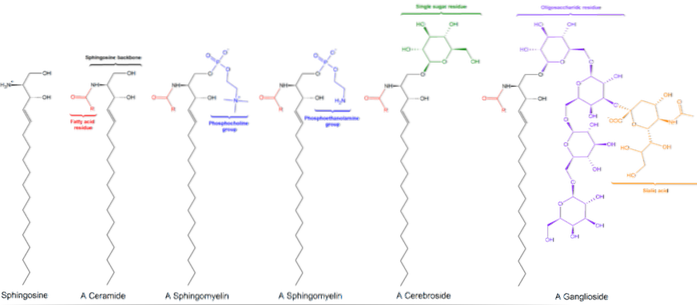
Alle sfingolipider er afledt af en L-serin, der kondenseres med en langkædet fedtsyre til dannelse af sfingoidbasen, også kendt som langkædebasen (LCB)..
De mest almindelige baser er sphinganin og sphingosin, som kun adskiller sig fra hinanden i nærværelse af en dobbeltbinding trans mellem kulstof 4 og 5 af fedtsyren fra sfingosin.
Kulstofferne 1, 2 og 3 i sfingosin er strukturelt analoge med kulstofferne i glycerol af glycerophospholipider. Når en fedtsyre er bundet til carbon 2 i sfingosin gennem amidbindinger, dannes et ceramid, som er et molekyle, der meget ligner diacylglycerol og repræsenterer den enkleste sfingolipid.
De langkædede fedtsyrer, der udgør de hydrofobe regioner i disse lipider, kan være meget forskellige. Længderne varierer fra 14 til 22 kulstofatomer, der kan have forskellige grader af mætning, normalt mellem kulstof 4 og 5.
I position 4 eller 6 kan de have hydroxylgrupper og dobbeltbindinger i andre positioner eller endda forgreninger som methylgrupper.
Egenskaber
De fedtsyrekæder, der er bundet af amidbindinger til ceramider, er almindeligvis mættede og har tendens til at være længere end dem, der findes i glycerophospholipider, hvilket synes at være afgørende for deres biologiske aktivitet..
Et særpræg ved sfingolipidskelettet er, at de kan have en nettopositiv ladning ved neutral pH, sjælden blandt lipidmolekyler..
Men den pKa af aminogruppen er lav sammenlignet med en simpel amin, mellem 7 og 8, så en del af molekylet ikke er ladet ved fysiologisk pH, hvilket kan forklare den "frie" bevægelse af disse mellem dobbeltlagene.
Den traditionelle klassificering af sfingolipider stammer fra de mange modifikationer, som ceramidmolekylet kan gennemgå, især med hensyn til substitutionerne af grupperne i det polære hoved.
Funktioner
Sphingolipider er essentielle i dyr, planter og svampe såvel som i nogle prokaryote organismer og vira..
-Strukturelle funktioner
Sphingolipider modulerer de fysiske egenskaber af membraner, herunder deres fluiditet, tykkelse og krumning. Modulering af disse egenskaber giver dem også direkte indflydelse på den rumlige organisering af membranproteiner..
I lipid "flåder"
I biologiske membraner kan detekteres dynamiske mikrodomæner med mindre fluiditet, der består af kolesterol og sfingolipidmolekyler kaldet lipidflåder..
Disse strukturer forekommer naturligt og er tæt beslægtet med integrerede proteiner, celleoverfladereceptorer og signalproteiner, transportører og andre proteiner med glycosylphosphatidylinositol (GPI) -ankre..
-Signalfunktioner
De har funktioner som signalmolekyler, der fungerer som sekundære budbringere eller som udskilte ligander for celleoverfladereceptorer..
Som sekundære budbringere kan de deltage i reguleringen af calciumhomeostase, cellevækst, tumorigenese og undertrykkelse af apoptose. Desuden afhænger aktiviteten af mange integrale og perifere membranproteiner af deres tilknytning til sfingolipider..
Mange interaktioner mellem celler og cellen med dens omgivelser afhænger af eksponeringen af de forskellige polære grupper af sfingolipider til plasmamembranens ydre overflade..
Bindingen af glycosphingolipider og lectiner er afgørende for associeringen af myelin med axoner, adhæsionen af neutrofiler til endotelet osv..
Byprodukter af dit stofskifte
De vigtigste signalerende sfingolipider er langkædede baser eller sfingosiner og ceramider såvel som deres phosphorylerede derivater, såsom sphingosin 1-phosphat.
De metaboliske produkter fra mange sfingolipider aktiverer eller inhiberer flere nedstrøms mål (proteinkinaser, phosphoproteinphosphataser og andre), som styrer kompleks cellulær adfærd såsom vækst, differentiering og apoptose..
-Som receptorer på membranen
Nogle patogener bruger glycosphingolipider som receptorer til at formidle deres indtræden i værtsceller eller til at levere virulensfaktorer til dem..
Sfingolipider har vist sig at deltage i flere cellulære begivenheder såsom sekretion, endocytose, kemotaxis, neurotransmission, angiogenese og inflammation.
De er også involveret i membranhandel og påvirker således internalisering af receptorer, ordning, bevægelse og fusion af sekretoriske vesikler som reaktion på forskellige stimuli..
Sphingolipid grupper
Der er tre underklasser af sfingolipider, alle afledt af ceramid og adskiller sig fra hinanden ved polære grupper, nemlig: sfingomyeliner, glycolipider og gangliosider..
Sphingomyelins

Disse indeholder phosphocholin eller phosphoethanolamin som en polær hovedgruppe, hvorfor de klassificeres som phospholipider sammen med glycerophospholipider. De ligner naturligvis phosphatidylcholiner i tredimensionel struktur og generelle egenskaber, da de ikke har nogen ladning på deres polære hoveder..
De er til stede i plasmamembranerne i dyreceller og er især rigelige i myelin, en kappe, der omgiver og isolerer axonerne i nogle neuroner..
Neutrale glycolipider eller glycosphingolipider (gratis)
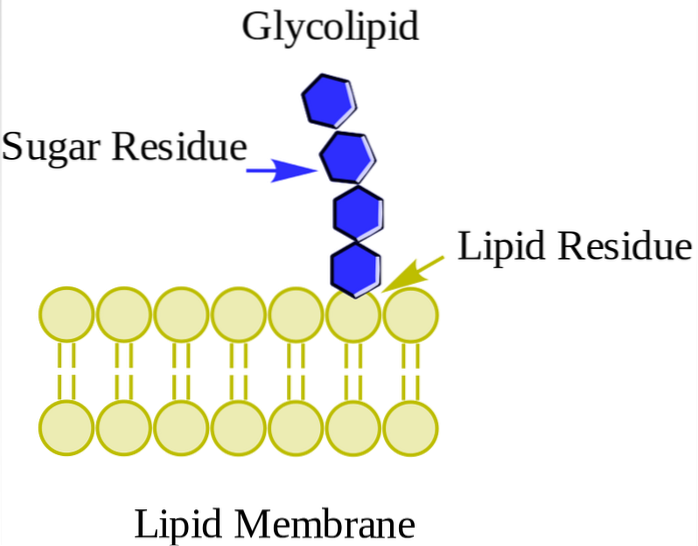
De findes primært på plasmamembranens ydre overflade og har et eller flere sukkerarter som en polær hovedgruppe bundet direkte til hydroxylen af carbon 1 i ceramiddelen. De har ikke fosfatgrupper. Da de ved pH 7 ikke har nogen ladning, kaldes de neutrale glycolipider.
Cerebrosider har et enkelt sukkermolekyle bundet til ceramid. De, der indeholder galactose, findes i plasmamembraner i ikke-nervevævsceller. Globosider er glycosphingolipider med to eller flere sukkerarter, sædvanligvis D-glucose, D-galactose eller N-acetyl-D-galactosamin..
Syre gangliosider eller glycosphingolipider
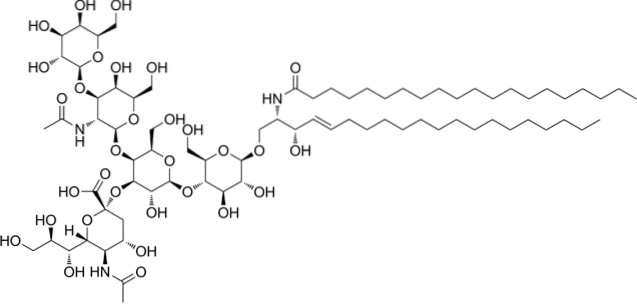
Disse er de mest komplekse sfingolipider. De har oligosaccharider som en polær hovedgruppe og en eller flere terminale N-acetylmuraminsyrerester, også kaldet sialinsyre. Sialinsyre giver gangliosider en negativ ladning ved pH 7, der adskiller dem fra neutrale glycosphingolipider..
Nomenklaturen for denne klasse af sfingolipider afhænger af mængden af sialinsyrerester, der er til stede i oligosacchariddelen af det polære hoved..
Syntese
Det langkædede basemolekyle eller sfingosin syntetiseres i det endoplasmatiske retikulum (ER), og tilsætningen af den polære gruppe til hovedet af disse lipider forekommer senere i Golgi-komplekset. Hos pattedyr kan der også forekomme en vis syntese af sfingolipider i mitokondrier.
Efter at have afsluttet deres syntese i Golgi-komplekset transporteres sfingolipider til andre celleområder gennem vesikelmedierede mekanismer..
Biosyntesen af sfingolipider består af tre grundlæggende begivenheder: syntese af langkædede baser, biosyntese af ceramider ved forening af en fedtsyre gennem en amidbinding og endelig dannelsen af komplekse sfingolipider gennem foreningen af de polære grupper på kulstof 1 i sfingoidbasen.
Ud over syntesen de novo, sfingolipider kan også dannes ved omsætning eller genanvendelse af langkædede baser og ceramider, som kan fodre puljen af sfingolipider.
Syntese af ceramidskelettet
Biosyntese af ceramid, rygraden i sfingolipider, begynder med den decarboxylative kondensation af et palmitoyl-CoA-molekyle og en L-serin. Reaktionen katalyseres af en heterodimer serin palmitoyl transferase (SPT), afhængig af pyridoxalphosphat, og produktet er 3-keto dihydrosphingosin..
Dette enzym inhiberes af β-halo-L-alaniner og L-cycloseriner. I gær kodes det af to gener, mens der i pattedyr er tre gener for dette enzym. Det aktive sted er placeret på det endoplasmatiske retikulums cytoplasmatiske ansigt.
Rollen af dette første enzym er bevaret i alle de undersøgte organismer. Der er dog nogle forskelle mellem taxaerne, der har at gøre med enzymets subcellulære placering: bakterienes cytoplasmatiske, gærenes, plantens og dyrens endoplasmatiske retikulum.
3-ketosphinganin reduceres efterfølgende af NADPH-afhængig 3-ketosphinganinreduktase til dannelse af sphinganin. Dihydroceramidsyntase (sphinganin-N-acyltransferase) acetylerer derefter sphinganin til dannelse af dihydroceramid. Ceramid dannes derefter af dihydroceramid-desaturase / reduktase, som indsætter en dobbeltbinding trans i position 4-5.
Hos pattedyr er der adskillige isoformer af ceramidsyntaser, der hver binder en specifik kæde af fedtsyrer til langkædede baser. Derfor tilvejebringer ceramidesyntaser og andre enzymer, langstrækninger, den vigtigste kilde til mangfoldighed af fedtsyrer i sfingolipider..
Specifik sfingolipidannelse
Sphingomyelin syntetiseres ved overførsel af en phosphocholin fra phosphatidylcholin til ceramid, hvorved diacylglycerol frigives. Reaktionen binder sphingolipid- og glycerophospholipid-signalveje.
Phosphoethanolamin ceramid syntetiseres fra phosphatidylethanolamin og ceramid i en reaktion analog med den af sfingomyelin-syntese, og når den er dannet, kan den methyleres til sfingomyelin. Inositolphosphat ceramider dannes ved transesterificering fra phosphatidylinositol.
Glycosphingolipider modificeres hovedsageligt i Golgi-komplekset, hvor specifikke glycosyltransferaseenzymer deltager i tilsætningen af oligosaccharidkæder i det hydrofile område af ceramidskelettet..
Metabolisme
Nedbrydningen af sfingolipider udføres af enzymerne glucohydrolaser og sfingomyelinaser, som har ansvaret for at fjerne modifikationerne af de polære grupper. På den anden side regenererer ceramidaser langkædede baser fra ceramider.
Gangliosider nedbrydes af et sæt lysosomale enzymer, der katalyserer trin-for-trin-eliminering af sukkerenheder og til sidst producerer et ceramid..
En anden nedbrydningsvej består af internalisering af sfingolipider i endocytiske vesikler, der sendes tilbage til plasmamembranen eller transporteres til lysosomerne, hvor de nedbrydes af specifikke syrehydrolaser..
Ikke alle langkædede baser genbruges, det endoplasmatiske retikulum har en rute for deres terminale nedbrydning. Denne nedbrydningsmekanisme består af phosphorylering i stedet for acylering af LCB'er, hvilket giver anledning til signalmolekyler, der kan være opløselige substrater for lyaseenzymer, der skærer LCBs-phosphat til dannelse af acyloaldehyder og phosphoethanolamin..
Regulering
Metabolismen af disse lipider er reguleret på forskellige niveauer, en af dem er de enzymer, der har ansvaret for syntese, deres posttranslationsmodifikationer og deres allosteriske mekanismer..
Nogle reguleringsmekanismer er celle-specifikke, enten for at kontrollere tidspunktet for celleudvikling, hvori de produceres, eller som reaktion på specifikke signaler..
Referencer
- Bartke, N., & Hannun, Y. (2009). Bioaktive sfingolipider: Metabolisme og funktion. Journal of Lipid Research, halvtreds, 19.
- Breslow, D. K. (2013). Sphingolipid Homeostase i det endoplasmatiske retikulum og videre. Cold Spring Harbour Perspectives in Biology, 5(4), a013326.
- Futerman, A. H., & Hannun, Y. A. (2004). Den komplekse levetid for enkle sfingolipider. EMBO-rapporter, 5(8), 777-782.
- Harrison, P. J., Dunn, T., og Campopiano, D. J. (2018). Sphingolipid biosyntese hos mennesker og mikrober. Naturlige produktrapporter, 35(9), 921-954.
- Lahiri, S., og Futerman, A. H. (2007). Metabolisme og funktion af sfingolipider og glycosphingolipider. Cellular og Molecular Life Sciences, 64(17), 2270-2284.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Bretscher, A., Ploegh, H., Martin, K. (2003). Molekylær cellebiologi (5. udgave). Freeman, W. H. & Company.
- Luckey, M. (2008). Membran strukturel biologi: med biokemiske og biofysiske fundamenter. Cambridge University Press. Hentet fra www.cambridge.org/9780521856553
- Merrill, A. H. (2011). Sphingolipid og glycosphingolipid metaboliske veje i sphingolipidomics æra. Kemiske anmeldelser, 111(10), 6387-6422.
- Nelson, D. L. og Cox, M. M. (2009). Lehninger Principper for biokemi. Omega-udgaver (5. udgave).
- Vance, J. E., & Vance, D. E. (2008). Biokemi af lipider, lipoproteiner og membraner. I New Comprehensive Biochemistry Vol.36 (4. udgave). Elsevier.



Endnu ingen kommentarer