
Calciumoxalat (CaC2O4) egenskaber, struktur, anvendelser, risici
Det calciumoxalat Det er en organisk forbindelse dannet af grundstofferne kulstof (C), ilt (O) og calcium (Ca). Dens kemiske formel er CaCtoELLER4. Det findes generelt i dets tre hydratiserede former: mono-, di- og trihydrat. Det vil sige med henholdsvis et, to eller tre vandmolekyler i dets krystallinske struktur..
Calciumoxalat findes i mineraler, planter, svampe og andre levende væsener såsom pattedyr og endda hos mennesker som en konsekvens af metabolismen af nogle proteiner. Det kan findes i urinen hos mennesker og nogle dyr.
Nogle fødevarer som spinat, rabarber, soja og chokolade indeholder en masse oxalater, og når følsomme mennesker spiser dem, kan der dannes calciumoxalatsten i deres nyrer..
CaC-sten kan forhindrestoELLER4 i nyrerne, hvis de indtager en masse væsker, især vand, undgår mad med højt indhold af oxalater og indtager dem, der er rige på calcium og magnesium.
Calciumoxalat danner uønsket skala i rør og tanke i processer såsom fremstilling af papirmasse og papir og også i bryggerier.
Artikelindeks
- 1 Struktur
- 2 Nomenklatur
- 3 egenskaber
- 3.1 Fysisk tilstand
- 3.2 Molekylvægt
- 3.3 Smeltepunkt
- 3.4 Specifik vægt
- 3.5 Opløselighed
- 3,6 pH
- 3.7 Kemiske egenskaber
- 4 Tilstedeværelse i naturen
- 4.1 I mineraler
- 4.2 I planter og svampe
- 5 Tilstedeværelse i menneskekroppen og pattedyr
- 5.1 Hos mennesker
- 5.2 Faktorer, der påvirker udseendet af sten i nyrerne
- 5.3 Måder at undgå dannelse af calciumoxalatsten på
- 5.4 Hos dyr
- 5.5 Kropsrespons på overskydende oxalat
- 6 anvendelser
- 6.1 Problemer i nogle processer
- 7 risici
- 8 Referencer
Struktur
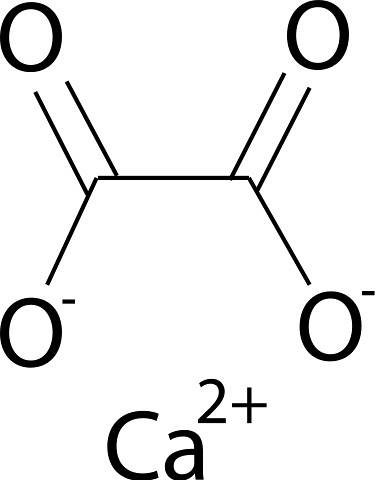
Calciumoxalat dannes af calciumionen Cato+ og oxalationen CtoELLER4to-. Oxalatanionen består af to carbonatomer og fire oxygenatomer. De negative ladninger af oxalatanionen findes på iltatomerne.
Nomenklatur
- Calciumoxalat
- Oxalsyre calciumsalt
- Ethandiosyre calciumsalt
Ejendomme
Fysisk tilstand
Farveløst, hvidt, gult eller brunt krystallinsk fast stof, der kan være i tre forskellige hydratiserede former.
Molekylær vægt
128,1 g / mol
Smeltepunkt
Calciumoxalatmonohydrat nedbrydes ved 200 ° C.
Specifik vægt
Monohydrat CaCtoELLER4 •HtoO = 2,22 g / cm3
Dihydrat CaCtoELLER4 •2HtoO = 1,94 g / cm3
Trihydrat CaCtoELLER4 •3HtoO = 1,87 g / cm3
Opløselighed
Næsten uopløselig i vand: 0,00061 g / 100 g vand ved 20 ° C. Monohydrat opløses i fortyndet syre.
pH
Vandige opløsninger af calciumoxalat er svagt basiske.
Kemiske egenskaber
Calciumoxalat er calciumsaltet af oxalsyre. Dette er et naturligt biprodukt af stofskiftet, så det er meget rigeligt i den menneskelige krop og er en del af mange fødevarer.
Oxalsyre og dens konjugatbase, oxalat, er stærkt oxiderede organiske forbindelser med kraftig chelateringsaktivitet, det vil sige, de kan let kombineres med positive ioner med ladninger på +2 eller +3.
Dens vandige opløsninger er svagt basiske, fordi oxalationen har tendens til at optage H-protoner.+ fra vand, som frigiver OH-ioner-. Efter at have taget to protoner H+ oxalationen bliver oxalsyre HtoCtoELLER4:
CtoELLER4to- + HtoO → HCtoELLER4- + Åh-
HCtoELLER4- + HtoO → HtoCtoELLER4 + Åh-
Tilstedeværelse i naturen
I mineraler
Calciumoxalat er det mest almindelige oxalat og kommer i form af mineralerne whewellite, weddellite og caoxite..
Whewellite er monohydratet CaCtoELLER4 •HtoEller og er den mest stabile form af denne forbindelse.

Weddellite er dihydratet CaCtoELLER4 •2HtoO og er mindre stabil end monohydrat.

Caoxite er calciumoxalattrihydrat CaCtoELLER4 •3HtoELLER.
I planter og svampe
Calciumoxalat findes forbundet med tør jord og blade, også med patogene svampe, fri, i symbiose eller forbundet med planter. I sidstnævnte dannes krystaller ved udfældning af calcium i form af dets oxalat..
CaC-dannelsetoELLER4 af svampe har en vigtig indflydelse på jordens biologiske og geokemiske processer, da det udgør en reserve af calcium til økosystemet.
Tilstedeværelse i menneskekroppen og pattedyr
Oxalat stammer fra leveren, i røde blodlegemer eller erythrocytter og i mindre grad i nyrerne. Det dannes ved metabolismen af aminosyrer (såsom phenylalanin og tryptophan) og ved oxidation af glyoxaldialdehyd,.
C-vitamin kan også omdannes til oxalat, når det udfører dets antioxidantfunktion.
Calciumoxalat findes i sten, der dannes i nyrerne hos mennesker eller dyr med nyresygdom..
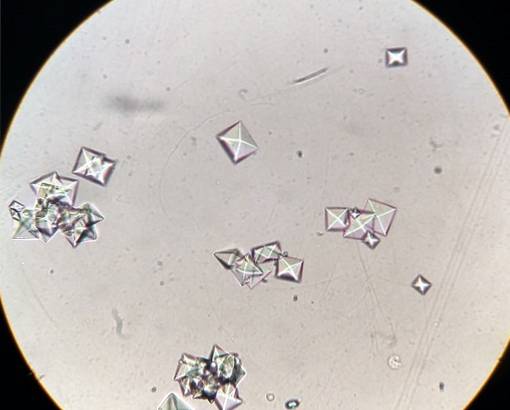
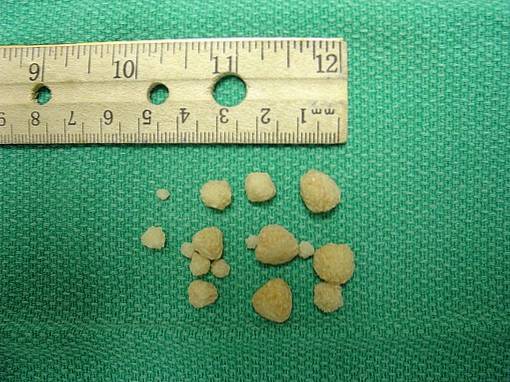
De såkaldte calciumoxalatsten eller sten dannes ved krystallisering eller aggregering af CaCtoELLER4 i urin overmættet med calcium og oxalat. Dette betyder, at urinen indeholder så meget calcium og oxalat, at det ikke er muligt for denne forbindelse at forblive opløst, men snarere at udfælde eller passere til fast tilstand i form af krystaller..
Hos mennesker
Dannelsen af grus eller sten i nyrerne er en sygdom kaldet nefrolithiasis; angriber ca. 10% af befolkningen, og ca. 75% af disse sten består af calciumoxalat CaCtoELLER4.
Dannelsen og væksten af calciumoxalatkrystaller i nyrerne opstår, fordi urinen hos nogle mennesker er overmættet med dette salt. Calciumoxalat udvikler sig i sur urin ved pH mindre end 6,0.
Overmætning opstår, når udskillelse eller eliminering af dette salt (som er meget dårligt opløseligt i vand) i urinen sker i et lille volumen vand..
Faktorer, der påvirker udseendet af sten i nyrerne
Blandt de faktorer, der favoriserer dannelsen af calciumoxalatkorn, er overskydende calcium i urinen eller hyperkalciuri, overskydende oxalat i urinen eller hyperoxaluri, grundstoffer fra kosten og fraværet af hæmmere.
Overskydende oxalat kan forekomme, når der spises store mængder spinat, rabarber, soja, nødder og chokolade..

Der er imidlertid stoffer, der hæmmer eller forhindrer dannelse af sten. Forbindelser, der forhindrer stendannelse, inkluderer små molekyler, såsom citrat og pyrophosphat, og store molekyler, såsom glycoproteiner og proteoglycaner..
Måder at undgå dannelse af calciumoxalatsten på
En god strategi for at forhindre gentagelse af korn eller calciumoxalatsten inkluderer at øge dit væskeindtag, øge dit indtag af calciumrige fødevarer (såsom mejeri) og begrænse bordsalt (NaCl), animalsk protein og fødevarer rig på oxalat.
Hos dyr
Siden begyndelsen af året 2000 er der observeret en stigning i calciumoxalatsten i urinsystemet hos katte og hunde. Det ser ud til, at dette afhænger af den diæt, som disse dyr spiser, og har at gøre med surhedsgraden i urinen og magnesium (Mg) -mangel.
Kropsrespons på overskydende oxalat
Der er beviser for, at både mennesker og dyr reagerer på overskydende oxalat ved at øge antallet af bakterier, der kan nedbryde oxalat..
Nogle af disse bakterier er Oxalobacter formigenes, Bifidobacterium sp., Porphyromonas gingivalis Y Bacillus sp., blandt andre og er naturligt til stede i tarmen.
Ansøgninger
Ifølge kendte kilder anvendes calciumoxalat til keramisk belægning.
Det er blevet brugt til at belægge kalkstenskulpturer og andre kunstneriske elementer, og det har vist sig at forbedre materialets hårdhed, mindske dets porøsitet og øge dets modstandsdygtighed over for syrer og baser..

Problemer i nogle processer
I papirmasse- og papirindustrien kan calciumoxalat danne skala, hvilket medfører mange problemer i processen..
For at forhindre dets dannelse i kanaler eller rør til industrielle processer er den enzymatiske nedbrydning af oxalsyre blevet foreslået ved hjælp af enzymer såsom oxalatoxidase..
Det har også en tendens til at akkumulere som sten i beholderne, hvor øl fremstilles, hvorfra det skal fjernes for at undgå dannelsen af mikroorganismer, der kan give en ubehagelig smag til drikken..
Risici
I høje koncentrationer kan oxalat forårsage død hos dyr og lejlighedsvis hos mennesker, hovedsageligt på grund af dets ætsende virkning..
Ophobning af oxalat og dets konjugerede syre, oxalsyre, kan forårsage lidelser som hjertefejl, calciumoxalatsten, nyresvigt og endda død på grund af toksicitet.
Referencer
- Glasauer, S.M. et al. (2013). Metaller og metalloider, transformation af mikroorganismer. Oxalater. I referencemodul i Earth Systems and Environmental Sciences. Gendannet fra sciencedirect.com.
- Baumann, J. M. og Casella, R. (2019). Forebyggelse af calciumnephrolithiasis: Indflydelse af diurese på calciumoxalatkrystallisation i urin. Adv Prev Med, 2019; 2019: 3234867. Gendannet fra ncbi.nlm.nih.gov.
- Breshears, M.A. og Confer, A.W. (2017). Urinvejene. Calciumoxalat Calculi. In Pathologic Basis of Veterinary Disease (Sixth Edition). Gendannet fra sciencedirect.com.
- Huang, Y. er al. (2019). Tge Håndtering af oxalat i kroppen og tge Oprindelsen af oxalat i calciumoxalatsten. Urol Int, 5. december 2019: 1-10. Gendannet fra ncbi.nlm.nih.gov.
- Nilvebrant, N.-O. et al. (2002). Bioteknologi inden for papirmasse- og papirindustrien. Igangværende inden for bioteknologi. Gendannet fra sciencedirect.com.
- Pahira, J.J. og Pevzner, M. (2007). Nefrolithiasis. Calcium Stones. I Penn Clinical Manual of Urology. Gendannet fra sciencedirect.com.
- Worcester, E. M. (1994). Urin Calcium Oxalate Crystal Growth Inhibitors. J Am Soc Nephrol 1994 nov; 5 (5 Suppl 1): S46-53). Gendannet fra jasn.asnjournals.org.
- Finkielstein, V.A. og Goldfarb, D.S. (2006). Strategier til forebyggelse af calciumoxalatsten. Gendannet fra ncbi.nlm.nih.gov.
- OS. National Library of Medicine. (2019). Calciumoxalat. Gendannet fra pubchem.ncbi.nlm.nih.gov.
- Peck, A.B. et al. (2015). Oxalatnedbrydende mikroorganismer eller oxalatnedbrydende enzymer: hvilken er den fremtidige terapi til enzymatisk opløsning af calciumoxalaturolitter i tilbagevendende stensygdom? Urolithiasis, 2016 feb; 44 (1): 27-32. Gendannet fra ncbi.nlm.nih.gov.
- Holames, R.P. et al. (2016). Sænkning af urinoxalatudskillelse for at mindske calciumoxalatstenesygdom. Urolithiasis. 2016 februar; 44 (1); 27-32. Gendannet fra ncbi.nlm.nih.gov.
- Cezar, T.M. (1998). Calciumoxalat: En overfladebehandling for kalksten. Journal of Conservation and Museum Studies 4, s. 6-10. Gendannet fra jcms-journal.com.
- Wikimedia (2019). Calciumoxalat. Gendannet fra en.wikipedia.org.



Endnu ingen kommentarer