
Aldehyder struktur, egenskaber, anvendelser og eksempler

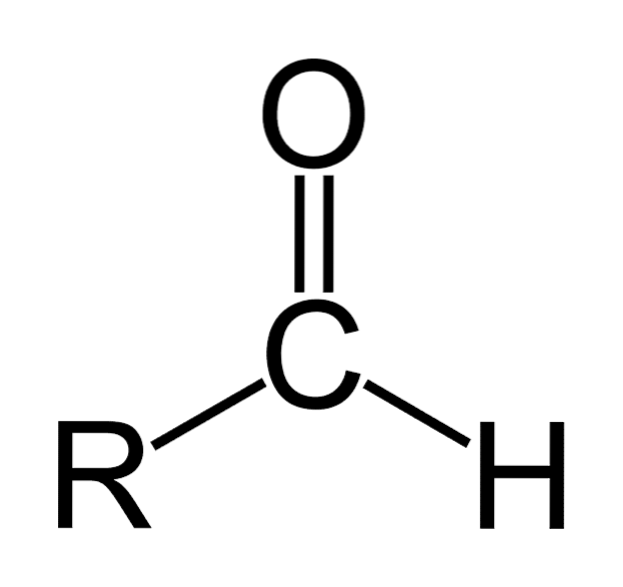
Det aldehyder de er organiske forbindelser, der har den almene formel RCHO. R repræsenterer en alifatisk eller aromatisk kæde; C til carbon; O til ilt og H til brint. De er karakteriseret ved at have en carbonylgruppe som ketoner og carboxylsyrer, hvorfor aldehyder også kaldes carbonylforbindelser.
Carbonylgruppen giver aldehydet mange af dets egenskaber. De er forbindelser, der let oxideres og er meget reaktive over for nukleofile tilsætninger. Dobbeltbindingen af carbonylgruppen (C = O) har to atomer, der har forskelle i deres grådighed over elektroner (elektronegativitet).
Ilt tiltrækker elektroner med større kraft end kulstof, så elektronskyen bevæger sig mod det, hvilket gør dobbeltbindingen mellem kulstof og ilt polar i naturen med et betydeligt dipolmoment. Dette gør aldehyder til polære forbindelser..
Aldehydernes polaritet vil påvirke deres fysiske egenskaber. Kogepunktet og opløseligheden af aldehyder i vand er højere end ikke-polære kemiske forbindelser med lignende molekylvægte, sådan er det tilfældet med kulbrinter..
Aldhyder med mindre end fem carbonatomer er opløselige i vand, da der dannes hydrogenbindinger mellem carbonylgruppens ilt og vandmolekylet. At øge antallet af carbonatomer i carbonhydridkæden frembringer imidlertid en stigning i den ikke-polære del af aldehydet, hvilket gør det mindre opløseligt i vand..
Men hvordan er de, og hvor kommer de fra? Selvom dens natur i det væsentlige afhænger af carbonylgruppen, bidrager resten af molekylstrukturen også meget til helheden. Således kan de have en hvilken som helst størrelse, lille eller stor, eller endda et makromolekyle kan have regioner, hvor aldehydernes karakter dominerer..
Som med alle kemiske forbindelser er der således "behagelige" aldehyder og andre bitre. De kan findes i naturlige kilder eller syntetiseres i stor skala. Eksempler på aldehyder er vanillin, der er meget til stede i is (topbillede) og acetaldehyd, som tilføjer smag til alkoholholdige drikkevarer..
Artikelindeks
- 1 Kemisk struktur
- 2 Fysiske og kemiske egenskaber
- 2.1 Smeltepunkter
- 2.2 Kogepunkter
- 2.3 Opløselighed i vand udtrykt i g / 100 g H2O
- 3 Reaktivitet
- 3.1 Oxidationsreaktion
- 3.2 Reduktion til alkohol
- 3.3 Reduktion til kulbrinter
- 3.4 Nukleofil tilsætning
- 4 Nomenklatur
- 5 anvendelser
- 5.1 Formaldehyd
- 5.2 Bakelit
- 5.3 Krydsfiner
- 5.4 Polyurethan
- 5.5 Butyraldehyd
- 5.6 Acetaldehyd
- 5.7 Syntese
- 6 Eksempler på aldehyder
- 6.1 Glutaraldehyd
- 6.2 Benzaldehyd
- 6.3 Glyceraldehyd
- 6.4 Glyceraldehyd-3-phosphat
- 6,5 11-cis-retinal
- 6.6 Pyridoxalphosphat (vitamin B6)
- 6.7 Salicylaldehyd
- 7 Referencer
Kemisk struktur

Aldehyder består af en carbonyl (C = O), hvortil et hydrogenatom er direkte bundet. Dette adskiller det fra andre organiske forbindelser såsom ketoner (RtoC = O) og carboxylsyrer (RCOOH).
Det øverste billede viser den molekylære struktur omkring -CHO, en formylgruppe. Formylgruppen er flad, fordi kulstof og ilt har SP-hybridiseringto. Denne planaritet gør den modtagelig for angreb af nukleofile arter, og derfor oxideres den let..
Hvad henviser denne oxidation til? Til dannelsen af en binding med ethvert andet atom, der er mere elektronegativt end kulstof; og i tilfælde af aldehyder er det ilt. Således oxideres aldehydet til en carboxylsyre, -COOH. Hvad hvis aldehydet blev reduceret? En primær alkohol ville blive dannet i stedet for, ROH.
Aldehyder produceres kun af primære alkoholer: dem, hvor OH-gruppen er i slutningen af en kæde. Tilsvarende formylgruppen for evigt er ved enden af en kæde eller stikker ud fra den eller ringen som en substituent (hvis der er andre vigtigere grupper, såsom -COOH).
Fysiske og kemiske egenskaber
Da de er polære forbindelser, er deres smeltepunkter højere end for ikke-polære forbindelser. Aldehydmolekyler er ikke i stand til intermolekylær binding gennem hydrogenbindinger, da de kun har carbonatomer bundet til hydrogenatomer..
På grund af ovenstående har aldehyder lavere kogepunkter end alkoholer og carboxylsyrer.
Smeltepunkter
Formaldehyd -92; Acetaldehyd -121; Propionaldehyd -81; n-butyraldehyd -99; n-Valeraldehyd -91; Caproaldehyd -; Heptaldehyd - 42; Phenylacetaldehyd -; Benzaldehyd -26.
Kogepunkter
Formaldehyd -21; Acetaldehyd 20; Propionaldehyd 49; n-butyraldehyd 76; n-Valeraldehyd 103; Caproaldehyd 131; Heptaldehyd 155; Phenylacetaldehyd 194; Benzaldehyd 178.
Opløselighed i vand udtrykt i g / 100 g HtoELLER
Formaldehyd, meget opløselig; Uendelig acetaldehyd; Propionaldehyd, 16; n-butyraldehyd, 7; n-Valeraldehyd, let opløselig; caproaldehyd, let opløselig; Let opløselig phenylacetaldehyd; Benzaldehyd, 0,3.
Kogepunkterne for aldehyder har tendens til at stige direkte med molekylvægt. Tværtimod er der en tendens til at nedsætte opløseligheden af aldehyder i vand, når deres molekylvægt stiger. Dette afspejles i de fysiske konstanter af de netop nævnte aldehyder..
Reaktivitet
Oxidationsreaktion
Aldehyder kan oxideres til den tilsvarende carboxylsyre i nærværelse af en hvilken som helst af disse forbindelser: Ag (NH3)to, KMnO4 okaytoCrtoELLER7.
Reduktion til alkohol
De kan hydrogeneres ved hjælp af nikkel-, platin- eller palladiumkatalysatorer. Således bliver C = O C-OH.
Reduktion til kulbrinter
I nærværelse af Zn (Hg), koncentreret HCI eller i NHtoNHto aldehyder mister carbonylgruppen og bliver carbonhydrider.
Nukleofil tilsætning
Der er flere forbindelser, der tilsættes til carbonylgruppen, blandt dem er: Grignard-reagenser, cyanid, derivater af ammoniak og alkoholer.
Nomenklatur
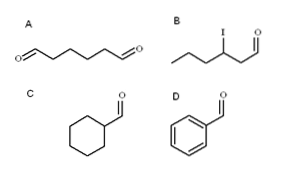
Fire aldehyder er illustreret i ovenstående billede. Hvordan navngives de??
Da de er oxiderede primære alkoholer, ændres alkoholens navn fra -ol til -al. Methanol (CH3OH) hvis oxideret til CH3CHO kaldes methanal (formaldehyd); CH3CHtoCHO ethanal (acetaldehyd); CH3CHtoCHtoCHO propanal og CH3CHtoCHtoCHtoCHO butanal.
Alle de nyligt navngivne aldehyder har -CHO-gruppen i slutningen af kæden. Når den findes i begge ender, som i A, forberedes slutningen -al med præfikset di-. Da A har seks carbonatomer (tæller dem fra begge formylgrupper), stammer det fra 1-hexanol, og dets navn er derfor: hexanurskive.
Når der er en substituent, såsom en alkylgruppe, en dobbelt- eller tredobbeltbinding eller et halogen, er kulstofferne i hovedkæden anført, hvilket giver -CHO tallet 1. Aldehyd B kaldes således: 3-iodhexanal.
I aldehyder C og D har gruppen -CHO imidlertid ingen prioritet til at identificere sådanne forbindelser fra andre. C er en cycloalkan, medens D en benzen, begge med en af deres H'er substitueret med en formylgruppe.
I dem, da hovedstrukturen er cyklisk, hedder formylgruppen carbaldehyd. Således er C cyclohexancarbaldehyd, og D er benzencarbaldehyd (bedre kendt som benzaldehyd).
Ansøgninger
Aldehyder findes i naturen, der er i stand til at give behagelige smag, sådan er det tilfældet med kanelaldehyd, der er ansvarlig for den karakteristiske smag af kanel. Derfor bruges de ofte som kunstige smagsstoffer i mange produkter såsom slik eller mad..
Formaldehyd
Formaldehyd er det mest industrielt producerede aldehyd. Formaldehydet opnået ved oxidation af methanol anvendes i en 37% opløsning af gassen i vand under navnet formalin. Dette bruges til garvning af huder og til bevarelse og balsamering af lig..
Ligeledes anvendes formaldehyd som et germicid, fungicid og insekticid til planter og grøntsager. Den største nytte er imidlertid bidraget til produktionen af polymert materiale. Plasten kaldet bakelit syntetiseres ved reaktionen mellem formaldehyd og phenol.
Bakelit
Bakelit er en meget hård polymer med en tredimensionel struktur, der bruges i mange husholdningsredskaber, såsom håndtag til gryder, pander, kaffemaskiner, knive osv..
Bakelitlignende polymerer er fremstillet af formaldehyd i kombination med forbindelserne urinstof og melamin. Disse polymerer anvendes ikke kun som plast, men også som klæbende lim og belægningsmateriale..
Krydsfiner
Krydsfiner er det kommercielle navn på et materiale dannet af tynde træplader, der er forbundet med polymerer fremstillet af formaldehyd. Mærkerne Formica og Melmac fremstilles med sidstnævntes deltagelse. Formica er et plastmateriale, der anvendes til møbelbeklædning.
Melmac plast bruges til at fremstille tallerkener, glas, kopper osv. Formaldehyd er råmaterialet til syntese af forbindelsen methylen-diphenyl-diisocyanat (MDI), en forløber for polyurethan.
Polyurethan
Polyurethan bruges som isolator i køleskabe og frysere, polstring til møbler, madrasser, belægninger, klæbemidler, såler osv..
Butyraldehyd
Butyraldehyd er den vigtigste forløber for syntesen af 2-ethylhexanol, der anvendes som blødgøringsmiddel. Det har en behagelig æblearoma, der gør det muligt at bruge det i mad som aroma.
Det bruges også til produktion af gummiacceleratorer. Gribe ind som et mellemreagens i fremstillingen af opløsningsmidler.
Acetaldehyd
Acetaldehyd blev anvendt til produktion af eddikesyre. Men denne rolle af acetaldehyd er blevet mindre i betydning, da den er blevet fortrængt af carbonyleringsprocessen af methanol..
Syntese
Andre aldehyder er forløbere for oxoalkoholer, der anvendes til fremstilling af vaskemidler. Såkaldte oxoalkoholer fremstilles ved at tilsætte carbonmonoxid og hydrogen til en olefin for at opnå et aldehyd. Og til sidst hydreres aldehydet for at opnå alkoholen.
Nogle aldehyder anvendes til fremstilling af parfume, som det er tilfældet med Chanel nr. 5. Mange aldehyder af naturlig oprindelse har behagelig lugt, for eksempel: heptanal har en grøn græsluft; den octanal en orange lugt; den nonanal en lugt af roser og citralen en lugt af kalk.
Eksempler på aldehyder
Glutaraldehyd
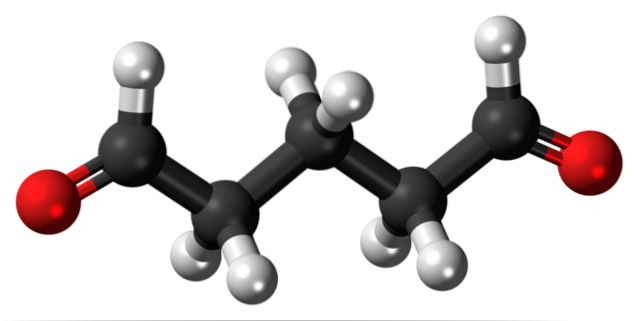
Glutaraldehyd har to formylgrupper i sin struktur i begge ender.
Markedsført under navnet Cidex eller Glutaral, det bruges som et desinfektionsmiddel til sterilisering af kirurgiske instrumenter. Det bruges til at behandle vorter på fødderne og anvende det som en væske. Det bruges også som et vævsfastgørelsesmiddel i histologi- og patologilaboratorier..
Benzaldehyd
Det er det enkleste aromatiske aldehyd, der dannes af en benzenring, hvor en formylgruppe er bundet.
Det findes i mandelolie, derfor er dets karakteristiske lugt, der gør det muligt at bruge det som madaroma. Derudover bruges det til syntesen af organiske forbindelser relateret til fremstilling af lægemidler og til fremstilling af plast..
Glyceraldehyd
Det er en aldotriose, et sukker, der består af tre kulstofatomer. Den har to isomerer kaldet D- og L-enantiomerer.Glyceraldehyd er det første monosaccharid, der opnås i fotosyntese i den mørke fase (Calvin-cyklus)..
Glyceraldehyd-3-phosphat
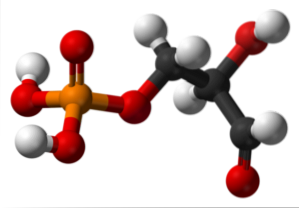
Det øverste billede illustrerer strukturen af glyceraldehyd-3-phosphat. De røde kugler ved siden af den gule svarer til fosfatgruppen, mens de sorte kulstofskelettet. Den røde kugle bundet til den hvide er OH-gruppen, men når den er bundet til den sorte kugle og den sidstnævnte til den hvide, er det CHO-gruppen.
Glyceraldehyd-3-phosphat er involveret i glykolyse, en metabolisk proces, hvor glukose nedbrydes til pyruvinsyre med produktionen af ATP, et energireservoir af levende væsener. Ud over produktionen af NADH, et biologisk reduktionsmiddel.
I glykolyse stammer glyceraldehyd-3-phosphat og dihydroacetonphosphat fra spaltningen af D-fructose-1-6-bisphosphat
Glyceraldehyd-3-phosphat er involveret i den metaboliske proces kendt som pentosecyklussen. I det genereres NADPH, en vigtig biologisk reduktionsmiddel..
11-cis-nethind
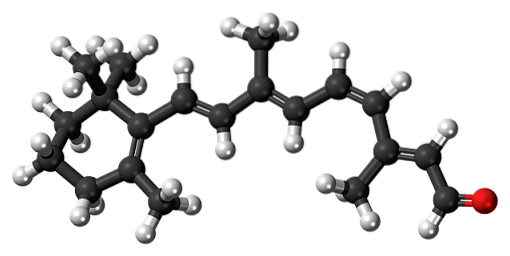
Β-caroten er et naturligt pigment, der findes i forskellige grøntsager, især gulerødder. Det gennemgår en oxidativ nedbrydning i leveren og omdannes således til retinolalkohol eller vitamin A. Oxidationen af vitamin A og den efterfølgende isomerisering af en af dets dobbeltbindinger danner 11-cis-retinal aldehyd.
Pyridoxalphosphat (vitamin B6)
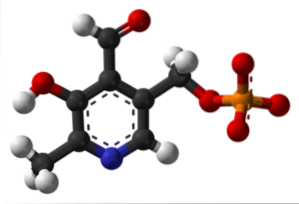
Det er en protesegruppe bundet til flere enzymer, som er den aktive form af vitamin B6 og deltager i synteseprocessen af den hæmmende neurotransmitter GABA.
Hvor er formylgruppen i din struktur? Bemærk, at dette adskiller sig fra resten af grupperne, der er knyttet til den aromatiske ring.
Salicylaldehyd
Det er et råmateriale til syntese af acetylsalicylsyre, et smertestillende og antipyretisk lægemiddel kendt som Aspirin..
Referencer
- Robert C. Neuman, Jr. kapitel 13, carbonylforbindelser: ketoner, aldehyder, carboxylsyrer. [PDF]. Hentet fra: chem.ucr.edu
- Germán Fernández. (14. september 2009). Nomenklatur for aldehyder. Hentet fra: quimicaorganica.net
- T.W. Graham Solomons, Craigh B. Fryhle. Organisk kemi. (Tiende udgave, s. 729-731) Wiley Plus.
- Jerry March og William H. Brown. (31. december 2015). Aldehyd. Hentet fra: britannica.com
- Wikipedia. (2018). Aldehyder. Hentet fra: https://en.wikipedia.org/wiki/Aldehyde
- Morrison, R. T. og Boyd, R. N. (1990). Organic Chemistry Femte udgave. Redaktionel Addison-Wesley Iberoamericana.
- Carey, F. A. (2006). Organic Chemistry Sixth Edition. Mc Graw Hill Publishing House.
- Mathews, Ch. K., Van Holde, K. E. og Athern, K. G. (2002). Biokemi. Tredje udgave. Udgiver Pearson Adisson Wesley.

Endnu ingen kommentarer