
Bakteriostatiske egenskaber, virkningsmekanismer og eksempler

Narkotika bakteriostatisk De er antibiotika, der reversibelt stopper reproduktion og vækst af bakterier. De bruges mod infektioner af følsomme mikroorganismer og hos patienter med et kompetent immunsystem.
Pasteur og Joubert var de første til at genkende den potentielle terapeutiske virkning af nogle mikrobielle produkter. I 1877 offentliggjorde de deres observationer, hvor de viste, hvordan almindelige mikroorganismer kunne stoppe væksten af Anthrax-bacillus i urinen..
Streptomycin, chloramphenicol og chlortetracyclin blev identificeret i slutningen af anden verdenskrig. Siden den tid er der udviklet hundreder af antimikrobielle lægemidler, og disse er tilgængelige til behandling af forskellige smitsomme sygdomme..
I øjeblikket er antibiotika et af de mest anvendte lægemidler i medicinsk behandling, mere end 30% af indlagte patienter får antibiotika. De er dog et af de mest misbrugte stoffer af læger og patienter. Unødvendige og misadministrerede behandlinger med disse lægemidler har været årsagen til udviklingen af bakterieresistens mod mange antibiotika.
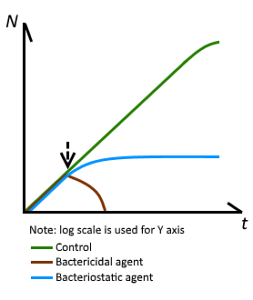
Antimikrobielle stoffer klassificeres i henhold til deres generelle virkningsmekanisme i baktericider (dem, der dræber bakterier) og bakteriostatier (dem, der hæmmer deres vækst og reproduktion). Mens denne differentiering er tydelig, når den testes i vitro, når den anvendes i terapi er denne sondring ikke så defineret.
Artikelindeks
- 1 Funktioner
- 2 Handlingsmekanisme
- 3 Virkningsmekanisme i tilfælde af bakteriostatika
- 3.1 Hæmning af aktiveringsfasen
- 3.2 Hæmning af initieringen af proteinsyntese
- 3.3 Hæmning af forlængelse med forskellige mekanismer
- 4 eksempler på hver virkningsmekanisme og følsomme mikroorganismer
- 4.1 Aktiviseringsfasehæmmere
- 4.2 Hæmning af initieringen af proteinsyntese
- 4.3 Hæmning af bindingen af aminoacyl-tRNA til ribosomet
- 4.4 Forlængelseshæmmere
- 4.5 Makrolider
- 5 Referencer
Egenskaber
Som forklaret ovenfor kan antimikrobielle lægemidler klassificeres i dem, der er i stand til at dræbe følsomme bakterier, der kaldes baktericider, og dem, der reversibelt hæmmer deres vækst og udvikling, kaldet bakteriostatier..
I øjeblikket betragtes denne differentiering set fra et klinisk synspunkt som noget diffus. Af denne grund siges det, at et givet antibiotikum fortrinsvis virker som en bakteriostatisk eller et baktericid..
Derfor kan det samme antibiotikum have en dobbelt effekt (bakteriostatisk eller bakteriedræbende) afhængigt af visse betingelser, såsom den koncentration, det kan nå i det område, hvor dets effekt er nødvendig, og den affinitet, den har for den involverede mikroorganisme..
Generelt er bakteriostatika med undtagelse af aminoglycosider antibiotika, der interfererer med proteinsyntesen af følsomme bakterier. Hvis kroppens immunsystem er et kompetent system, er det nok at hæmme væksten og reproduktionen af en bakterie, så den kan eliminere den.
På den anden side kan baktericider have forskellige virkningsmekanismer: de kan interferere med syntesen af bakteriecellevæggen, ændre den cytoplasmatiske membran eller interferere med nogle processer relateret til syntesen og metabolismen af bakterielt DNA..
Handlingsmekanisme
Flere ordninger er blevet brugt til at klassificere antimikrobielle lægemidler, blandt dem er grupperingen af disse lægemidler i henhold til fælles handlingsmekanismer. I henhold til deres virkningsmekanisme klassificeres antibiotika således i:
- Antibiotika, der hæmmer syntesen af bakterievæggen: blandt disse er penicilliner og cephalosporiner, cycloserin, vancomycin og bacitracin.
- Antibiotika, der ændrer mikroorganismers membranpermeabilitet, hvilket tillader intracellulære forbindelser at slippe ud: dette inkluderer vaskemidler som polymyxin og polyen.
- Midler, der påvirker funktionen af 30S og 50S ribosomale underenheder og forårsager en reversibel hæmning af proteinsyntese: disse er bakteriostatiske lægemidler. Eksempler chloramphenicol, tetracycliner, erythromycin, clindamycin og pristanamycin.
- Midler, der binder til 30S-underenheden og ændrer proteinsyntese og til sidst forårsager bakteriens død: blandt disse er aminoglykosider.
- Antibiotika, der påvirker nukleinsyremetabolismen, hæmmer RNA-polymerase: rifamycin er et eksempel.
- Antimetabolitmidler, der hæmmer folatmetabolismenzymer - eksempler på disse er trimethoprin og sulfonamider.
Handlingsmekanisme i tilfælde af bakteriostatika
Virkningsmekanismen for bakteriostatiske midler har at gøre med ændringen af proteinsyntesen af målbakterierne. Dette opnås ved forskellige mekanismer:
Hæmning af aktiveringsfase
- Isoleucyl-tRNA-synthetaseenzyminhibitorer.
Hæmning af initieringen af proteinsyntese
- Undgå dannelse af 70S-initieringskomplekset, eller bind til 50S-underenheden.
- Hæmning af bindingen af aminoacyl-tRNA til ribosomet.
Hæmning af forlængelse ved forskellige mekanismer
- Forstyrrer transpeptidationsprocessen.
- Interfererer med peptidyltransferase i 23S rRNA af 50S underenheden af ribosomet.
- Hæmning af forlængelsesfaktor G-translokation.
Et separat tilfælde inkluderer virkningsmekanismen for aminoglycosider, da de virker på 30S ribosomal underenhed og således interfererer med proteinsyntese og derfor er bakteriostatiske. Imidlertid udøver de en effekt på membranen af nogle bakterier, hvilket forårsager en hovedsagelig bakteriedræbende virkning..
Eksempler på hver virkningsmekanisme og følsomme mikroorganismer
Hæmmere af aktiveringsfase
Mucopirocin er et bakteriostatisk antibiotikum, der er i stand til konkurrencedygtigt at hæmme enzymet isoleucyl-tRNA-synthetase og dermed hæmme inkorporeringen af isoleucin og standse syntesen..
Dette antibiotikum syntetiseres af nogle arter af Pseudomonas, så det ekstraheres derfra. Det har en særlig kraftig virkning mod gram-positive bakterier. Det bruges primært til hudinfektioner, topisk eller til udryddelse af den sunde bærestatus af Staphylococcus aureus.
Hæmning af initieringen af proteinsyntese
Hos bakterier sker initieringen af syntese med inkorporeringen af methionin som formylmethionin bundet til et tRNA (transfer RNA). 30S og 50S ribosomale underenheder deltager i initieringskomplekset med to vigtige loci: Locus A og Locus P.
Gruppen af oxazolidinoner og aminoglycosider udviser denne virkningsmekanisme. Gruppen af oxazolidinoner er en gruppe syntetiske antibiotika, der for nylig er introduceret i klinisk praksis, og som ikke udviser krydsresistens med andre bakteriostatiske antibiotika..
Linezolid er repræsentanten for oxazolidinoner, den er aktiv over for grampositive bakterier, herunder stammer af Staphylococcus aureus og af Streptococcus spp. multiresistent og har ingen aktivitet mod gram-negative stoffer.
Aminoglycosider er af naturlig oprindelse, de syntetiseres af actinomyceter i jorden eller fra semisyntetiske derivater deraf. De er aktive mod en lang række bakteriearter, især mod aerobe gramnegativer.
Afhængigt af bakterierne og deres placering kan de udvise en bakteriostatisk eller bakteriedræbende virkning..
Hæmning af bindingen af aminoacyl-tRNA til ribosomet
Tetracyclinerne og deres derivater, glycylcyclinerne, er repræsentanter for denne gruppe. De blokerer eller inhiberer Locus A. Tetracycliner kan være naturligt forekommende (streptomyces) eller semisyntetiske; Disse inkluderer doxycyclin, minocyclin og oxytetracyclin..

Tigecyclin er en glycylcyclin afledt af minocyclin med den samme virkningsmekanisme, men med fem gange mere affinitet end minocyclin, og som også påvirker den cytoplasmiske membran. De er meget aktive mod enterokokker og mod mange bakterier, der er resistente over for andre antibiotika.
Forlængelseshæmmere
Chloramphenicol og lincosamider er eksempler på denne gruppe, der virker på locus P. Fusinsyre er et eksempel på en mekanisme til inhibering af translokation af forlængelsesfaktor G. Macrolider og ketolider binder til peptidyltransferase i 23S rRNA af 50S underenhed af ribosomet.
Chloramphenicol og derivater deraf, såsom thiamphenicol, er bredspektret bakteriostatiske antibiotika mod grampositive og negative og mod anaerobe stoffer. De er meget aktive mod salmonella og shigella såvel som mod bakterier, med undtagelse af B. Fragilis.
Det vigtigste lincosamid er clindamycin, som er en bakteriostatisk, men afhængigt af dosis, dets koncentration i målet og typen af mikroorganisme kan det udvise en bakteriedræbende virkning..
Clindamycin er effektivt mod grampositive stoffer, med undtagelse af enterokokker, det er det valg til B. fragilis og det er effektivt mod nogle protozoer som f.eks Plasmodium Y Toxoplasma gondii.
Macrolides
Disse lægemidler indbefatter erythromycin, clarithromycin og roxithromycin (som 14-carbon makrolider) og azithromycin (som 15-carbon-gruppe). Spiramycin, josamycin og midecamycin er eksempler på makrolider med 16 carbonatomer.
Telithromycin er et ketolid afledt af erythromycin. Både makrolider og ketolider er aktive mod gram-positive bakterier, Bordetella pertussis, Haemophilus ducreyi, Neisseria ssp, Helicobacter pylori (clarithromycin er mere effektiv) og Treponemes, blandt andre.
Referencer
- Calvo, J. og Martínez-Martínez, L. (2009). Virkningsmekanismer for antimikrobielle stoffer. Infektiøse sygdomme og klinisk mikrobiologi, 27(1), 44-52.
- Goodman og Gilman, A. (2001). Det farmakologiske grundlag for terapi. Tiende udgave. McGraw-Hill
- Meyers, F. H., Jawetz, E., Goldfien, A., & Schaubert, L. V. (1978). Gennemgang af medicinsk farmakologi. Lange medicinske publikationer.
- Ocampo, P. S., Lázár, V., Papp, B., Arnoldini, M., Zur Wiesch, P. A., Busa-Fekete, R.,… & Bonhoeffer, S. (2014). Antagonisme mellem bakteriostatiske og bakteriedræbende antibiotika er udbredt. Antimikrobielle stoffer og kemoterapi, 58(8), 4573-4582.
- Rodríguez-Julbe, M. C., Ramírez-Ronda, C. H., Arroyo, E., Maldonado, G., Saavedra, S., Meléndez, B.,… & Figueroa, J. (2004). Antibiotika hos ældre voksne. Puerto Rico tidsskrift om sundhedsvidenskab, 2. 3(1).



Endnu ingen kommentarer