
Benzoinstruktur, egenskaber, anvendelser og risici
Det benzoin eller benzoe Det er et hvidt krystallinsk fast stof med en kamferlugt, der består af en organisk forbindelse. Det er en acetone, specifikt en acetophenon med tilstødende hydroxy- og phenylcarboner. Det produceres ved katalytisk kondensation af benzaldehyd med kaliumcyanid som katalysator.
Det blev første gang rapporteret i 1828 af Julius Von Liebig og Friedrich Woehler under deres undersøgelser af en bitter mandelolie, der bestod af benzaldehyd og hydrocyansyre. Den katalytiske syntese af benzoin blev senere forbedret af Nikolai Zinin.
Benzoin er praktisk talt uopløselig i vand, men det er opløseligt i varm alkohol og andre organiske opløsningsmidler, såsom carbondisulfid og acetone..
Dette navn bruges også til at henvise til benzoinharpiks, der fås fra træet Styrax benzoin. Harpiksen indeholder benzoesyre, phenylpropionsyre, benzaldehyd, kanelsyre, benzylbenzoat og vanillin, hvilket giver den en vanilje-lugt..
Denne essentielle olie bør ikke forveksles med forbindelsen benzoin, som har en anden sammensætning og oprindelse..
Artikelindeks
- 1 Struktur af benzoin
- 2 egenskaber
- 2.1 Navne
- 2.2 Molekylær formel
- 2.3 Molær masse
- 2.4 Fysisk beskrivelse
- 2.5 Smag
- 2.6 Kogepunkt
- 2.7 Smeltepunkt
- 2.8 Flammepunkt
- 2.9 Opløselighed i vand
- 2.10 Opløselighed i organiske opløsningsmidler
- 2,11 pH
- 2.12 Stabilitet
- 2.13 En anden eksperimentel egenskab
- 3 Syntese
- 4 anvendelser
- 4.1 Mellemmand
- 4.2 I mad
- 4.3 Human- og veterinærmedicin
- 4.4 Personlig pleje
- 4.5 Anvendelse af benzoin æterisk olie
- 5 Toksicitet
- 6 Referencer
Benzoins struktur
På billedet ovenfor blev benzoins molekylære struktur vist med en kugle- og stangmodel. Det kan ses, at den har to aromatiske ringe adskilt af to iltbærende carbonatomer; fra venstre mod højre, CHOH og CO. Bemærk også, at ringene har forskellige retninger i rummet..
Den hydrofobe del dominerer i sin struktur, mens oxygener bidrager let til dens dipolmoment; da begge aromatiske ringe tiltrækker elektrondensitet mod dem, spredes ladningen mere homogent.
Resultatet er, at benzoinmolekylet ikke er for polært; hvilket retfærdiggør, at det er dårligt opløseligt i vand.
Ved at fokusere på begge oxygenatomer vil det ses, at OH-gruppen kunne danne en intramolekylær hydrogenbinding med den tilstødende carbonylgruppe; det vil sige, at de ikke ville binde to benzoinmolekyler, men snarere en specifik rumlig konformation ville blive forstærket, hvilket forhindrede H (OH) C-CO-bindingen i at rotere for meget.
Selvom benzoin ikke betragtes som et højpolaritetsmolekyle, giver dets molekylære masse det tilstrækkelig samhørighedskraft til at definere en monoklinisk hvid krystal, der smelter omkring 138 ° C; afhængigt af urenhedsniveauet kan det være ved en lavere eller højere temperatur.
Ejendomme
Navne
Nogle af dens mange yderligere navne er:
- 2-hydroxy-1,2-diphenylethanon.
- benzoylphenylcarbanol.
- 2-hydroxy-2-phenylacetophenon.
- 2-hydroxy-1,2-diphenylethan-1-on.
Molekylær formel
C14H12ELLERto eller C6H5COCH (OH) C6H5.
Molar masse
212,248 g / mol.
Fysisk beskrivelse
Benzoin er et hvidt til off-white krystallinsk fast stof med en kamferlugt. Når de er brudt, er de friske overflader mælkehvide. Det kan også fremstå som et tørt pulver eller hvide eller gule krystaller.
Smag
Ikke beskrevet. Lidt skarpt.
Kogepunkt
344 ºC.
Smeltepunkt
137 ºC.
Antændelsespunkt
181 ºC.
Vandopløselighed
Næsten uopløselig.
Opløselighed i organiske opløsningsmidler
Opløselig i varm alkohol og kuldisulfid.
pH
I alkoholholdig opløsning er den sur, bestemmes af lakmuspapir.
Stabilitet
I stald. Det er en brændbar forbindelse og uforenelig med stærke oxidationsmidler.
En anden eksperimentel egenskab
Reducer Fehlings løsning.
Syntese
Det nederste billede viser kondensationsreaktionen af benzaldehyd for at give anledning til benzoin. Denne reaktion foretrækkes i nærværelse af kaliumcyanid i ethylalkoholopløsning..
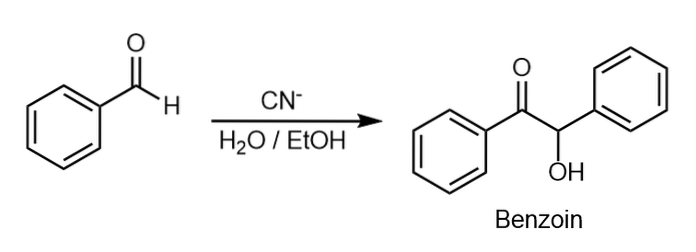
To benzaldehydmolekyler er kovalent bundet ved frigivelse af et vandmolekyle.
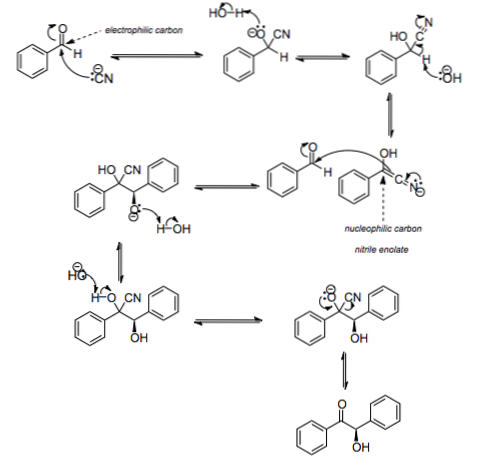
Hvordan sker dette? Gennem mekanismen illustreret ovenfor. CN anion- det fungerer som en nukleofil ved at angribe carbonet i carbonylgruppen i benzaldehyd. Ved at gøre dette og med deltagelse af vand bliver C = O C = N; men nu erstattes H med en OH, og benzaldehydet bliver nitrilenolat (anden række i billedet).
Den negative ladning af kvælstof delokaliseres mellem det og kulstof -C-CN; dette kulstof siges derefter at være nukleofilt (det ser ud til positive ladninger). Så meget, at det angriber carbonylgruppen i et andet benzaldehydmolekyle.
Igen griber et vandmolekyle ind for at producere en OH- og deprotonere en OH-gruppe; som senere danner en dobbeltbinding med kulstof for at give anledning til en C = O-gruppe, mens CN-gruppen migrerer som en cyanidanion. Således CN- katalyserer reaktionen uden at blive forbrugt.
Ansøgninger
Mellemmand
Benzoin er involveret i syntesen af organiske forbindelser gennem katalytisk polymerisation. Det er et mellemprodukt til syntese af α-benzoinoxim, et analytisk reagens for metaller. Det er et forstadium til benzyl, der fungerer som en fotoinitiator.
Syntesen af benzyl foregår ved organisk oxidation ved hjælp af kobber (III), salpetersyre eller ozon. Benzoin anvendes til fremstilling af farmaceutiske lægemidler såsom oxaprozin, ditazol og phenytoin.
I mad
Benzoin bruges som et smagsstof til fødevarer.
Human- og veterinærmedicin
Inden for veterinærmedicin bruges det som et antiseptisk middel til topisk anvendelse, der anvendes til behandling af sår i huden for at producere deres heling.
Det bruges også i medicin i formuleringer til fremstilling af inhalationsmidler til behandling af bronkitis og slimløsende til oral brug..
Personlig pleje
Benzoin anvendes til fremstilling af deodoranter.
Benzoin æterisk olie anvendelser
Denne essentielle olie er rapporteret at stimulere cirkulationen. En gavnlig virkning på nervesystemet er også rapporteret, manifesteret af lindring af angst og stress. Ligeledes er det blevet antydet, at det har en antiseptisk virkning på åbne sår..
Nogle forbindelser, der findes i benzoin-essentiel olie, såsom benzaldehyd, benzoesyre og benzylbenzoat, er bakteriedræbende og fungicide stoffer, der forhindrer sepsis..
Det er blevet antydet, at det har antiflatulent og carminativ virkning, en effekt, der tilskrives dets afslappende virkning på mavemusklerne. Ligeledes tilskrives det en vanddrivende virkning, der bidrager til eliminering af giftige stoffer til kroppen.
Denne essentielle olie bruges som et slimløsende middel, der lindrer luftvejsbelastning. Ligeledes er de blevet brugt til lindring af gigt gennem topisk anvendelse, der muliggør absorption af medicinske komponenter gennem huden..
Toksicitet
Benzoin ved kontakt forårsager rødme og irritation af hud og øjne. Ved indånding af det sammensatte støv opstår irritation af luftvejene, der manifesteres ved hoste. Imidlertid er det generelt ikke en meget giftig forbindelse..
Til tinktur af benzoin, et alkoholisk ekstrakt af træets harpiks Stirax benzoin, Et sæt giftige handlinger er blevet påpeget for ham. Måske fordi tinkturen er en blanding af forbindelser; herunder benzoesyre, benzaldehyd osv..
Kontakt med huden forårsager ikke signifikant irritation. Men kontakt med øjnene kan forårsage irritation, manifesteret af rødme, smerte, rive og sløret syn..
Indånding af dampe fra benzointinktur kan forårsage irritation af luftvejene, hoste, nysen, løbende næse, hæshed og ondt i halsen..
Endelig kan indtagelse af tinkturen forårsage gastrointestinal irritation, manifesteret af mavesmerter, kvalme, opkastning og diarré..
Referencer
- Wikipedia. (2019). Benzoin (organisk forbindelse). Gendannet fra: en.wikipedia.org
- National Center for Biotechnology Information. (2019). Benzoin. PubChem-database. CID = 8400. Gendannet fra: pubchem.ncbi.nlm.nih.gov
- Donald L. Robertson. (2012). Flertrinssyntese-koenzymkatalyseret syntese af benzoin og derivater. Gendannet fra: home.miracosta.edu
- Tim Soderberg. (2014, 29. august). Vitamin B1. Kemi LibreTexts. Gendannet fra: chem.libretexts.org
- Haisa, S. Kashino og M. Morimoto. (1980). Benzoins struktur. Acta Cryst. B36, 2832-2834. doi.org/10.1107/S0567740880010217
- Meenakshi Nagdeve. (21. maj 2019). 11 vidunderlige fordele ved benzoin æterisk olie. Organiske fakta. Gendannet fra: organicfacts.net
- Bre. (2019). Benzoin æterisk olie elsket af antikke royalty. Gendannet fra: monq.com



Endnu ingen kommentarer