
Phosphodiester binder, hvordan det dannes, funktion og eksempler
Det phosphodiesterbindinger er de kovalente bindinger, der forekommer mellem to af oxygenatomerne i en phosphatgruppe og hydroxylgrupperne i to andre forskellige molekyler. I denne type binding fungerer fosfatgruppen som en stabil bindings "bro" mellem de to molekyler gennem deres iltatomer..
Den grundlæggende rolle af phosphodiesterbindinger i naturen er dannelsen af nukleinsyrekæder, både DNA og RNA. Sammen med pentosesukkerne (deoxyribose eller ribose, alt efter omstændighederne), er phosphatgrupperne en del af den bærende struktur af disse vigtige biomolekyler..
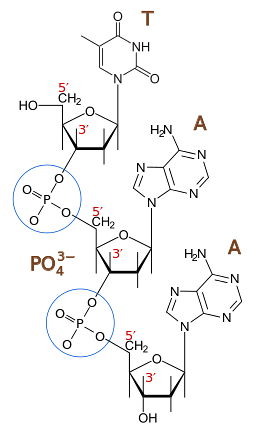
Nukleotidkæderne af DNA eller RNA kan ligesom proteiner antage forskellige tredimensionelle konformationer, der er stabiliseret af ikke-kovalente bindinger, såsom hydrogenbindinger mellem komplementære baser..
Den primære struktur er imidlertid givet af den lineære sekvens af nukleotider, der er kovalent bundet via phosphodiesterbindinger..
Artikelindeks
- 1 Hvordan dannes en phosphodiesterbinding?
- 1.1 Enzymer involveret
- 2 Funktion og eksempler
- 3 Referencer
Hvordan dannes en fosfodiesterbinding?
Ligesom peptidbindinger i proteiner og glykosidbindinger mellem monosaccharider, skyldes phosphodiesterbindinger dehydreringsreaktioner, hvor et vandmolekyle går tabt. Her er det generelle skema for en af disse dehydratiseringsreaktioner:
H-X1-OH + H-Xto-OH → H-X1-xto-OH + HtoELLER
Phosphationer svarer til den fuldstændigt deprotonerede konjugatbase af phosphorsyre og kaldes uorganiske phosphater, forkortet Pi. Når to phosphatgrupper er bundet sammen, dannes der en vandfri phosphatbinding, og der opnås et molekyle kendt som uorganisk pyrophosphat eller PPi..
Når en phosphation er bundet til et carbonatom i et organisk molekyle, kaldes den kemiske binding en phosphatester, og den resulterende art er et organisk monophosphat. Hvis det organiske molekyle binder til mere end en fosfatgruppe, dannes organiske diphosphater eller triphosphater.
Når et enkelt uorganisk phosphatmolekyle er bundet til to organiske grupper, anvendes en phosphodiester- eller "phosphatdiester" -binding. Det er vigtigt ikke at forveksle phosphodiesterbindingerne med de højenergiske phosphoanhydrobindinger mellem fosfatgrupperne af molekyler som f.eks. ATP..
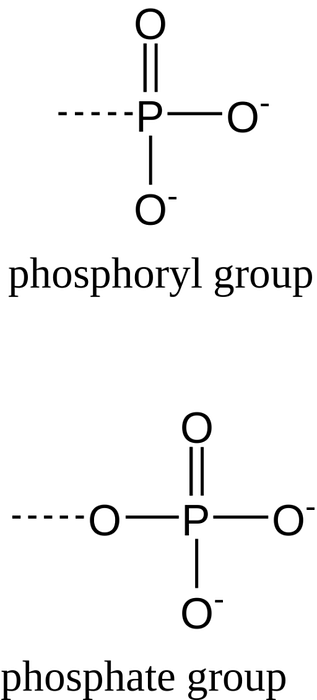
Phosphodiesterbindinger mellem tilstødende nukleotider består af to phosphoesterbindinger, der forekommer mellem hydroxylen ved 5'-positionen af et nukleotid og hydroxylen ved 3'-positionen af det næste nukleotid i en DNA- eller RNA-streng.
Afhængig af miljøforholdene kan disse bindinger hydrolyseres både enzymatisk og ikke-enzymatisk..
Involverede enzymer
Dannelse og nedbrydning af kemiske bindinger er afgørende for alle vitale processer, som vi kender dem, og tilfældet med phosphodiesterbindinger er ingen undtagelse..
Blandt de vigtigste enzymer, der kan danne disse bindinger, er DNA- eller RNA-polymeraser og ribozymer. Phosphodiesterase-enzymer er i stand til enzymatisk at hydrolysere dem.
Under replikation er en vigtig proces til celleproliferation i hver reaktionscyklus et dNTP (deoxynukleotidtriphosphat) komplementært til skabelonbasen inkorporeret i DNA'et gennem en nukleotidoverførselsreaktion..
Polymerasen er ansvarlig for at danne en ny binding mellem 3'-OH af skabelonstrengen og α-phosphatet af dNTP takket være den energi, der frigøres fra brydningen af bindingerne mellem α og β-phosphaterne i dNTP, som er bundet af phosphoanhydrobindinger.
Resultatet er forlængelsen af kæden med et nukleotid og frigivelsen af et molekyle af pyrophosphat (PPi). Disse reaktioner er blevet bestemt til at fortjene to divalente magnesiumioner (Mgto+), hvis tilstedeværelse tillader den elektrostatiske stabilisering af nukleofil OH- for at få tilnærmelsen til enzymets aktive sted.
Det pKtil af en phosphodiesterbinding er tæt på 0, så i en vandig opløsning er disse bindinger fuldstændigt ioniserede, negativt ladede.
Dette giver nukleinsyremolekyler en negativ ladning, som neutraliseres takket være ioniske interaktioner med de positive ladninger af proteinaminosyrerester, elektrostatisk binding med metalioner eller tilknytning til polyaminer..
I en vandig opløsning er phosphodiesterbindingerne i DNA-molekyler meget mere stabile end i RNA-molekyler. I alkalisk opløsning spaltes disse bindinger i RNA-molekyler ved intramolekylær forskydning af nukleosidet i 5'-enden med en 2'-oxyanion.
Funktion og eksempler
Som nævnt er den mest relevante rolle for disse bindinger deres deltagelse i dannelsen af rygraden i nukleinsyremolekyler, som er en af de vigtigste molekyler i den cellulære verden..
Aktiviteten af topoisomeraseenzymer, som aktivt deltager i DNA-replikation og proteinsyntese, afhænger af interaktionen mellem phosphodiesterbindingerne i 5'-enden af DNA og sidekæden af tyrosinrester i det aktive sted af disse enzymer.
Molekyler, der deltager som anden budbringere, såsom cyklisk adenosinmonophosphat (cAMP) eller cyklisk guanosintriphosphat (cGTP), har phosphodiesterbindinger, der hydrolyseres af specifikke enzymer kendt som phosphodiesteraser, hvis deltagelse er af største betydning for mange signalprocesser mobile.
Glycerophospholipider, grundlæggende komponenter i biologiske membraner, består af et glycerolmolekyle, der binder gennem phosphodiesterbindinger til de polære "hoved" -grupper, der udgør den hydrofile region af molekylet..
Referencer
- Fothergill, M., Goodman, M. F., Petruska, J., & Warshel, A. (1995). Struktur-energi-analyse af rollen af metalioner i phosphodiester-bindingshydrolyse ved hjælp af DNA-polymerase I. Journal of the American Chemical Society, 117(47), 11619-11627.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Bretscher, A., Ploegh, H., Martin, K. (2003). Molekylær cellebiologi (5. udgave). Freeman, W. H. & Company.
- Nakamura, T., Zhao, Y., Yamagata, Y., Hua, Y. J., & Yang, W. (2012). Ser DNA-polymerase η skabe en phosphodiesterbinding. Natur, 487(7406), 196-201.
- Nelson, D. L. og Cox, M. M. (2009). Lehninger Principper for biokemi. Omega-udgaver (5. udgave)
- Oivanen, M., Kuusela, S., & Lönnberg, H. (1998). Kinetik og mekanismer til spaltning og isomerisering af phosphodiesterbindingerne af RNA med bronstesyrer og baser. Kemiske anmeldelser, 98(3), 961-990.
- Pradeepkumar, P. I., Höbartner, C., Baum, D., og Silverman, S. (2008). DNA-katalyseret dannelse af nukleopeptidbindinger. Angewandte Chemie International Edition, 47(9), 1753-1757.
- Soderberg, T. (2010). Organisk kemi med en biologisk vægt bind II (Bind II). Minnesota: University of Minnesota Morris Digital Well. Hentet fra www.digitalcommons.morris.umn.edu


Endnu ingen kommentarer