
Interatomiske links egenskaber og typer

Det link interatomær Det er den kemiske binding, der dannes mellem atomer for at producere molekyler. Selvom forskere i dag generelt er enige om, at elektroner ikke drejer sig om kernen, troede man gennem historien, at hver elektron kredsede omkring atomets kerne i en separat skal..
I dag har forskere konkluderet, at elektroner svæver over bestemte områder af atomet og ikke danner baner, men valensskallen bruges stadig til at beskrive tilgængeligheden af elektroner..
Linus Pauling bidrog til den moderne forståelse af kemisk binding ved at skrive bogen "The Nature of Chemical Bonding", hvor han samlede ideer fra Sir Isaac Newton, Étienne François Geoffroy, Edward Frankland og især Gilbert N. Lewis..
I det forbandt han kvantemekanikens fysik med den kemiske natur af de elektroniske interaktioner, der opstår, når der dannes kemiske bindinger..
Paulings arbejde fokuserede på at fastslå, at ægte ioniske bindinger og kovalente bindinger ligger i enderne af et bindingsspektrum, og at de fleste kemiske bindinger klassificeres mellem disse ekstremer..
Pauling udviklede yderligere en glideskala af bindingstype styret af elektronegativiteten af de atomer, der er involveret i båndet..
Paulings enorme bidrag til vores moderne forståelse af kemisk binding førte til, at han blev tildelt Nobelprisen i 1954 for "undersøgelse af arten af kemisk binding og dens anvendelse til at belyse strukturen af komplekse stoffer."
Levende ting består af atomer, men i de fleste tilfælde flyder disse atomer ikke bare individuelt. I stedet interagerer de normalt med andre atomer (eller grupper af atomer).
For eksempel kan atomer forbindes med stærke bindinger og organiseres i molekyler eller krystaller. Eller de kan danne midlertidige, svage bindinger med andre atomer, der kolliderer med dem..
Både de stærke bindinger, der binder molekyler, og de svage bindinger, der skaber midlertidige forbindelser, er vigtige for vores krops kemi og for selve livets eksistens..
Atomer har en tendens til at arrangere sig i de mest stabile mønstre, hvilket betyder, at de har en tendens til at fuldføre eller udfylde deres yderste elektronbaner..
De binder sig til andre atomer for at gøre netop det. Kraften, der holder atomer sammen i samlinger kendt som molekyler, er kendt som en kemisk binding..
Typer af interatomiske kemiske bindinger
Metallisk binding
Den metalliske binding er den kraft, der holder atomerne sammen i et rent metallisk stof. Et sådant fast stof består af tæt pakkede atomer.
I de fleste tilfælde overlapper den yderste elektronskal af hvert af metalatomer med et stort antal nabostater. Som en konsekvens bevæger valenselektroner konstant sig fra atom til atom og er ikke forbundet med noget specifikt atomerpar..
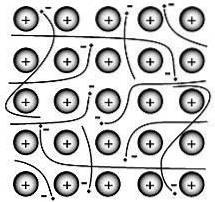
Metaller har flere unikke kvaliteter, såsom evnen til at lede elektricitet, lav ioniseringsenergi og lav elektronegativitet (så de giver let op elektroner, det vil sige de er kationer)..
Deres fysiske egenskaber inkluderer et skinnende (skinnende) udseende, og de er formbare og duktile. Metaller har en krystallinsk struktur. Imidlertid er metaller også formbare og duktile.
I 1900'erne kom Paul Drüde op med elektronhavsteorien ved at modellere metaller som en blanding af atomkerner (atomkerner = positive kerner + indre elektronskal) og valenselektroner..
I denne model er valenselektronerne frie, delokaliserede, mobile og ikke forbundet med et bestemt atom..
Ionisk binding
Ioniske bindinger er elektrostatiske. De opstår, når et element med en positiv ladning forbinder et med en negativ ladning ved coulombiske interaktioner.
Elementer med lav ioniseringsenergi har tendens til let at miste elektroner, mens elementer med høj elektronaffinitet har tendens til at få dem til at producere henholdsvis kationer og anioner, hvilket er hvad der danner ionbindinger..
Forbindelser, der viser ionbindinger, danner ioniske krystaller, hvor positive og negativt ladede ioner svinger tæt på hinanden, men der er ikke altid en direkte 1-1 korrelation mellem positive og negative ioner..
Ioniske bindinger kan typisk brydes gennem hydrogenering eller tilsætning af vand til en forbindelse.
Stoffer, der holdes sammen af ionbindinger (såsom natriumchlorid) kan ofte adskilles i ægte ladede ioner, når de påvirkes af en ekstern kraft, såsom når de opløses i vand..
Desuden tiltrækkes individuelle atomer i fast form ikke af en individuel nabo, men danner i stedet gigantiske netværk, der tiltrækkes af hinanden ved elektrostatiske interaktioner mellem kernen i hvert atom og nærliggende valenselektroner..
Tiltrækningskraften mellem nærliggende atomer giver ioniske faste stoffer en ekstremt ordnet struktur kendt som et ionisk gitter, hvor modsat ladede partikler flugter med hinanden for at skabe en tæt bundet stiv struktur..

Kovalent binding
Kovalent binding opstår, når par af elektroner deles af atomer. Atomer vil forbinde kovalent med andre atomer for at opnå mere stabilitet, hvilket opnås ved at danne en komplet elektronskal.
Ved at dele deres yderste (valens) elektroner kan atomer fylde deres ydre skal med elektroner og få stabilitet..
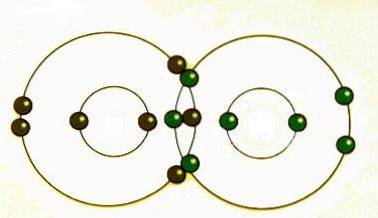
Selvom atomer siges at dele elektroner, når de danner kovalente bindinger, deler de ofte ikke elektroner ens. Først når to atomer af det samme element danner en kovalent binding, deles de delte elektroner faktisk ligeligt mellem atomerne..
Når atomer med forskellige elementer deler elektroner gennem kovalent binding, trækkes elektronen yderligere mod atomet med den højeste elektronegativitet, hvilket resulterer i en polær kovalent binding..
Sammenlignet med ioniske forbindelser har kovalente forbindelser normalt et lavere smelte- og kogepunkt og er mindre tilbøjelige til at opløses i vand..
Kovalente forbindelser kan være i gas, flydende eller fast tilstand og leder ikke elektricitet eller varme godt op..
Brintbindinger
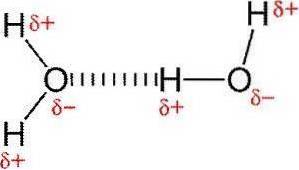
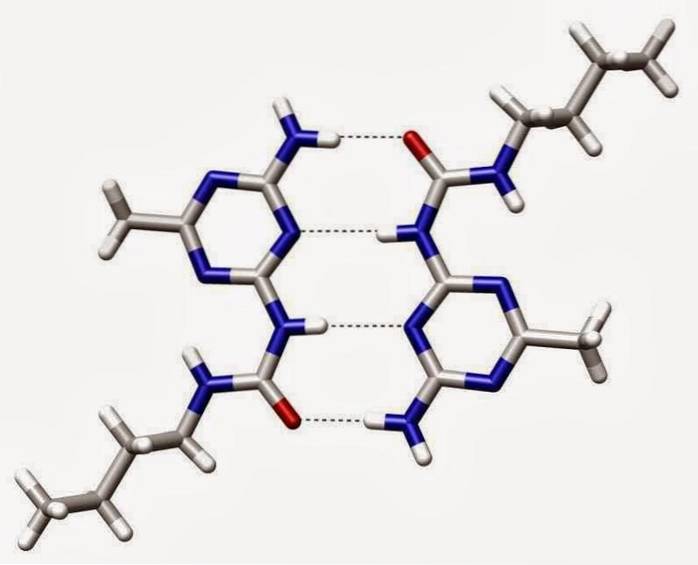
Hydrogenbindinger eller hydrogenbindinger er svage interaktioner mellem et hydrogenatom, der er knyttet til et elektronegativt element med et andet elektronegativt element.
I en polær kovalent binding, der indeholder hydrogen (for eksempel en O-H-binding i et vandmolekyle), vil hydrogenet have en let positiv ladning, fordi bindingselektronerne trækkes stærkere mod det andet element..
På grund af denne lille positive ladning vil brint blive tiltrukket af eventuelle negative ladninger..
Links til Van der Waals
De er relativt svage elektriske kræfter, der tiltrækker neutrale molekyler til hinanden i gasser, i flydende og størknede gasser og i næsten alle organiske og faste væsker..
Styrkerne er opkaldt efter den hollandske fysiker Johannes Diderik van der Waals, som i 1873 først postulerede disse intermolekylære kræfter i at udvikle en teori til at forklare egenskaberne af ægte gasser..
Van der Waals-kræfter er et generelt udtryk, der bruges til at definere tiltrækningen af intermolekylære kræfter mellem molekyler..
Der er to klasser af Van der Waals-kræfter: Londons spredningskræfter, der er svage og stærkere dipol-dipolkræfter..
Referencer
- Anthony Capri, A. D. (2003). Kemisk binding: Arten af den kemiske binding. Hentet fra visionlearning visionlearning.com
- Camy Fung, N. M. (2015, 11. august). Kovalente obligationer. Hentet fra chem.libretexts chem.libretexts.org
- Clark, J. (2017, 25. februar). Metallisk limning. Hentet fra chem.libretexts chem.libretexts.org
- Encyclopædia Britannica. (2016, 4. april). Metallisk binding. Hentet fra britannica britannica.com.
- Encyclopædia Britannica. (2016, 16. marts). Van der Waals styrker. Hentet fra britannica britannica.com
- Kathryn Rashe, L. P. (2017, 11. marts). Van der waals styrker. Hentet fra chem.libretexts chem.libretexts.org.
- Khan, S. (S.F.). Kemiske bindinger. Hentet fra khanacademy khanacademy.org.
- Martinez, E. (2017, 24. april). Hvad er Atomic Bonding? Hentet fra sciencing sciencing.com.
- Wyzant, Inc. (S.F.). Obligationer. Hentet fra wyzant wyzant.com.


Endnu ingen kommentarer