
Fucosa karakteristika, struktur, funktioner
Det fucose (forkortet Fuc), eller 6-L-deoxy-galactose, er en delvist deoxygeneret (deoxysukker) seks-carbon monosaccharid, hvis empiriske formel er C6H12ELLER5. Som andre monosaccharider er det et polyvalent sukker.
Når en hydroxylgruppe erstattes af et hydrogenatom, afledes en deoxysukker. Selvom denne udskiftning teoretisk kan påvirke enhver hydroxylgruppe af ethvert monosaccharid, er der i naturen kun et lille udvalg af deoxysukker.
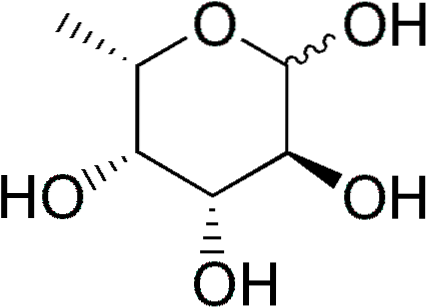
Nogle deoxysukker er: 1) deoxyribose (2-deoxy-D-ribose), afledt af D-ribose, som er en del af DNA; 2) rhamnose (6-D-deoxymannose), afledt af D-mannose; 3) fucose, afledt af L-galactose. Sidstnævnte er mere almindelig end D-fucose, afledt af D-galactose.
Artikelindeks
- 1 Egenskaber og struktur
- 2 Udbredelse i naturen
- 3 Fucosemetabolisme
- 4 funktioner
- 4.1 Kræftens rolle
- 4.2 Roll i andre sygdomme
- 4.3 Biomedicinsk potentiale
- 5 Referencer
Karakteristika og struktur
Fucose er også kendt under navnene 6-deoxy-galacto-hexose, fucopyranose, galactomethylose og rodeose..
Selvom det normalt findes ved dannelse af polysaccharider og glycoproteiner, er det isoleret som et monosaccharid sødere end galactose. Dette skyldes det faktum, at udskiftningen af en hydroxylgruppe med et hydrogenatom øger den hydrofobe karakter og derfor sødheden af molekylet..
Hydroxylgrupperne af fucose kan gennemgå de samme reaktioner som andre sukkerarter og producere en lang række acetaler, glycosider, ethere og estere..
Et fucosyleret biomolekyle er et, hvortil fucosemolekyler ved hjælp af en fucosyltransferase er bundet gennem glykosidiske bindinger. Når hydrolysen af glykosidbindinger sker ved virkningen af en fucosidase og således adskiller fucosen, siges det, at biomolekylet er defucosyleret.
Når glucaner fucosyleres, genereres mere komplekse glucaner kaldet fucans, som måske eller ikke er en del af glycoproteiner. Sulfaterede fucaner defineres som de polysaccharider, der indeholder sulfaterede L-fucoserester. De er typiske for brune alger. Eksempler inkluderer ascophylan, sargasan og pelvetan..
En af de bedst studerede fucaner er fucoidan, opnået fra brune alger Fucus vesiculosus, som er blevet markedsført (Sigma-Aldrich Chemical Company) i årtier.
Distribution i naturen
D-fucose er til stede i antibiotiske stoffer produceret af mikrober og i planteglykosider, såsom convolvulin, chartreusin, ledienosid og keirotoksin.
L-fucose er en bestanddel af polysaccharider fra alger, blommer, hør, soja- og rapsfrø, tragantgummi, kartoffelcellevægge, kassava-knolde, kiwifrugter, barken af ceiba og mucigel af majscaliptra samt andre planter.
L-fucose er også til stede i søpindsvinæg og i gelatinen, der beskytter frøæg.
Hos pattedyr danner fucaner med L-fucose ligander, der virker på selectin-medieret leukocyt-endotel adhæsion, og deltager i adskillige ontogenetiske hændelser.
L-fucose er rigelig i fucosphingolipiderne i mave-tarmepitel og knoglemarv og forekommer i små proportioner i brusk og keratinstrukturer.
Hos mennesker er L-fucosefucaner en del af glykoproteiner i spyt og mavesaft. De er også en del af antigenerne, der definerer ABO-blodgrupper. De er til stede i forskellige oligosaccharider i modermælk.
Fukosemetabolisme
Fucosyltransferaser bruger BNP-fucose, en nukleotidaktiveret form af fucose, som en fucosedonor i konstruktionen af fucosylerede oligosaccharider.
BNP-fucose er afledt af BNP-mannose ved den successive virkning af to enzymer: BNP-mannose 4,6-dehydratase og BNP-4-keto-6-deoximanose 3,5-epimerase-4-reduktase.
Ved hjælp af en NADP + cofaktor katalyserer det første enzym dehydrering af BNP-mannose. Reduktion af position 6 og oxidation af position 4 producerer BNP-6-deoxy-4-keto-mannose (under reaktionen overføres hybrid fra position 4 til 6 i sukkeret).
Det andet enzym, som er NADPH-afhængigt, katalyserer epimeriseringen af position 3 og 5 og reduktionen af 4-ketogruppen af BNP-6-deoxy-4-keto-mannose..
Bakterier kan vokse ved hjælp af fucose som den eneste kilde til kulstof og energi ved hjælp af et fucose-inducerbart operon, der koder for kataboliske enzymer til dette sukker..
Ovenstående fremgangsmåde involverer: 1) indgang af fri fucose gennem cellevæggen medieret af en permease; 2) isomerisering af fucose (en aldose) til dannelse af fuculose (en ketose); 3) phosphorylering af fuculose til dannelse af fuculose-1-phosphat; 4) en aldolasereaktion til dannelse af lactaldehyd og dihydroxyacetonphosphat ud fra fuculose-1-phosphat.
Funktioner
Roll i kræft
Symptomer på mange typer kræfttumorer inkluderer tilstedeværelsen af glucanbundne proteiner, der skelnes ved at have en ændret oligosaccharidsammensætning. Tilstedeværelsen af disse unormale glucaner, blandt hvilke fucaner skiller sig ud, er knyttet til disse tumors malignitet og metastatiske potentiale..
I brystkræft inkorporerer tumorceller fucose i glycoproteiner og glycolipider. Fucose bidrager til progressionen af denne kræft og favoriserer aktivering af kræftstamceller, hæmatogen metastase og invasionen af tumorer gennem ekstracellulære matricer.
I lungecarcinom og hepatocarcinogenese er øget fucoseekspression forbundet med et højt metastatisk potentiale og en lav sandsynlighed for overlevelse.
I modsætning hertil er nogle sulfaterede fucaner lovende stoffer til behandling af kræft, som det er blevet bestemt ved talrige in vitro-undersøgelser med kræftcellelinjer, herunder dem, der forårsager bryst-, lunge-, prostata-, gastrisk, tyktarms- og endetarmscancer..
Roll i andre sygdomme
Øget ekspression af fucaner i serumimmunglobuliner har været forbundet med juvenil og voksen reumatoid arthritis.
Leukocytadhæsionsmangel II er en sjælden medfødt sygdom på grund af mutationer, der ændrer aktiviteten af en FDP-fucose-transportør placeret i Golgi-apparatet.
Patienter lider af mental og psykomotorisk retardation og lider af tilbagevendende bakterieinfektioner. Denne sygdom reagerer gunstigt på orale doser af fucose.
Biomedicinsk potentiale
Sulfaterede fucaner opnået fra brune alger er vigtige reservoirer af forbindelser med terapeutisk potentiale.
De har antiinflammatoriske og antioxidantegenskaber, der hæmmer migrering af lymfocytter på infektionssteder og favoriserer frigivelse af cytokiner. Forøg immunresponset ved at aktivere lymfocytter og makrofager.
De har antikoagulerende egenskaber. Oralt vist sig at hæmme blodpladeaggregering hos humane patienter.
De har antibiotisk og antiparasitisk potentiale og hæmmer væksten af mavepatogene bakterier Helicobacter pylori. Dræb parasitter Plasmodium spp. (forårsagende middel til malaria) og Leishmania donovani (forårsagende middel til amerikansk viscerotrop leishmaniasis).
Endelig har de kraftige antivirale egenskaber, der hæmmer indtrængen i cellen af flere vira af stor betydning for menneskers sundhed, herunder Arenavirus, Cytomegalovirus, Hantavirus, Hepadnavirus, HIV, herpes simplex-virus og influenzavirus.
Referencer
- Becker, D. J., Lowe, J. B. 2003. Fucose: biosyntese og biologisk funktion hos pattedyr. Glykobiologi, 13, 41R-53R.
- Deniaud-Bouët, E., Hardouin, K., Potin, P., Kloareg, B., Hervé, C. 2017. En gennemgang af brune alge cellevægge og fucoseholdige sulfaterede polysaccharider: cellevæggekontekst, biomedicinske egenskaber og nøgle forskning udfordrer kulhydratpolymerer, http://dx.doi.org/10.1016/j.carbpol.2017.07.082.
- Blomster H. M. 1981. Kemi og biokemi af D- og L-fucose. Fremskridt inden for kulhydratkemi og biokemi, 39, 279-345.
- Listinsky, J. J., Siegal, G. P., Listinsky, C. M. 2011. Den nye betydning af a-L-fucose i human brystkræft: en gennemgang. Am. J. Transl. Res., 3, 292-322.
- Murray, R. K., et al. 2003. Harpers illustrerede biokemi. McGraw-Hill, New York.
- Pereira, L. 2018. Terapeutiske og ernæringsmæssige anvendelser af alger. CRC Press, Boca Raton.
- Staudacher, E., Altmann, F., Wilson, I. B. H., März, L. 1999. Fucose i N-glycaner: fra plante til menneske. Biochimica et Biophysica Acta, 1473, 216-236.
- Tanner, W., Loewus, F. A. 1981. Plantekulhydrater II. Ekstracellulære kulhydrater. Springer, New York.
- Vanhooren, P. T., Vandamme, E. J. 1999. L-fucose: forekomst, fysiologisk rolle, kemisk, enzymatisk og mikrobiel syntese. Journal of Chemical Technology and Biotechnology, 74, 479-497.



Endnu ingen kommentarer