
Helicobacter pylori karakteristika, morfologi, habitat
Helicobacter pylori det er en gramnegativ spiralformet bakterie, der er involveret i udviklingen af gastritis, mavesår og forbundet med gastrisk kræft. Det blev opdaget i 1983 af australske patologer Robin Warren og Barry Marshall, da de undersøgte gastrisk slimhinde fra menneskelige maver..
Marshall eksperimenterede endda med sig selv og indtog materiale, der var forurenet med bakterierne, hvor han fandt ud af, at det forårsagede gastritis og var i stand til at verificere tilstedeværelsen af bakterierne i hans egen mavebiopsi. Det bekræftede også, at det reagerede på antibiotikabehandling.
Med dette demonterede de gamle teorier, der hævdede, at gastritis var forårsaget af indtagelse af krydret mad eller af stress. Af denne grund blev Warren og Marshal i 2005 tildelt Nobelprisen i medicin..
Artikelindeks
- 1 Generelle egenskaber
- 2 Habitat
- 3 Virulensfaktorer
- 3.1 Flagella
- 3.2 Klæbestoffer
- 3.3 Lipopolysaccharider (LPS)
- 3.4 Ureas
- 3.5 Vakuoliserende cytotoksin (VacA)
- 3.6 Cytotoksin (CagA)
- 3.7 Superoxiddismutase og katalase
- 3.8 Inducerbar nitrogenoxidsyntase (iNOS):
- 3.9 Fosfolipaser, lipaser og mukinaser
- 4 Taxonomi
- 5 Morfologi
- 6 Diagnose
- 6.1 -Invasive metoder
- 6.2 -Ikke-invasive metoder
- 7 Livscyklus
- 8 Patogenese
- 8.1 Inflammatorisk infiltration
- 9 Patologi
- 10 Kliniske manifestationer
- 11 Smitte
- 12 Behandling
- 13 Referencer
Generelle egenskaber
På grund af dets store lighed med slægten Campylobacter blev den oprindeligt kaldt Campylobacter pyloridis og efterfølgende Campylobacter pylori, men så blev den omklassificeret til en ny genre.
Infektion af Helicobacter pylori det har en bred fordeling i mange hovedsageligt underudviklede lande og er en af de hyppigste infektioner hos mennesker, som normalt forekommer fra barndommen.
Det antages, at når mikroorganismen er erhvervet for første gang, kan den forblive i årevis eller i en levetid, i nogle tilfælde asymptomatisk.
På den anden side ser maven ikke ud til at være det eneste sted, hvor mikroorganismen kan opbevares, menes det at H. pylori kan konsolideres i munden inden kolonisering af maven.
Ligeledes er det muligt, at H. pylori til stede i mundhulen kan inficere maven igen efter behandling. Dette forstærkes ved at konstatere, at nogle asymptomatiske børn har isoleret mikroorganismen fra tandplaque..
Men selvom infektion med Helicobacter pylori er asymptomatisk hos nogle mennesker, det er ikke harmløst, da det har været forbundet med 95% af duodenalsår, 70% af peptiske mavesår og 100% af kronisk gastritis i antral placering.
Hvad mere er, Helicobacter pylori er blevet klassificeret som kræftfremkaldende klasse I af Det Internationale Agentur for Kræftforskning på grund af dets sammenhæng mellem infektion og gastrisk kræft.
Habitat
Helicobacter pylori fundet i følgende værter: mand, abe og katte.
Denne bakterie kræver en mikroaerofil atmosfære (10% COto, 5% Oto og 85% af Nto) der skal dyrkes, hvor jern er et væsentligt element for dets vækst og stofskifte.
Den optimale væksttemperatur er 35 til 37 ºC, selvom nogle stammer er i stand til at udvikle sig ved 42 ºC. Ligeledes favoriserer en vis fugtighedsgrad dens vækst..
Helicobacter pylori vokser langsomt i laboratoriet og kan kræve fra 3 til 5 dage og endda op til 7 dage for kolonien at blive tydelig i mediet.
Ikke-selektive medier suppleret med blod kan bruges til dets kultur..
På den anden side, Helicobacter pylori det er kendetegnet ved at være mobilt og på grund af sin spiralform giver det det mulighed for at have helixbevægelser som om det var skruet. Dette hjælper det med at bevæge sig gennem gastrisk slim..
Det er også katalase- og oxidase-positivt og en stor producent af urease, hvor sidstnævnte opfylder en vital funktion for mikroorganismen. Uris gør det muligt at overleve i sure pH-miljøer ved at generere ammoniak, som hjælper med at alkalisere pH.
Mikroorganismen har brug for en pH-værdi på 6 til 7 for at vokse. For at gøre dette, ud over at bruge urease, er det installeret til at leve under gastrisk slimhinde, hvor gastrisk slim beskytter det mod den ekstreme surhed i mavelumen (pH 1,0 - 2,0).
På den anden side ændrer proteaserne, der udskilles af bakterierne, gastrisk slim, hvilket reducerer muligheden for, at syren diffunderer gennem slimet..
Virulensfaktorer
Flagella
Bevægelsen af bakterierne repræsenterer en virulensfaktor, fordi den hjælper den med at kolonisere maveslimhinden.
Klæbestoffer
Bakterierne præsenterer pilis og fimbriumhæmagglutinin, som virker på mikroorganismens vedhæftning til gastriske og duodenale celler.
Overholdelse er en strategi for bakterierne til at modstå peristaltik i slimhinden, hvor de opholder sig, for senere at migrere til epitelcellerne.
På den anden side forsinker specifikke sialinsyrehæmagglutininer på slimhindeoverfladen vedhæftning og indtagelse af H. pylori.
Lipopolysaccharider (LPS)
Det er endotoksisk som LPS for andre gramnegative bakterier. Oprenset antigen kan inducere apoptose.
Urease
Bakterierne bruger produktionen af urease til at nedbryde urinstof til ammoniak og kuldioxid..
Denne handling gør det muligt at opretholde en alkalisk pH omkring den og dermed undgå at blive ødelagt af saltsyre i maven, hvilket garanterer dens overlevelse..
Denne egenskab er kodet af Ura A-genet.
Vakuoliserende cytotoksin (VacA)
Det er et protein, der skaber vakuoler i maveens epitelceller, hvorfor vævet mavesår. Det er kodet af VacA-genet.
Cytotoksin (CagA)
Stammer med CagA-genet er mere virulente. Disse er forbundet med svær gastritis, atrofisk gastritis, duodenitis og / eller gastrisk kræft.
Dette CagA-cytotoksin øger proliferationen af gastriske celler uden apoptose, hvilket fører til en ændring i det normale fornyelsesmønster i maveepitel..
Superoxiddismutase og katalase
Det er vigtigt for beskyttelse mod neutrofile O2-afhængige dødsfald.
Det virker ved at nedbryde hydrogenperoxid, en metabolit, der er giftig for bakterier.
Inducerbar nitrogenoxidsyntase (iNOS):
Bakterier inducerer iNOS og makrofager in vitro.
Dette fund antyder, at den høje produktion af nitrogenoxid på grund af induktion af denne synthase, i forbindelse med immunaktivering, deltager i vævsskader..
Fosfolipaser, lipaser og mucinaser
De tillader invasion af mikroorganismen under maveslimhinden og modificerer derefter slimet, så det fungerer som et vandtæt lag, der beskytter det mod syren i maven..
Desuden er immunresponsen på dette sted fuldstændig ineffektiv..
Taxonomi
Domæne: Bakterie
Phylum: Proteobakterier
Klasse: Epsilonproteobakterier
Bestille: Campylobacterales
Familie: Helicobacteraceae
Køn: Helicobacter
Arter: pylori
Morfologi
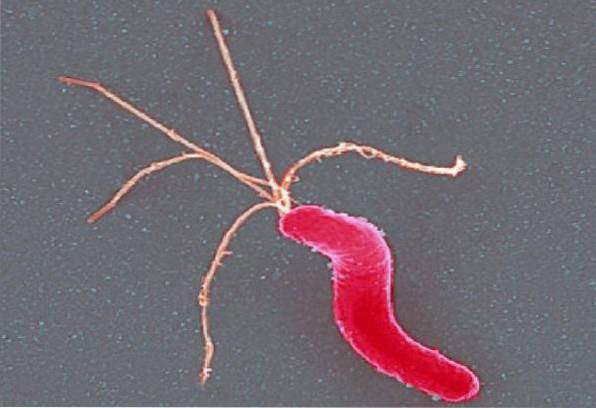
Helicobacter pylori Det er en lille, buet, let stump, Gram-negativ tynd spiralformet stang. Den måler cirka 3 µm lang og 0,5 µm bred. Pletter godt med Hematoxylin-Eosin, modificeret Giensa-plet eller Warthin-Starry-teknik.
Det er mobilt takket være tilstedeværelsen af flere polære flageller (tuftet), mellem 4 og 6 i alt, der er karakteristisk beklædt.
Skeden, der dækker flagellen, indeholder proteiner og lipopolysaccharid svarende til komponenterne i den ydre membran. Imidlertid er dens funktion ukendt..
Det danner ikke sporer og er ikke kapslet. Cellevæggen svarer til den for andre gramnegative bakterier.
Kolonierne i Helicobacter pylori de er normalt små grå og gennemsigtige. Efterhånden som kolonierne bliver ældre (langvarige kulturer), bliver bacillære former coccoid.
Diagnose
Til diagnose af Helicobacter pylori der er mange metoder, og de er klassificeret som invasive og ikke-invasive.
-Invasive metoder
Gastrisk slimhindebiopsi
Det tages gennem endoskopi, den mest følsomme metode til diagnose af Helicobacter pylori.
Mikroorganismerne kan observeres i vævsafsnittene, derudover at slimhinden vil have patognomiske egenskaber ved deres tilstedeværelse.
Ulempen er, at fordelingen af H. pylori i maven er ikke ensartet.
Hurtig ureasetest
Det er en metode til indirekte påvisning af bakterierne.
Dele af prøverne kan nedsænkes i urinstof med en pH-indikator (Phenol Red) og på mindre end en time kan resultaterne observeres.
Urinstof bouillon medium bliver fra gul til fuchsia på grund af ændringen i pH forårsaget af produktionen af ammoniak fra urinstof ved ureas virkning..
Følsomheden af denne test afhænger af bakteriel belastning i maven..
Dyrkning af gastrisk slimhindeprøver
En del af prøven taget ved endoskopi kan være bestemt til at blive dyrket. En negativ kultur er den mest følsomme indikator for en kur efter behandling.
Den gastriske eller duodenale biopsiprøve skal være nyere, og transporten må ikke tage mere end 3 timer. De kan opbevares i op til 5 timer ved 4 ° C, og vævet skal holdes fugtigt (beholder med 2 ml steril fysiologisk saltopløsning).
Inden prøven sås, skal der udføres en mos for at opnå større følsomhed. Prøven kan sås på Brucella-agar, hjerneinfusion eller soja-trypticase suppleret med 5% får- eller hesteblod.
Polymerasekædereaktion (PCR).
Vævsafsnit kan underkastes molekylærbiologiske teknikker til påvisning af DNA fra mikroorganismen.
Fordelen ved PCR er, at den kan bruges i analysen af prøver såsom spyt, hvilket muliggør diagnosen af H. pylori ikke-invasivt, selvom det faktum, at bakterierne er i spyt, ikke nødvendigvis er en indikation af en maveinfektion.
-Ikke-invasive metoder
Serologi
Denne metode har en følsomhed på 63-97%. Den består af måling af IgA-, IgM- og IGG-antistoffer gennem ELISA-teknikken. Det er en god diagnostisk mulighed, men den har begrænset nytte til overvågning af behandlingen..
Dette skyldes, at antistofferne kan forblive forhøjede i op til 6 måneder, efter at mikroorganismen er elimineret. Det har fordelen ved at være en hurtig, enkel og billigere metode end dem, der kræver biopsi-endoskopi..
Det skal bemærkes, at antistofferne genereres mod H. pylori, de tjener til diagnose, men forhindrer ikke kolonisering. Derfor er de mennesker, der erhverver H. pylori har tendens til at lide af kroniske sygdomme.
Åndedrætsprøve
Til denne test skal patienten indtage kulstofmærket urinstof (13C eller 14C). Når denne forbindelse kommer i kontakt med ureasen produceret af bakterierne, omdannes den til markeret kuldioxid (COto C14) og ammonium (NHto).
Kuldioxid passerer ind i blodbanen og derfra til lungerne, hvor det udåndes gennem åndedrættet. Patientens åndedrætsprøve samles i en ballon. En positiv test er bekræftende for infektion med denne bakterie.
Modificeret åndedrætsprøve
Det er det samme som det foregående, men i dette tilfælde tilføjes et kolloid på 99mTc, der ikke absorberes i fordøjelsessystemet.
Dette kolloid gør det muligt at visualisere produktionen af urinstof nøjagtigt på det sted i fordøjelsessystemet, hvor det genereres ved hjælp af et gammakamera.
Livscyklus
Helicobacter pylori i kroppen opfører den sig på to måder:
98% af befolkningen i H. pylori de bor gratis i maveslimen. Dette tjener som et reservoir for sammenhængende bakterier, der tjener til transmission.
Mens 2% er bundet til epitelceller, som opretholder infektionen.
Derfor er der to populationer, klæbende og ikke-klæbende, med forskellige overlevelsesegenskaber..
Patogeni
Når bakterierne kommer ind i kroppen, kan den hovedsagelig kolonisere gastrisk antrum ved hjælp af virulensfaktorer, den har..
Bakterierne kan vare længe installeret i maveslimhinden, nogle gange for livet uden at forårsage ubehag. Invaderer og koloniserer de dybe lag af gastrisk og tolvfingertarmslim gennem proteaser og phospholipaser.
Derefter fastgør den sig til de overfladiske epitelceller i maven og tolvfingertarmen uden at invadere væggen. Dette er en strategisk placering, som bakterierne indtager for at beskytte sig mod den ekstremt sure pH i mavelumen..
Samtidig på dette sted udfolder bakterierne urinstoffet for at alkalisere sit miljø yderligere og forblive levedygtige..
For det meste forekommer en kontinuerlig inflammatorisk reaktion i maveslimhinden, hvilket igen ændrer mekanismerne til regulering af mavesyresekretion. Sådan aktiveres visse ulcerogene mekanismer, såsom:
Hæmning af parietal cellefunktion gennem inhibering af somatostatin, hvor den utilstrækkelige produktion af gastrin er favoriseret.
Den producerede ammoniak plus VacA-cytotoksin-mishandling af epitelceller, hvilket forårsager læsioner i mave- eller duodenalslimhinden.
Derfor observeres degenerative ændringer af epiteloverfladen inklusive mucinudtømning, cytoplasmatisk vakuolisering og desorganisering af slimkirtlerne..
Inflammatorisk infiltration
De førnævnte læsioner resulterer i, at slimhinden og dens lamina propria bliver invaderet af en tæt infiltration af inflammatoriske celler. Oprindeligt kan infiltratet være minimalt med kun mononukleære celler.
Men senere kan betændelsen spredes med tilstedeværelsen af neutrofiler og lymfocytter, som forårsager skade på slim- og parietalcellerne, og der kan endda dannes mikroabscesser.
CagA-cytotoksinet for sin del kommer ind i gastrisk epitelcelle, hvor der udløses flere enzymatiske reaktioner, der forårsager reorganisering af actin-cytoskeletet.
De specifikke mekanismer til carcinogenese er ukendte. Imidlertid antages betændelse og aggression over en lang periode at føre til metaplasi og til sidst kræft..
Patologi
Generelt stammer kronisk overfladisk gastritis inden for et par uger eller måneder efter, at bakterierne har slået sig ned. Denne gastritis kan udvikle sig til et peptisk mavesår og senere føre til gastrisk lymfom eller adenocarcinom..
Ligeledes infektion med Helicobacter pylori er en tilstand, der disponerer for MALT-lymfom (mucosa-associeret lymfoid vævslymfom).
På den anden side nævner de seneste undersøgelser det Helicobacter pylori forårsager ekstragastriske sygdomme. Disse inkluderer: jernmangelanæmi og idiopatisk trombocytopeni purpura.
Også hudsygdomme som rosacea (den mest almindelige hudsygdom forbundet med H. pylori), kronisk kløe, kronisk idiopatisk urticaria, psoriasis blandt andre. Hos gravide kan det forårsage hyperemesis gravidarum.
Andre mindre hyppige steder, der menes at være H. pylori kan have en rolle, der forårsager patologi er på niveauet med:
Mellemøre, næsepolypper, lever (hepatocellulært carcinom), galdeblære, lunger (bronchiectasis og KOL kronisk obstruktiv lungesygdom).
Det har også været forbundet med øjensygdom (åbenvinklet glaukom), hjerte-kar-sygdomme, autoimmune lidelser, blandt andre.
Kliniske manifestationer
Denne patologi kan være asymptomatisk hos op til 50% af de voksne. Ellers kan det i den primære infektion forårsage kvalme og øvre mavesmerter, der kan vare op til to uger.
Senere forsvinder symptomerne for at dukke op igen senere, når gastritis og / eller mavesår er installeret.
I dette tilfælde er de mest almindelige symptomer kvalme, anoreksi, opkastning, epigastrisk smerte og endnu mindre specifikke symptomer såsom rap..
Mavesår kan forårsage alvorlig blødning, der kan kompliceres af peritonitis på grund af lækage af gastrisk indhold i bughulen.
Smitte
Mennesker med Helicobacter pylori de kan udskille bakterierne i deres afføring. På denne måde kan drikkevand blive forurenet. Derfor er den vigtigste kontamineringsvej for individet fækal-oral.
Det menes, at det kan være i vand eller i nogle grøntsager, der normalt spises rå, såsom salat og kål.
Disse fødevarer kan blive forurenet ved at blive vandet med forurenet vand. Imidlertid er mikroorganismen aldrig blevet isoleret fra vand..
En anden ualmindelig kontamineringsvej er oral-oral, men det blev dokumenteret i Afrika efter nogle mødres sædvane til at tygge deres børns mad på forhånd..
Endelig er smitte ved den iatrogene rute mulig. Denne vej består af kontaminering ved anvendelse af kontamineret eller dårligt steriliseret materiale i invasive procedurer, der involverer kontakt med gastrisk slimhinde..
Behandling
Helicobacter pylori in vitro det er modtageligt for en række forskellige antibiotika. Blandt dem: penicillin, nogle cephalosporiner, makrolider, tetracycliner, nitroimidazoler, nitrofuraner, quinoloner og bismuthsalte.
Men de er iboende resistente over for receptorblokkere (cimetidin og ranitidin), polymyxin og trimethoprim..
Blandt de mest succesrige behandlinger er der:
- Kombination af medicin, inklusive 2 antibiotika og 1 protonpumpehæmmer.
- Den mest almindelige kombination af antibiotika er clarithromycin + metronidazol eller clarithromycin + amoxicillin eller clarithromycin + furazolidon eller metronidazol + tetracyclin.
- Protonpumpehæmmeren kan være omeprazol eller esomeprazol.
- Nogle behandlinger kan også omfatte forbrug af vismut salte.
Behandlingen skal være afsluttet i mindst 14 dage, som anbefalet af FDA. Hos nogle patienter er denne terapi imidlertid vanskelig at tolerere. For dem anbefales det at kombinere behandlingen med forbruget af fødevarer, der indeholder probiotika.
Disse terapier er effektive, men i de senere år har der været modstand fra Helicobacter pylori metronidazol og clarithromycin.
Mikroorganismen kan udryddes, men reinfektion er mulig. I anden behandling til geninfektion anbefales brug af levofloxacin..
Referencer
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Mikrobiologisk diagnose. (5. udgave). Argentina, redaktionelt Panamericana S.A.
- Forbes B, Sahm D, Weissfeld A. Bailey & Scott mikrobiologisk diagnose. 12. udgave Argentina. Redaktionel Panamericana S.A; 2009.
- Ryan KJ, Ray C.. Sherris. Mikrobiologi Medical, 6. udgave McGraw-Hill, New York, U.S.A; 2010.
- Cava F og Cobas G. To årtier af Helicobacter pylori. VacciMonitor, 2003; 2 (1): 1-10
- González M, González N. Manual of Medical Microbiology. 2. udgave, Venezuela: Direktoratet for medier og publikationer ved University of Carabobo; 2011
- Testerman TL, Morris J. Beyond the stomach: en opdateret visning af Helicobacter pylori patogenese, diagnose og behandling. Verden J Gastroenterol. 2014; 20 (36): 12781-808.
- Safavi M, Sabourian R, Foroumadi A. Behandling af Helicobacter pylori-infektion: Nuværende og fremtidig indsigt. World J Clin sager. 2016; 4 (1): 5-19.


Endnu ingen kommentarer