
Hydroxids egenskaber, nomenklatur og eksempler

Det hydroxider er uorganiske og ternære forbindelser, der består af interaktionen mellem et metalkation og den funktionelle gruppe OH (hydroxidanion, OH-). De fleste af dem er ioniske, selvom de også kan have kovalente bindinger.
For eksempel kan et hydroxid repræsenteres som den elektrostatiske interaktion mellem kationen M+ og OH-anionen-, eller som den kovalente binding gennem M-OH-bindingen (lavere billede). I den første forekommer den ioniske binding, mens den anden er den kovalente. Denne kendsgerning afhænger i det væsentlige af metallet eller kationen M+, såvel som dets ladning og ioniske radius.
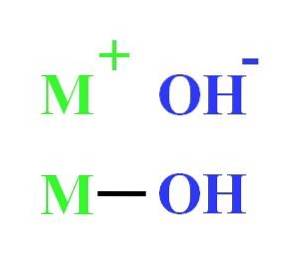
Da de fleste af dem kommer fra metaller, svarer det til at nævne dem som metalhydroxider.
Artikelindeks
- 1 Hvordan dannes de??
- 2 Egenskaber ved hydroxider
- 2.1 OH-anion-
- 2.2 Ionisk og grundlæggende karakter
- 2.3 Periodisk tendens
- 2.4 Amfoterisme
- 2.5 Strukturer
- 2.6 Dehydrering reaktion
- 3 Nomenklatur
- 3.1 Traditionel
- 3.2 Lager
- 3.3 Systematik
- 4 Eksempler på hydroxider
- 5 Referencer
Hvordan dannes de?
Der er to hovedsyntetiske veje: ved at reagere det tilsvarende oxid med vand eller med en stærk base i et surt medium:
MO + HtoO => M (OH)to
MO + H+ + Åh- => M (OH)to
Kun de metaloxider, der er opløselige i vand, reagerer direkte for at danne hydroxidet (første kemiske ligning). Andre er uopløselige og kræver sure arter for at frigive M+, som derefter interagerer med OH- fra stærke baser (anden kemisk ligning).
Disse stærke baser er imidlertid metalhydroxider NaOH, KOH og andre fra gruppen af alkalimetaller (LiOH, RbOH, CsOH). Disse er ioniske forbindelser, der er meget opløselige i vand, derfor deres OH- er frie til at deltage i kemiske reaktioner.
På den anden side er der metalhydroxider, der er uopløselige og derfor meget svage baser. Nogle af dem er endda sure, som det er tilfældet med tellursyre, Te (OH)6.
Hydroxidet etablerer en opløselighedsligevægt med det omgivende opløsningsmiddel. Hvis det f.eks. Er vand, udtrykkes ligevægten som følger:
M (OH)to <=> Mto+(ac) + OH-(ac)
Hvor (ac) angiver, at mediet er vandigt. Når det faste stof er uopløseligt, er den opløste OH-koncentration lille eller ubetydelig. Af denne grund kan uopløselige metalhydroxider ikke danne opløsninger så basiske som NaOH..
Af ovenstående kan det udledes, at hydroxider udviser meget forskellige egenskaber, knyttet til den kemiske struktur og interaktionerne mellem metal og OH. Selvom mange således er ioniske med varierede krystallinske strukturer, har andre således komplekse og uordnede polymere strukturer..
Egenskaber ved hydroxider
OH anion-
Hydroxylionen er et oxygenatom kovalent bundet til hydrogen. Dette kan således let repræsenteres som OH-. Den negative ladning er placeret på iltet, hvilket gør denne anion til en elektrondoneart: en base.
Hvis OH- donerer sine elektroner til et hydrogen, dannes et H-molekyletoO. Du kan også donere dine elektroner til positivt ladede arter: såsom metalcentre M+. Således dannes et koordinationskompleks gennem den dative M-OH-binding (ilt tilvejebringer paret elektroner).
For at dette kan ske, skal iltet være i stand til at koordinere effektivt med metallet, ellers vil interaktionerne mellem M og OH have en markant ionisk karakter (M+ Åh-). Da hydroxylionen er den samme i alle hydroxider, ligger forskellen mellem dem alle i kationen, der ledsager den.
På samme måde, fordi denne kation kan komme fra ethvert metal i det periodiske system (gruppe 1, 2, 13, 14, 15, 16 eller overgangsmetallerne), varierer egenskaberne af sådanne hydroxider enormt, skønt alt sammen overvejer nogle aspekter til fælles.
Ionisk og grundlæggende karakter
Selv om de har koordinationsbindinger i hydroxider, har de en latent ionisk karakter. I nogle, såsom NaOH, er deres ioner en del af et krystalgitter, der består af Na-kationer+ og OH-anioner- i forhold 1: 1; det vil sige for hver Na-ion+ der er en OH-ion- modstykke.
Afhængigt af metalets ladning vil der være mere eller mindre OH-anioner- omkring det. For eksempel til et metalkation Mto+ der vil være to OH-ioner- interagerer med ham: M (OH)to, hvad der er tegnet som HO- Mto+ Åh-. På samme måde sker det med metallerne M3+ og med andre med mere positive ladninger (selvom de sjældent overstiger 3+).
Denne ioniske karakter er ansvarlig for mange af de fysiske egenskaber, såsom smelte- og kogepunkter. Disse er høje, hvilket afspejler de elektrostatiske kræfter, der virker inden for krystalgitteret. Når hydroxider opløses eller smelter, kan de ligeledes lede elektrisk strøm på grund af deres ioners mobilitet..
Imidlertid har ikke alle hydroxider de samme krystalgitter. Dem med de mest stabile vil være mindre tilbøjelige til at opløses i polære opløsningsmidler som vand. Som en generel regel, jo mere adskilte M's ioniske radier+ og OH-, mere opløseligt vil være det samme.
Periodisk tendens
Dette forklarer, hvorfor opløseligheden af alkalimetalhydroxider øges, når man bevæger sig ned ad gruppen. Den stigende rækkefølge af opløseligheder i vand for disse er således som følger: LiOH OH- er en lille anion, og når kationen bliver mere voluminøs, svækkes krystalgitteret energisk. På den anden side danner jordalkalimetaller mindre opløselige hydroxider på grund af deres højere positive ladninger. Dette skyldes, at Mto+ tiltrækker OH stærkere- sammenlignet med M+. Ligeledes er dets kationer mindre og derfor mindre ulige i størrelse med hensyn til OH-. Resultatet af dette er eksperimentelt bevis for, at NaOH er meget mere basisk end Ca (OH).to. Den samme ræsonnement kan anvendes på andre hydroxider, enten for overgangsmetalerne eller for p-blokmetalerne (Al, Pb, Te osv.). Desuden er jo mindre og større den ioniske radius og den positive ladning af M+, jo lavere er den ioniske karakter af hydroxidet, med andre ord dem med meget høje ladningstætheder. Et eksempel på dette forekommer med berylliumhydroxid, Be (OH)to. Det skal han væreto+ det er en meget lille kation, og dens divalente ladning gør den elektrisk meget tæt. Hydroxider M (OH)to reagerer med syrer til dannelse af et vandigt kompleks, det vil sige M+ ender omgivet af vandmolekyler. Der er dog et begrænset antal hydroxider, der også kan reagere med baser. Disse er såkaldte amfotere hydroxider. Amfotere hydroxider reagerer med både syrer og baser. Den anden situation kan repræsenteres af følgende kemiske ligning: M (OH)to + Åh- => M (OH)3- Men hvordan skal man bestemme, om et hydroxid er amfotert? Gennem et simpelt laboratorieeksperiment. Fordi mange metalhydroxider er uopløselige i vand, tilføjer en stærk base til en opløsning med M-ionerne+ opløst, for eksempel Al3+, det tilsvarende hydroxid udfældes: Til3+(aq) + 3OH-(ac) => Al (OH)3(s) Men at have et overskud af OH- hydroxidet reagerer fortsat: Al (OH)3(s) + OH- => Al (OH)4-(ac) Som et resultat solvatiseres det nye negativt ladede kompleks af de omgivende vandmolekyler og opløser det hvide aluminiumhydroxidfaststof. De hydroxider, der forbliver uændrede med ekstra tilsætning af base, opfører sig ikke som syrer og er derfor ikke amfotere. Hydroxider kan have krystallinske strukturer svarende til dem af mange salte eller oxider; nogle enkle og andre meget komplekse. Derudover kan dem, hvor der er et fald i ionisk karakter, præsentere metalcentre forbundet med iltbroer (HOM-O-MOH). I løsning er strukturer forskellige. Selvom det for stærkt opløselige hydroxider er nok at betragte dem som ioner opløst i vand, er det nødvendigt for andre at tage hensyn til koordineringskemi. Således hver kation M+ den kan koordineres til et begrænset antal arter. Jo større det er, jo større er antallet af molekyler vand eller OH.- knyttet til det. Herfra kommer den berømte koordinationsoktaeder af mange metaller opløst i vand (eller i ethvert andet opløsningsmiddel): M (OHto)6+n, hvor n er lig med metalets positive ladning. Cr (OH)3, for eksempel danner den faktisk en oktaeder. Hvordan? I betragtning af forbindelsen som [Cr (OHto)3(OH)3], hvoraf tre af vandmolekylerne er erstattet af OH-anioner-. Hvis alle molekylerne blev erstattet af OH-, derefter komplekset med negativ ladning og oktaedrisk struktur [Cr (OH)6]3-. -3-ladningen er resultatet af OH's seks negative ladninger-. Hydroxider kan betragtes som "hydratiserede oxider". Imidlertid er "vand" i dem i direkte kontakt med M+; mens de er i de hydratiserede oxider MO nHtoEller vandmolekylerne er en del af en ekstern koordinationssfære (de er ikke tæt på metallet). Disse vandmolekyler kan ekstraheres ved opvarmning af en prøve af hydroxid: M (OH)to + Q (varme) => MO + HtoELLER MO er metaloxidet dannet som et resultat af dehydrering af hydroxidet. Et eksempel på denne reaktion er den, der observeres, når kobberhydroxid, Cu (OH), er dehydreretto: Cu (OH)to (blå) + Q => CuO (sort) + HtoELLER Hvad er den rigtige måde at nævne hydroxider på? IUPAC foreslog tre nomenklaturer til dette formål: den traditionelle, bestanden og den systematiske. Det er korrekt at bruge en af de tre, men for nogle hydroxider kan det være mere praktisk eller praktisk at nævne det på en eller anden måde. Den traditionelle nomenklatur er simpelthen at tilføje suffikset -ico til metalets højeste valens; og suffikset -oso til det laveste. Således, for eksempel, hvis metallet M har valenser +3 og +1, er hydroxidet M (OH)3 det kaldes hydroxid (metalnavn)ico, mens MOH-hydroxid (metalnavn)bjørn. For at bestemme metalets valens i hydroxidet skal du bare se på tallet efter OH, der er lukket i parentes. Således M (OH)5 betyder, at metallet har en ladning eller valens på +5. Den største ulempe ved denne nomenklatur er imidlertid, at det kan være kompliceret for metaller med mere end to oxidationstilstande (såsom krom og mangan). I sådanne tilfælde bruges præfikserne hyper- og hypo- til at betegne de højeste og laveste valenser.. Således, hvis M i stedet for kun at have +3 og +1 valenser, har den også +4 og +2, så er navnene på dens hydroxider med de højeste og laveste valenser: hydroxid hyper(metalnavn)ico, og hydroxid hikke(metalnavn)bjørn. Af alle nomenklaturer er dette den enkleste. Her er navnet på hydroxidet simpelthen efterfulgt af valensen af metallet, der er lukket i parentes og skrevet med romertal. Igen for M (OH)5, for eksempel vil din lagernomenklatur være: (metalnavn) hydroxid (V). (V) betegner derefter (+5). Endelig er den systematiske nomenklatur kendetegnet ved at anvende multiplikationspræfikser (di-, tri-, tetra-, penta-, hexa- osv.). Disse præfikser bruges til at specificere både antallet af metalatomer og OH-ioner.-. På denne måde er M (OH)5 navngivet som: (metalnavn) pentahydroxid. I tilfælde af Hgto(OH)to, for eksempel ville det være dimercurisk dihydroxid; et af de hydroxider, hvis kemiske struktur er kompleks ved første øjekast. Nogle eksempler på hydroxider og deres tilsvarende nomenklaturer er som følger: -NaOH (natriumhydroxid) -Ca (OH) 2 (Calciumhydroxid) -Fe (OH)3. (Jernhydroxid; jern (III) hydroxid; eller jerntrihydroxid) -V (OH)5 (Pervanadisk hydroxid; Vanadium (V) hydroxid; eller vanadium pentahydroxid). -Sn (OH)4 (Stanisk hydroxid; tin (IV) hydroxid; eller tin tetrahydroxid). -Ba (OH)to (Bariumhydroxid eller bariumdihydroxid). -Mn (OH)6 (Manganhydroxid, mangan (VI) hydroxid eller manganhexahydroxid). -AgOH (sølvhydroxid, sølvhydroxid eller sølvhydroxid). Bemærk, at der for denne forbindelse ikke er nogen skelnen mellem bestand og systematiske nomenklaturer. -Pb (OH)4 (Blyhydroxid, bly (IV) hydroxid eller blytetrahydroxid). -LiOP (lithiumhydroxid). -Cd (OH) 2 (cadmiumhydroxid) -Ba (OH)to (Bariumhydroxid) -ChromhydroxidAmfoterisme
Strukturer
Dehydrering reaktion
Nomenklatur
Traditionel
Lager
Systematisk
Eksempler på hydroxider


Referencer


Endnu ingen kommentarer