
Hvad er materiens kvantitative egenskaber?
Det kvantitative egenskaber af stof er karakteristika for stof, der kan måles -temperatur, masse, densitet ... - og hvoraf størrelser kan udtrykkes.
Materiets fysiske egenskaber er egenskaber ved et stof, som kan observeres og måles uden at ændre stoffets identitet. De klassificeres i kvantitative egenskaber og kvalitative egenskaber.

Ordet kvantitativ henviser til kvantitative data eller information, der er baseret på mængder opnået gennem en kvantificerbar måleproces, det vil sige ethvert objektivt målegrundlag. I modsætning hertil registrerer kvalitativ information beskrivende, subjektive eller vanskelige målbare kvaliteter.
For at forstå det kvantitative udtryk er det nødvendigt at forstå, at dets modsatte, de kvalitative egenskaber, er dem, der kan observeres gennem sanserne: syn, lyd, lugt, berøring; uden at tage målinger som farve, lugt, smag, struktur, duktilitet, smidighed, klarhed, glans, homogenitet og tilstand.
Tværtimod er materiens kvantitative fysiske egenskaber dem, der kan måles og tildeles en bestemt værdi..
Kvantitative egenskaber er ofte unikke for et bestemt element eller forbindelse, plus registrerede værdier er tilgængelige for reference (kan søges i tabeller eller grafer).
Enhver kvantitativ egenskab indebærer et tal og en tilsvarende enhed samt et tilknyttet instrument, der gør det muligt at måle det..
Eksempler på kvantitative egenskaber ved stof
Temperatur

Det er et mål for et stofs varme med henvisning til en standardværdi. Det er den kinetiske energi (bevægelse) af partiklerne i et stof, målt i grader Celsius (° C) eller grader Fahrenheit (° F) med et termometer.
Smeltepunkt

Temperatur, hvor skiftet fra fast tilstand til flydende tilstand forekommer. Det måles i grader celsius (° C) eller grader Fahrenheit (° F). Et termometer bruges til at måle det.
Kogepunkt
Temperatur, hvor skiftet fra væske til gasform sker. Det måles i grader celsius (° C) eller grader Fahrenheit (° F). Måleinstrumentet er termometeret.
Massefylde

Mængden af masse i et givet volumen af et stof. Vandtætheden er 1,0 g / ml og er ofte referencen for andre stoffer.
Det måles i gram over kubikcentimeter (g / cm3) eller gram over milliliter (g / ml) eller gram over liter (g / l) osv. Og metoden til markerede volumener bruges.
Ledningsevne
Et stofs ledningsevne til at lede elektricitet eller varme. Hvis det er elektricitet, måles det i ohm (ohm), og hvis det er varme, måles det i watt pr. Meter Kelvin (W / m K). Der anvendes henholdsvis et multimeter og en temperatursensor.
pH
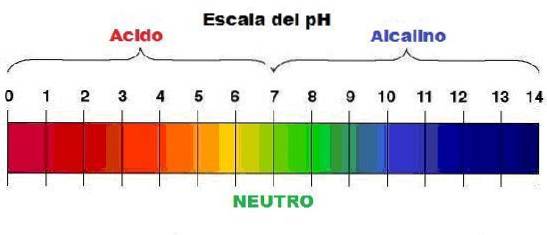
Andelen af vandmolekyler, der har fået et brintatom (H3ELLER+) til vandmolekyler, der har mistet et hydrogenatom (OH-).
Dens enhed går fra 1 til 14, hvilket indikerer mængden af H3ELLER+. Indikatorer (kemiske produkter i opløsning) bruges til at måle pH, som tilsættes til den testede opløsning og reagerer med den, hvilket forårsager en farveændring til kendte mængder H3ELLER+.
Opløselighed

Mængden af stof (kaldet opløst stof), der kan opløses i en given mængde af et andet (opløsningsmiddel).
Almindeligt målt i gram opløst stof pr. 100 gram opløsningsmiddel eller i gram pr. Liter (g / l) og i mol pr. Liter (mol / l). For at måle det bruges værktøjer som balance og den markerede volumenmetode..
Viskositet
Væskens modstand mod at strømme. Det måles i Poise (P) og i Stokes (S). Og dens måleinstrument kaldes et viskosimeter.
Hårdhed
Evne til at modstå ridser. Det måles med hårdhedsskalaer, såsom Brinell, Rockwell og Vicker; med et durometer indstillet til den ønskede skala.
Masse
Det er mængden af stof i en prøve og måles i gram (g), kg (kg), pund (lb) osv. Og det måles med skalaen.
Længde
Det er måling af længde fra den ene ende til den anden, og de mest anvendte måleenheder er centimeter (cm), meter (m), kilometer (km), inches (in) og fødder (ft). Lineal, indikator, kilometertæller eller digitalt mikrometer er måleinstrumenterne.
Bind
Det er den mængde plads, der optages af et stof og måles i kubikcentimeter (cm3), ml (ml) eller liter (L). Den markerede volumen metode bruges.
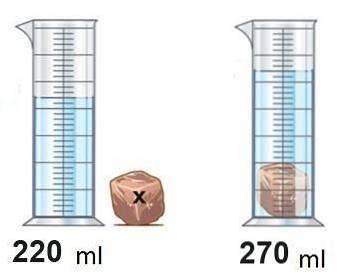
Vægt
Det er tyngdekraften på et stof, og dets måleenhed er newton (N), pundkraften (lbf), dynerne (din) og kilopondene (kp).
Vejr
Det er varigheden af en begivenhed, den måles i sekunder, minutter (min) og timer (h). Der anvendes et ur eller stopur.
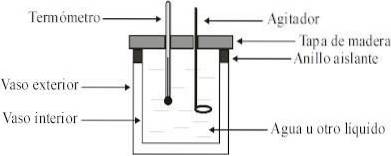
Specifik varme
Det defineres som den mængde varme, der er nødvendig for at hæve temperaturen på 1,0 g af et stof med 1 grad Celsius..
Det er en indikation af, hvor hurtigt eller langsomt en bestemt masse af et objekt bliver opvarmet eller kølet. Jo lavere den specifikke varme er, desto hurtigere bliver den opvarmet eller kølet ned.
Den specifikke varme af vand er 4,18 J / g C og måles næsten altid i disse enheder (Joule over gram pr. Grad Celsius). Det måles med kalorimeteret.
Fusionsvarme
Det er den mængde varme, der er nødvendig for at smelte nøjagtigt en bestemt masse af dette stof. Fusionsvarmen med vand er 334 J / g, og ligesom den specifikke varme måles den med kalorimeteret og udtrykkes i Joule over gram pr. Grad Celsius.
Fordampningsvarme
Det er den mængde varme, der er nødvendig for at fordampe nøjagtigt en bestemt masse af dette stof. Fordampningsvarmen for vand er 2260 J / g (Joule over gram pr. Grad Celsius). Det måles med kalorimeteret.
Ioniseringsenergi
Det er den energi, der er nødvendig for at fjerne de svageste eller længste elektroner fra et atom. Ioniseringsenergi er angivet i elektronvolt (eV), joule (J) eller kilojoule pr. Mol (kJ / mol).
Metoden, der bruges til at bestemme den, kaldes atomspektroskopi, som bruger stråling til at måle energiniveauet.
Temaer af interesse
Generelle egenskaber.
Omfattende egenskaber.
Intensive egenskaber.
Materialets egenskaber.
Referencer
- Business Dictionary redaktør team. (2017). "Kvantitativt". Gendannet fra businessdictionary.com.
- Sims, C. (2016). "Fysiske egenskaber ved materie". Gendannet fra slideplayer.com.
- Ahmed, A. (2017). "Kvantitative observationer - materieegenskaber". Gendannet fra sciencedirect.com.
- Helmenstine, A. (2017). "Liste over fysiske egenskaber". Gendannet fra thoughtco.com.
- Ma, S. (2016). "Materialets fysiske og kemiske egenskaber". Gendannet fra chem.libretexts.org.
- Carter, J. (2017). "Kvalitative og kvantitative egenskaber". Gendannet fra cram.com.


Endnu ingen kommentarer