
ATP (adenosintriphosphat) struktur, funktioner, hydrolyse
Det ATP (adenosintrifosfat) er et organisk molekyle med højenergibindinger, der består af en adeninring, en ribose og tre fosfatgrupper. Det har en grundlæggende rolle i stofskiftet, da det transporterer den nødvendige energi for at holde en række cellulære processer effektivt..
Det er almindeligt kendt under betegnelsen "energivaluta", da dets dannelse og anvendelse sker let, hvilket tillader "betalt" hurtigt for kemiske reaktioner, der kræver energi.

Selvom molekylet for det blotte øje er lille og simpelt, lagrer det en betydelig mængde energi i sine bindinger. Fosfatgrupper har negative ladninger, som er i konstant frastødning, hvilket gør det til en labil og let brudt binding..
Hydrolysen af ATP er nedbrydningen af molekylet ved tilstedeværelsen af vand. Ved denne proces frigives den indeholdte energi.
Der er to hovedkilder til ATP: phosphorylering på substratniveau og oxidativ phosphorylering, hvor sidstnævnte er den vigtigste og mest anvendte af cellen..
Oxidativ phosphorylering parrer oxidation af FADHto og NADH + H+ i mitokondrier og substratniveau sker phosphorylering uden for elektrontransportkæden, i veje såsom glykolyse og tricarboxylsyrecyklus.
Dette molekyle er ansvarlig for at tilvejebringe den nødvendige energi til de fleste af de processer, der forekommer inde i cellen for at finde sted, fra proteinsyntese til bevægelse. Derudover tillader det trafik af molekyler gennem membraner og virker på cellesignalering..
Artikelindeks
- 1 Struktur
- 2 funktioner
- 2.1 Energiforsyning til natrium- og kaliumtransport over membranen
- 2.2 Deltagelse i proteinsyntese
- 2.3 Forsyning af energi til bevægelse
- 3 Hydrolyse
- 3.1 Hvorfor forekommer denne frigivelse af energi??
- 4 Sådan får du ATP
- 4.1 Oxidativ fosforylering
- 4.2 Substratniveau fosforylering
- 5 ATP-cyklus
- 6 Andre energimolekyler
- 7 Referencer
Struktur
ATP er, som navnet antyder, et nukleotid med tre fosfater. Dens særlige struktur, specifikt de to pyrofosfatbindinger, gør det til en energirig forbindelse. Den består af følgende elementer:
- En nitrogenholdig base, adenin. Nitrogenbaser er cykliske forbindelser, der indeholder en eller flere nitrogen i deres struktur. Vi finder dem også som komponenter i nukleinsyrer, DNA og RNA.
- Ribose er placeret i midten af molekylet. Det er et sukker af pentose-typen, da det har fem kulstofatomer. Dens kemiske formel er C5H10ELLER5. Carbon 1 af ribose er fastgjort til adeninringen.
- Tre fosfatradikaler. De sidste to er "højenergibindinger" og er repræsenteret i de grafiske strukturer med vippesymbolet: ~. Fosfatgruppen er en af de vigtigste i biologiske systemer. De tre grupper kaldes alfa, beta og gamma, fra det nærmeste til det længste.
Dette link er meget labilt, så det opdeles hurtigt, let og spontant, når organismens fysiologiske forhold berettiger det. Dette sker, fordi de negative ladninger fra de tre fosfatgrupper konstant forsøger at bevæge sig væk fra hinanden..
Funktioner
ATP spiller en uundværlig rolle i energimetabolismen i stort set alle levende organismer. Af denne grund omtales det ofte som en energivaluta, da den kontinuerligt kan bruges og genopfyldes på få minutter..
Direkte eller indirekte leverer ATP energi til hundredvis af processer ud over at fungere som en fosfatdonor.
Generelt fungerer ATP som et signalmolekyle i de processer, der forekommer inde i cellen, det er nødvendigt at syntetisere komponenterne i DNA og RNA, og til syntese af andre biomolekyler deltager det i blandt andet handel med membraner.
Anvendelsen af ATP kan opdeles i hovedkategorier: transport af molekyler gennem biologiske membraner, syntese af forskellige forbindelser og endelig mekanisk arbejde.
ATP's funktioner er meget brede. Desuden er det involveret i så mange reaktioner, at det ville være umuligt at navngive dem alle. Derfor vil vi diskutere tre specifikke eksempler for at eksemplificere hver af de tre nævnte anvendelser..
Energiforsyning til natrium- og kaliumtransport over membranen
Cellen er et meget dynamisk miljø, der kræver, at specifikke koncentrationer opretholdes. De fleste molekyler kommer ikke tilfældigt eller tilfældigt ind i cellen. For at et molekyle eller stof kan komme ind, skal det gøres af sin specifikke transportør.
Transportører er membranomspændende proteiner, der fungerer som cellulære "gatekeepers", der styrer materialestrømmen. Derfor er membranen semi-permeabel: den tillader visse forbindelser at komme ind, og andre ikke..
En af de mest kendte transporter er natrium-kaliumpumpen. Denne mekanisme er klassificeret som aktiv transport, da ioners bevægelse sker mod deres koncentrationer, og den eneste måde at udføre denne bevægelse på er ved at indføre energi i systemet i form af ATP..
Det anslås, at en tredjedel af ATP dannet i cellen bruges til at holde pumpen aktiv. Natriumioner pumpes konstant til ydersiden af cellen, mens kaliumioner pumpes i den modsatte retning..
Logisk set er brugen af ATP ikke begrænset til transport af natrium og kalium. Der er andre ioner, såsom calcium, magnesium, blandt andre, der har brug for denne energivaluta for at komme ind.
Deltagelse i proteinsyntese
Proteinmolekyler består af aminosyrer, der er bundet sammen af peptidbindinger. For at danne dem kræves det, at fire højenergibindinger brydes. Med andre ord skal et betydeligt antal ATP-molekyler hydrolyseres til dannelse af et protein med gennemsnitlig længde..
Proteinsyntese forekommer i strukturer kaldet ribosomer. Disse er i stand til at fortolke den kode, som messenger-RNA har, og oversætte den til en aminosyresekvens, en ATP-afhængig proces..
I de mest aktive celler kan proteinsyntese lede op til 75% af ATP syntetiseret i dette vigtige arbejde.
På den anden side syntetiserer cellen ikke kun proteiner, den har også brug for lipider, kolesterol og andre essentielle stoffer, og for at gøre det kræver den energi indeholdt i ATP-bindingerne..
Giv energi til bevægelse
Mekanisk arbejde er en af de vigtigste funktioner i ATP. For eksempel for at vores krop kan sammentrække muskelfibre, er det nødvendigt med store mængder energi..
I muskler kan kemisk energi omdannes til mekanisk energi takket være omorganiseringen af proteinerne med evnen til at trække sig sammen, der danner den. Længden af disse strukturer er modificeret, forkortet, hvilket skaber en spænding, der oversættes til dannelsen af bevægelse.
I andre organismer forekommer cellernes bevægelse også takket være tilstedeværelsen af ATP. For eksempel forekommer bevægelse af cilia og flagella, der tillader bevægelse af visse encellede organismer ved brug af ATP.
En anden særlig bevægelse er den amøbeiske, der involverer fremspring af en pseudopod ved celleenderne. Flere celletyper bruger denne bevægelsesmekanisme, herunder leukocytter og fibroblaster..
I tilfælde af kimceller er bevægelse vigtig for en effektiv udvikling af embryoet. Embryonale celler bevæger sig vigtige afstande fra deres oprindelsessted til det område, hvor de skal have specifikke strukturer.
Hydrolyse
Hydrolysen af ATP er en reaktion, der involverer nedbrydningen af molekylet ved tilstedeværelsen af vand. Reaktionen er repræsenteret som følger:
ATP + Vand ⇋ ADP + Pjeg + Energi. Hvor, udtrykket Pjeg henviser til den uorganiske phosphatgruppe, og ADP er adenosindiphosphat. Bemærk, at reaktionen er reversibel.
Hydrolysen af ATP er et fænomen, der involverer frigivelse af en enorm mængde energi. Brud på en hvilken som helst af pyrofosfatbindingerne resulterer i frigivelse af 7 kcal pr. Mol - specifikt 7,3 fra ATP til ADP og 8,2 til produktion af adenosinmonophosphat (AMP) fra ATP. Dette svarer til 12.000 kalorier pr. Mol ATP..
Hvorfor forekommer denne frigivelse af energi?
Fordi hydrolyseprodukterne er meget mere stabile end den oprindelige forbindelse, det vil sige ATP.
Det skal nævnes, at kun den hydrolyse, der forekommer på pyrofosfatbindingerne for at give anledning til dannelsen af ADP eller AMP, fører til frembringelse af energi i betydelige mængder.
Hydrolysen af de andre bindinger i molekylet giver ikke så meget energi, med undtagelse af hydrolyse af uorganisk pyrophosphat, som har en stor mængde energi.
Frigivelsen af energi fra disse reaktioner bruges til at udføre metaboliske reaktioner inde i cellen, da mange af disse processer har brug for energi til at fungere, både i de indledende trin af nedbrydningsveje og i biosyntese af forbindelser..
For eksempel involverer de første trin i glukosemetabolisme phosphorylering af molekylet. I de følgende trin genereres ny ATP for at opnå en positiv nettofortjeneste.
Fra et energisynspunkt er der andre molekyler, hvis frigivelsesenergi er større end ATP, inklusive 1,3 bisphosphoglycerat, carbamylphosphat, kreatininfosfat og phosphoenolpyruvat..
Opnåelse af ATP
ATP kan opnås på to måder: oxidativ phosphorylering og phosphorylering på substratniveau. Førstnævnte kræver ilt, mens sidstnævnte ikke gør det. Cirka 95% af det dannede ATP forekommer i mitokondrier.
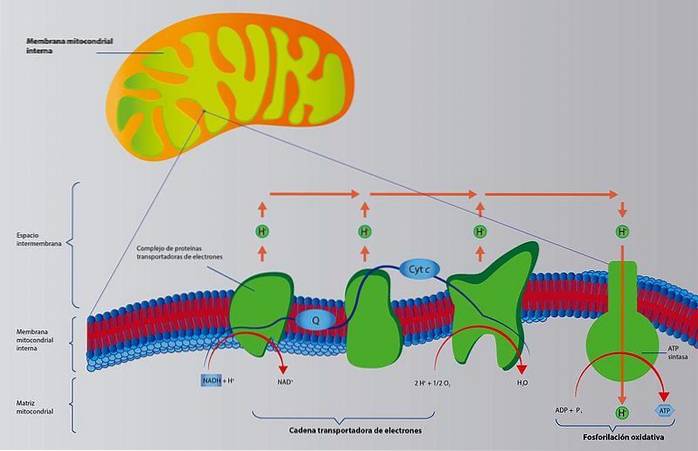
Oxidativ fosforylering
Oxidativ phosphorylering involverer en to-fase næringsstofoxidationsproces: opnåelse af reducerede co-enzymer NADH og FADHto stammer fra vitaminer.
Reduktionen af disse molekyler kræver anvendelse af hydrogen fra næringsstoffer. I fedt er produktionen af co-enzymer bemærkelsesværdig takket være den enorme mængde hydrogen, de har i deres struktur sammenlignet med peptider eller kulhydrater.
Selvom der er flere ruter for coenzymproduktion, er den vigtigste rute Krebs-cyklussen. Derefter koncentreres de reducerede co-enzymer i åndedrætskæderne placeret i mitokondrier, som overfører elektronerne til ilt..
Elektrontransportkæden består af en række membrankoblede proteiner, der pumper protoner (H +) udad (se billede). Disse protoner kommer ind og krydser membranen igen ved hjælp af et andet protein, ATP-syntase, der er ansvarlig for syntesen af ATP.
Med andre ord har vi, at reduktionen af co-enzymer, mere ADP og ilt genererer vand og ATP.
Substratniveau fosforylering
Fosforylering på substratniveau er ikke så vigtig som den ovenfor beskrevne mekanisme, og da den ikke kræver iltmolekyler, er den ofte forbundet med gæring. Selvom det er meget hurtigt, trækker denne rute lidt energi ud, hvis vi sammenligner den med oxidationsprocessen, ville den være omkring femten gange mindre.
I vores krop forekommer gæringsprocesser på muskelniveau. Dette væv kan fungere uden ilt, så det er muligt, at et glukosemolekyle nedbrydes til mælkesyre (når vi f.eks. Udfører en udtømmende sportsaktivitet).
I gæringer har det endelige produkt stadig energipotentiale, der kan ekstraheres. I tilfælde af gæring i muskler er kulstofferne i mælkesyre på det samme reduktionsniveau som det oprindelige molekyle: glucose.
Således sker energiproduktion gennem dannelsen af molekyler, der har bindinger med høj energi, inklusive 1,3-bisphosphoglyrat og phosphoenolpyruvat..
I glykolyse er f.eks. Hydrolysen af disse forbindelser forbundet med produktionen af ATP-molekyler, deraf udtrykket "på substratniveau".
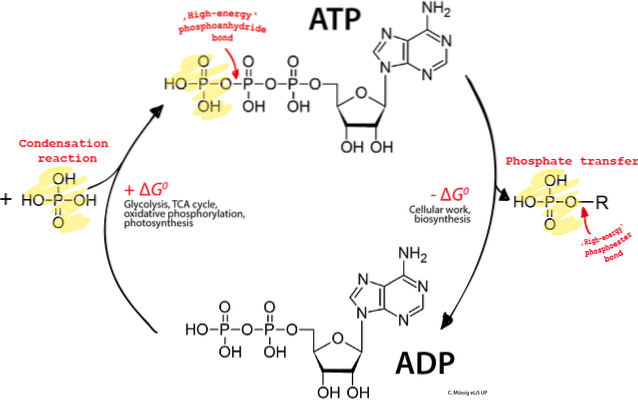
ATP-cyklus
ATP lagres aldrig. Det er i en kontinuerlig cyklus af brug og syntese. Dette skaber en balance mellem det dannede ATP og dets hydrolyserede produkt, ADP..
Andre energimolekyler
ATP er ikke det eneste molekyle, der består af bisphosphatnukleosider, der findes i cellulær metabolisme. Der er et antal molekyler med strukturer, der ligner ATP, der har sammenlignelig energifunktion, selvom de ikke er så populære som ATP.
Det mest fremtrædende eksempel er GTP, guanosintriphosphat, som anvendes i den velkendte Krebs-cyklus og i den glukoneogene vej. Andre mindre anvendte er CTP, TTP og UTP.
Referencer
- Guyton, A. C., & Hall, J. E. (2000). Lærebog i human fysiologi.
- Hall, J. E. (2017). Guyton E Hall-afhandling om medicinsk fysiologi. Elsevier Brasilien.
- Hernandez, A. G. D. (2010). Ernæringsafhandling: Sammensætning og ernæringskvalitet af fødevarer. Panamerican Medical Ed..
- Lim, M. Y. (2010). Det væsentlige i stofskifte og ernæring. Elsevier.
- Pratt, C. W., og Kathleen, C. (2012). Biokemi. Editorial The Modern Manual.
- Voet, D., Voet, J. G., & Pratt, C. W. (2007). Fundamentals of Biochemistry. Redaktionel Médica Panaméricana.

Endnu ingen kommentarer