
Sodium bisulfite (NaHSO3) struktur, egenskaber, anvendelser, produktion

Det natriumbisulfit er et uorganisk fast stof dannet af en natriumion Na+ og en bisulfition HSO3-. Dens kemiske formel er NaHSO3. Det er et hvidt krystallinsk fast stof og på grund af dets antioxidantegenskaber bruges det i vid udstrækning som et fødevarekonserveringsmiddel (for eksempel i nogle syltetøj).
NaHSO3 det er en reducerende kemisk forbindelse, som er det modsatte af oxidant, og derfor fungerer den som en antioxidant i mange af dens anvendelser, såsom i spiselige produkter, da det forhindrer deres forringelse.

Imidlertid er denne anvendelse blevet sat i tvivl, da der er rapporteret om tilfælde af astma hos mennesker, efter at de har spist mad, der indeholder natriumbisulfit. Det siges endda at ødelægge vitamin B1 i disse.
Internationale sundhedsorganisationer har begrænset brugen til mikromængder i mad.
Imidlertid har natriumbisulfit mange andre anvendelser, såsom ved opnåelse af jod, som et anti-infektiøst, til at gøre væv lysere, til fordøjelsen af træ under fremstillingen af papirmasse, som et desinfektionsmiddel til øl- og vinfade osv.
Artikelindeks
- 1 Kemisk struktur
- 2 Nomenklatur
- 3 egenskaber
- 3.1 Fysisk tilstand
- 3.2 Molekylvægt
- 3.3 Smeltepunkt
- 3.4 Tæthed
- 3.5 Opløselighed
- 3,6 pH
- 3.7 Kemiske egenskaber
- 3.8 Risici
- 4 Opnåelse
- 5 anvendelser
- 5.1 I papirmasse- og papirindustrien
- 5.2 I fødevareindustrien
- 5.3 Kontrovers over dets anvendelse i mad
- 5.4 I landbrugsapplikationer
- 5.5 Ved opnåelse af jod
- 5.6 I møbel- og træindustrien
- 5.7 I forskellige applikationer
- 6 Referencer
Kemisk struktur
Sodium bisulfite består af en natriumkation Na+ og en bisulfitanion HSO3-.
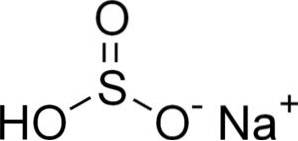
I vandige opløsninger danner bisulfit 4 arter. I fortyndet opløsning er der en balance mellem nedenstående strukturer:
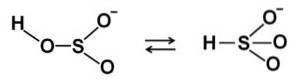
Når koncentrationen stiger, interagerer to bisulfitmolekyler med hinanden og danner pyrosulfitionen StoELLER5to-:
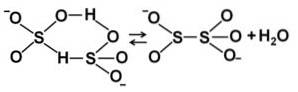
Nomenklatur
-Natriumbisulfit
-Natriumhydrogensulfit
-Natriumhydrosulfit.
Ejendomme
Fysisk tilstand
Fast hvid krystallinsk.
Molekylær vægt
104,06 g / mol
Smeltepunkt
Det nedbrydes.
Massefylde
1,48 g / cm3 ved 20 ºC.
Opløselighed
Opløselig i vand: 29 g / 100 g vand.
pH
Dens opløsninger er sure med en pH mellem 2,5 og 5,5.
Kemiske egenskaber
I vandig opløsning natriumbisulfit NaHSO3 adskilles i dets ioner: natriumkationen Na+ og bisulfitanionen HSO3-.
Hvis natriumbisulfit udsættes for luft, mister den noget SOto og oxideres langsomt til Na-sulfattoSW4.
Hvis det opvarmes til nedbrydning, udsender det dampe af svovloxider og natriummonoxid..
Det er et reduktionsmiddel, som er det modsatte af oxidant. Og af denne grund kan det opføre sig som en antioxidant.
Den har en svag lugt af svovl. Det er ikke brandfarligt.
Risici
NaHSO-natriumbisulfit3 det er stærkt irriterende for hud og væv. Støv irriterer øjne, næse og hals. Ved indtagelse irriterer det maven. Store doser kan forårsage voldelig kolik, diarré, depression og død..
Det er ikke brændbart, men hvis det opvarmes, producerer det irriterende og giftige gasser.
Opnåelse
Det fremstilles ved at mætte en natriumcarbonatopløsning NatoCO3 med svovldioxid SOto og krystalliserer i opløsning.
Ansøgninger
I papir- og papirmasseindustrien
NaHSO3 Det bruges i fordøjelsen af træ, så det senere kan blive papir. Det tjener også som en pulpblegemiddel.
Det bruges også til at fjerne klor, når papirmasse er bleget med det..
I fødevareindustrien
Natriumbisulfit fungerer på grund af dets reducerende egenskab som en antioxidant.
Det bruges som konserveringsmiddel i et stort antal fødevarer og drikkevarer, herunder vin og øl, for at forhindre ødelæggelse og forbedre smag.
Det bruges til at blege fødevarer, såsom visse spiselige stivelser.
Det reducerer eller forhindrer madspild, tillader konditionering af dejen, der bruges i bagværk og tjener til at blødgøre majskerne under vådformaling, blandt andre anvendelser.
Ud over at kontrollere gæringen af vin og øl fungerer det som et antiseptisk middel i dets tilberedning, da det tjener som sterilisator og fungicid i tønder og kar..

I tørrede frugter findes den i koncentrationer over 100 ppm (ppm betyder "dele pr. Million"), i mange andre fødevarer findes den i koncentrationer mellem 10 og 100 ppm, såsom frosne og tørrede kartofler, syltede agurker, saucer og syltetøj.

Kontrovers over dets anvendelse i mad
Der har været en vis bekymring over både de umiddelbare og langvarige toksiske virkninger af natriumbisulfit i fødevarer. Der er forskellige meninger.
Der er rapporter om bivirkninger hos patienter med astma, som er en luftvejssygdom, efter indtagelse af mad med NaHSO3. Andre kilder indikerer, at bisulfitionen kan ødelægge vitamin B1 eller thiamin.

Imidlertid fandt visse forskere i 1985, at natriumbisulfit tjener til at beskytte mod stråling og kemiske agenser og hæmmer eller forhindrer transformation af celler til kræft. Lave doser er de bedste.
Denne beskyttende virkning er blevet forklaret på baggrund af dens reducerende eller antioxidantegenskaber, og at den på denne måde kunne angribe frie radikaler.
På den anden side Verdenssundhedsorganisationen eller WHO (for dets akronym på engelsk Verdens Sundhedsorganisation), anbefaler som et acceptabelt niveau af daglig indtagelse ca. 0,7 mg / kg af personens vægt.
Det betyder, at det anbefales ikke at overskride dette beløb..
United States Food and Drug Administration eller USFDA. US Food and Drug Administration), klassificeret natriumbisulfit som "generelt anerkendt som sikkert".
I landbrugsapplikationer
NaHSO anvendt i lave koncentrationer3 fungerer som en plantevækstregulator til forbedring af fotosyntese og fremme afgrødeudbytte.
Det er testet til dette formål i forskellige typer planter, såsom jordbær- og teplanter..

Det er den aktive ingrediens i mange pesticider og biocider.
I vandmiljøer kan det også fremskynde omdannelsen af visse herbicider til mindre giftige produkter ved at eliminere klor..
Ved opnåelse af jod
NaHSO3 er den reducerende forbindelse, der anvendes til at frigøre iod fra natriumiodid NaIO3. Dette er en af måderne at få jod fra kilder som nitro fra Chile eller noget saltvand.
Efter krystallisering af natriumnitratet fra den rå Chile-nitratopløsning forbliver en NaIO-opløsning3 som behandles med natriumbisulfit NaHSO3, genererer gratis jod.
2 NaIO3 + 5 NaHSO3 → 3 NaHSO4 + NatoSW4 + jegto
I møbel- og træindustrien
NaHSO3 Det er blevet testet for at modificere sojaproteiner og forbedre deres adhæsionsegenskaber med træ for at klæbe træstykker sammen for at forberede f.eks. Spånplader, pap eller papier-mache, krydsfiner osv. Alt dette til møbler eller brædder, blandt forskellige applikationer.

Dette gøres for at erstatte traditionelle formaldehydbaserede klæbemidler, fordi de både i deres fremstillingsproces og under deres brug har tendens til at frigive formaldehyd i atmosfæren, som er en giftig forbindelse..
Natriumbisulfit forbedrer faststofindholdet i sojaproteinklæbemidlet og nedsætter dets viskositet og forbedrer dets fluiditet, så det bedre trænger ind i træets porer og øger dets sammenhæng med det og mellem stykkerne..
NaHSO-modificeret sojaproteinlim3 har god vandmodstand og fremragende opbevaringsstabilitet på grund af antioxidantvirkningen af natriumbisulfit.
Dette bekræfter, at NaHSO-modificerede sojaproteinlim3 kan sammenlignes med formaldehydbaserede klæbemidler og kan bruges i møbel- og træindustrien, da de er mindre forurenende.
I forskellige applikationer
Det har flere anvendelser, generelt baseret på dets reducerende egenskaber (hvilket er det modsatte af oxidant). Her er nogle applikationer.
-I fotografering.
-Ved garvning af læder for at fjerne hår fra huder.
-Terapeutiske anvendelser: anti-infektiøs. Det bruges som en antioxidant i nogle øjendråber.
-Ved udvinding af naturgas ved hydraulisk frakturering.
-Ved farvning af fibre bruges det til fremstilling af varme eller kolde badekar til at opløse visse farvestoffer eller farvestoffer.
-Som reduktionsmiddel i vasketøj eller blegning til at blege uld, silke og vegetabilske fibre.
-I kemilaboratorier til fjernelse af permanganatpletter fra hud og tøj. I biokemilaboratorier som konserveringsmiddel for væsker eller opløsninger, der kan forringes over tid. Som et kemisk reagens.
-Til koagulation af gummilatex.
-I den kosmetiske industri som en antioxidant.
-Desinfektionsmiddel og blegemiddel.
-Ved behandling af spildevand for at eliminere det klor, der blev brugt i den sidste desinfektionsfase, og for at udlede det allerede behandlede vand til miljøet.

Referencer
- OS. National Library of Medicine. (2019). Natriumbisulfit. Gendannet fra pubchem.ncbi.nlm.nih.gov.
- Qi, G. et al. (2013). Adhæsion og fysisk-kemiske egenskaber af sojaprotein modificeret af natriumbisulfit. J Am Oil Chem Soc (2013) 90: 1917-1926. Gendannet fra aocs.onlinelibrary.wiley.com.
- Borek, C. et al. (1985). Natriumbisulfit beskytter mod radiogen og kemisk induceret transformation i hamsterembryo og mus C3H / 10T-1/2-celler. Toxicol Ind Health 1985Sep; 1 (1): 69-74. Gendannet fra journals.sagepub.com.
- Friedler, E. et al. (2015). En kontinuerlig aktiv overvågningsmetode til identifikation af krydsforbindelser mellem drikkevand og spildevandsfordelingssystemer. Environ Monit Assess (2015) 187: 131. Gendannet fra link.springer.com.
- Cotton, F. Albert og Wilkinson, Geoffrey. (1980). Avanceret uorganisk kemi. Fjerde udgave. John Wiley & Sons.
- Sunnyvale Cleanwater-program. (2019). Vandplan for forureningsbekæmpelsesanlæg. Gendannet fra sunnyvalecleanwater.com.
- Barros Santos, C. (2008). Tilsætningsstoffer i spansk mad og lovgivning, der regulerer deres godkendelse og anvendelse. Vision Books. Gendannet fra books.google.co.ve.



Endnu ingen kommentarer