
Kapillaritetsegenskaber og eksempel i vand
Det kapillaritet Det er en egenskab ved væsker, der gør det muligt for dem at bevæge sig gennem rørformede huller eller porøse overflader selv mod tyngdekraften. Til dette skal der være en balance og koordinering af to kræfter relateret til væskens molekyler: samhørighed og adhæsion; disse to har en fysisk refleksion kaldet overfladespænding.
Væsken skal være i stand til at våde rørets indvendige vægge eller porerne i det materiale, gennem hvilket det bevæger sig. Dette sker, når adhæsionskraften (væske-kapillærrørsvæg) er større end den intermolekylære samhørighedskraft. Derfor skaber væskemolekylerne stærkere interaktioner med materialets atomer (glas, papir osv.) End med hinanden..
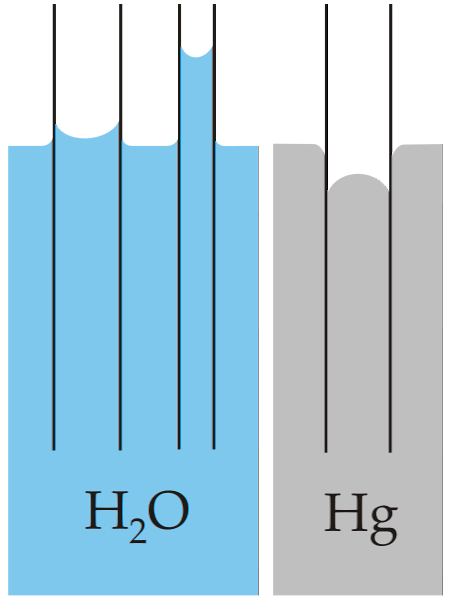
Det klassiske eksempel på kapillaritet illustreres ved at sammenligne denne egenskab med to meget forskellige væsker: vand og kviksølv..
På billedet ovenfor kan det ses, at vandet stiger op ad rørets vægge, hvilket betyder, at det har større vedhæftningskræfter; mens det med kviksølv sker det modsatte, fordi dets samhørighedskræfter af metallisk binding forhindrer det i at befugte glasset.
Af denne grund danner vand en konkav menisk og kviksølv en konveks (kuppelformet) menisk. Det skal også bemærkes, at jo mindre radius på røret eller den sektion, gennem hvilken væsken bevæger sig, jo større er højden eller den tilbagelagte afstand (sammenlign højderne på vandsøjlerne for begge rør).
Artikelindeks
- 1 Karakteristik af kapillaritet
- 1.1-Væskens overflade
- 1.2 -Højde
- 1.3-Overfladespænding
- 1.4 -Radius af kapillær eller pore, gennem hvilken væsken stiger
- 1,5 -Kontaktvinkel (θ)
- 2 Vandets kapillaritet
- 2.1 I planter
- 3 Referencer
Kapillaritetsegenskaber
-Flydende overflade
Væskens overflade, for eksempel vand, i en kapillær er konkav; menisken er konkav. Denne situation opstår, fordi den resulterende af de kræfter, der udøves på vandmolekylerne nær rørvæggen, er rettet mod dette.
I hver menisk er der en kontaktvinkel (θ), som er den vinkel, der dannes af kapillarrørets væg med en linje, der tangerer væskeoverfladen ved kontaktpunktet.
Adhæsions- og samhørighedskræfter
Hvis væskens vedhæftningskraft til kapillærvæggen hersker over den intermolekylære samhørighedskraft, er vinklen θ < 90º; el líquido moja la pared capilar y el agua asciende por el capilar, observándose el fenómeno conocido como capilaridad.
Når der placeres en dråbe vand på overfladen af et rent glas, spreder vandet sig over glasset, så θ = 0 og cos θ = 1.
Hvis den intermolekylære samhørighedskraft er fremherskende over væskekapillærvæggens vedhæftningskraft, for eksempel i kviksølv, vil menisken være konveks, og vinklen θ vil have en værdi> 90º; kviksølv fugter ikke kapillærvæggen og løber derfor ned ad den indvendige væg.
Når en dråbe kviksølv placeres på overfladen af et rent glas, opretholder dråben sin form og vinklen θ = 140º.
-Højde
Vandet stiger gennem kapillarrøret, indtil det når en højde (h), hvor vandsøjlens vægt kompenserer for den lodrette komponent af den intermolekylære samhørighedskraft.
Efterhånden som mere vand stiger, vil der komme et punkt, hvor tyngdekraften stopper dens opstigning, selv med overfladespænding, der virker til din fordel..
Når dette sker, kan molekylerne ikke fortsætte med at "klatre" de indre vægge, og alle fysiske kræfter udlignes. På den ene side er der kræfterne, der fremmer vandets stigning, og på den anden side dens egen vægt, der skubber det ned.
Jurins lov
Dette kan skrives matematisk som følger:
2 π rϒcosθ = ρgπrtoh
Hvor den venstre side af ligningen afhænger af overfladespændingen, hvis størrelse også er relateret til samhørighed eller intermolekylære kræfter; Cosθ repræsenterer kontaktvinklen og r radius af hullet, gennem hvilket væsken stiger.
Og på højre side af ligningen har vi højden h, tyngdekraften g og væskens tæthed; hvad ville være vandet?.
Løsning for h vi har
h = (2ϒcosθ / ρgr)
Denne formulering er kendt som Jurins lov, som definerer den højde, der nås med væskesøjlen, i kapillarrøret, når vægten af væskesøjlen afbalanceres med opstigningskraften ved kapillærvirkning..
-Overfladespænding
Vand er et dipolmolekyle på grund af iltatomets elektronegativitet og dets molekylære geometri. Dette får den del af vandmolekylet, hvor iltet er placeret, til at blive negativt ladet, mens den del af vandmolekylet, der indeholder de 2 hydrogenatomer, er positivt ladet..
Molekylerne i væsken interagerer takket være dette gennem flere hydrogenbindinger og holder dem sammen. De vandmolekyler, der er i vandet: luftgrænsefladen (overflade), udsættes dog for en nettotiltrækning af væskens sinusmolekyler, ikke kompenseret af den svage tiltrækning med luftmolekylerne.
Derfor udsættes vandmolekylerne ved grænsefladen for en attraktiv kraft, der har tendens til at fjerne vandmolekyler fra grænsefladen; det vil sige, at hydrogenbindingerne dannet med molekylerne i bunden trækker dem, der er på overfladen. Således søger overfladespænding at reducere overfladen af vandet: luftgrænsefladen..
Forholdet til h
Hvis vi ser på Jurins lovligning, finder vi ud af, at h er direkte proportional med ϒ; jo højere overfladespænding væsken er, jo større er højden, der kan stige gennem en kapillær eller pore af et materiale.
På denne måde kan det forventes, at for to væsker, A og B, med forskellige overfladespændinger, vil den med større overfladespænding stige til en højere højde..
Det kan konkluderes med hensyn til dette punkt, at en høj overfladespænding er den vigtigste egenskab, der definerer en væskes kapillære egenskab..
-Radius af kapillær eller pore, gennem hvilken væsken stiger
Observation af Jurins lov indikerer, at den højde, som en væske når i en kapillær eller pore, er omvendt proportional med den samme radius.
Derfor er jo mindre radius, jo større er højden, som væskesøjlen når ved kapillaritet. Dette kan ses direkte på billedet, hvor vand sammenlignes med kviksølv.
I et glasrør med en radius på 0,05 mm radius vil vandkolonnen pr. Kapillaritet nå en højde på 30 cm. I kapillarrør med en radius på 1 µm med et sugetryk på 1,5 x 103 hPa (som er lig med 1,5 atm) svarer til en beregning af vandsøjlens højde på 14 til 15 m.
Dette svarer meget til hvad der sker med de sugerør, der tænder på sig selv flere gange. Ved at nippe til væsken skabes en trykforskel, der får væsken til at stige til munden.
Den maksimale højde af søjlen, der nås ved kapillaritet, er teoretisk, da kapillærernes radius ikke kan reduceres ud over en bestemt grænse..
Poiseuilles lov
Dette fastslår, at strømmen af en reel væske er givet ved følgende udtryk:
Q = (πr4/ 8ηl) AP
Hvor Q er væskestrømmen, η er dens viskositet, l er rørets længde, og AP er trykforskellen.
Efterhånden som en kapillærradius aftager, skal den flydende søjles højde, der nås ved kapillærvirkning, øges på ubestemt tid. Poiseuille påpeger dog, at når radius aftager, falder væskestrømmen gennem denne kapillær også..
Viskositet, som er et mål for modstand mod strømmen af en reel væske, ville også reducere væskestrømmen yderligere..
-Kontaktvinkel (θ)
Jo større værdien af cosθ, jo større er vandkolonnens højde ved kapillaritet, som angivet i Jurins lov.
Hvis θ er lille og nærmer sig nul (0), er cosθ = 1, så værdien h vil være maksimal. Tværtimod, hvis θ er lig med 90º, er cosθ = 0 og værdien af h = 0.
Når værdien af θ er større end 90 °, hvilket er tilfældet med den konvekse menisk, stiger væsken ikke med kapillaritet, og dens tendens er at falde ned (som det sker med kviksølv).
Vandets kapillaritet
Vand har en overfladespændingsværdi på 72,75 N / m, relativt høj sammenlignet med værdierne for overfladespænding af følgende væsker:
-Aceton: 22,75 N / m
-Ethylalkohol: 22,75 N / m
-Hexan: 18,43 N / m
-Methanol: 22,61 N / m.
Derfor har vand en usædvanlig overfladespænding, som favoriserer udviklingen af kapillaritetsfænomenet, der er nødvendigt for planternes absorption af vand og næringsstoffer..
I planterne

Kapillaritet er en vigtig mekanisme til opstigning af saften gennem plantens xylem, men det er i sig selv ikke tilstrækkeligt til at få saften til træernes blade..
Sværing eller fordampning er en vigtig mekanisme i opstigningen af saft gennem plantens xylem. Bladene mister vand gennem fordampning, hvilket genererer et fald i mængden af vandmolekyler, hvilket forårsager en tiltrækning af de vandmolekyler, der findes i kapillærerne (xylem).
Vandmolekyler virker ikke uafhængigt af hinanden, men interagerer af Van der Waals kræfter, hvilket får dem til at stige sammenbundet gennem plantens kapillærer mod bladene.
Ud over disse mekanismer skal det bemærkes, at planter absorberer vand fra jorden ved osmose, og at et positivt tryk, der genereres i roden, driver starten på vandstigningen gennem plantens kapillarrør..
Referencer
- García Franco A. (2010). Overfladiske fænomener. Gendannet fra: sc.ehu.es
- Overfladefænomener: overfladespænding og kapillaritet. [PDF]. Gendannet fra: ugr.es
- Wikipedia. (2018). Kapillaritet. Gendannet fra: es.wikipedia.org
- Risvhan T. (s.f.) Kapillaritet i planter. Gendannet fra: academia.edu
- Helmenstine, Anne Marie, Ph.D. (22. december 2018). Kapillær handling: Definition og eksempler. Gendannet fra: thoughtco.com
- Ellen Ellis M. (2018). Kapillær handling af vand: definition og eksempler. Undersøgelse. Gendannet fra: study.com
- ScienceStruck-personale. (16. juli 2017). Eksempler, der forklarer begrebet og betydningen af kapillær handling. Gendannet fra: sciencestruck.com


Endnu ingen kommentarer