
Formel perchlorsyre, egenskaber og anvendelser

Det perchlorsyre Det er en meget stærk mineralsyre, der normalt findes som en farveløs og lugtfri vandig opløsning, ætsende for metaller og stoffer. Det er et stærkt oxidationsmiddel, når det er varmt, men dets vandige opløsninger (op til ca. 70 vægt%) ved stuetemperatur er generelt sikre og viser kun stærke syreegenskaber og ingen oxidationsegenskaber..
Perchlorsyre og salte deraf (især ammoniumperchlorat [NH4ClO4, CAS: 7790-98-9], natriumperchlorat [NaClO4, 7601-89-0] og kaliumperchlorat [KClO4, 7778-74-7]), find mange applikationer på grund af deres stærke oxidationsevne.

Dens produktion er steget på grund af dets anvendelse som udgangsmateriale til produktion af rent ammoniumperchlorat, en grundlæggende ingrediens i sprængstoffer og faste drivmidler til raketter og missiler..

Perchlorsyre anvendes også i begrænset omfang som et reagens til analytiske formål. Dens lukkede beholderbeholdere kan briste voldsomt under langvarig udsættelse for varme..
Formler: Perchlorsyre: HClO4
CAS: 7601-90-3
2D struktur
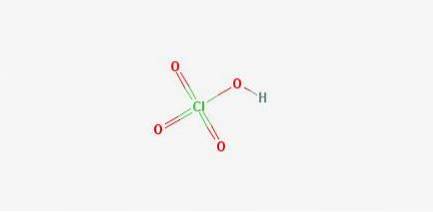
3D-struktur
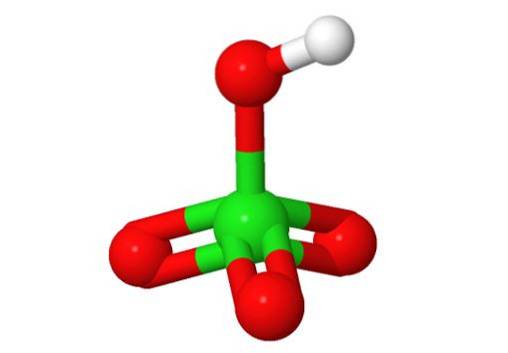
Perchlorsyre-egenskaber
Fysiske og kemiske egenskaber
- Udseende: farveløs væske
- Lugt: lugtfri
- Molekylvægt: 100.454 g / mol
- Kogepunkt: 19 ° C
- Smeltepunkt: -112 ° C
- Massefylde: 1.768 g / cm3
- Opløselighed i vand: blandbar
- Surhed (pKa): -15,2 (± 2,0)
Perchlorsyre hører til gruppen af stærke oxiderende syrer.
Brændbarhed
-Stærke oxiderende syrer er generelt ikke brandfarlige, men kan fremskynde forbrændingen af andre materialer ved at tilvejebringe ilt (fungerer som oxidationsmidler).
-Saltsyreopløsninger kan eksplodere fra varme eller forurening.
-Når de opvarmes over 160 ° C eller er involveret i en brand, kan de nedbrydes eksplosivt.
-De kan reagere eksplosivt med kulbrinter (brændstoffer). Det kan antænde brændstoffer (træ, papir, olie, tøj osv.).
-Beholdere kan eksplodere, når de opvarmes.
-Afstrømning kan skabe brand eller eksplosionsfare.
Reaktivitet
-Stærke oxiderende syrer er generelt opløselige i vand med frigivelse af hydrogenioner. De resulterende opløsninger har en pH-værdi på 1 eller tæt på 1.
-Materialer i denne gruppe reagerer med kemiske baser (f.eks. Uorganiske aminer og hydroxider) til dannelse af salte. Disse neutraliseringsreaktioner opstår, når basen accepterer brintioner, som syren donerer.
-Neutraliseringer kan generere farligt store mængder varme i små rum.
-Tilsætningen af vand til syrer genererer ofte nok varme i blandingens lille område til at koge den del af vandet eksplosivt, hvilket kan føre til meget farlige syresprøjt..
-Disse materialer har en betydelig kapacitet som oxidationsmidler, men denne kapacitet varierer fra den ene til den anden..
-De kan reagere med aktive metaller (såsom jern og aluminium) og også med mange mindre aktive metaller for at opløse metallet og frigive brint og / eller giftige gasser.
-Dens reaktioner med cyanidsalte og dets forbindelser frigiver gasformigt hydrogencyanid..
-Brandfarlige og / eller giftige gasser dannes også ved deres reaktioner med dithiocarbamater, isocyanater, mercaptaner, nitrider, nitriler, sulfider og svage eller stærke reduktionsmidler..
-Yderligere gasgenererende reaktioner forekommer med sulfitter, nitritter, thiosulfater (for at give H2S og SO3), dithionitter (SO2) og endda carbonater: Kuldioxidgassen i sidstnævnte er ikke giftig, men varmen og sprøjten fra reaktionen kan blive forstyrret.
-Perchlorsyreopløsninger er stærke oxiderende syreopløsninger.
-De kan reagere kraftigt eller detonere, når de blandes med oxiderbare materialer (alkoholer, aminer, boraner, dicyanogen, hydraziner, carbonhydrider, brint, nitroalkaner, pulveriserede metaller, silaner og thioler, blandt andre).
-Perchlorsyre antændes ved kontakt med sulfinylchlorid.
Toksicitet
-Stærke oxiderende syrer er ætsende for stoffer. Syredampe irriterer følsomt væv (såsom øjne og åndedrætsorganer) alvorligt.
-Indånding, indtagelse eller kontakt (af hud, øjne osv.) Med perchlorsyreopløsninger eller dets dampe kan forårsage alvorlig personskade, forbrændinger eller død..
-Når de kommer i kontakt med ild, kan de producere irriterende, ætsende og / eller giftige gasser..
-Afstrømning fra brandkontrol eller fortyndingsvand kan forårsage forurening.
Ansøgninger
-Perchlorsyre anvendes inden for videnskabelig forskning og udvikling og til fremstilling af kemikalier og elektrisk, elektronisk og optisk udstyr.
-Det bruges som en forløber til produktion af rent ammoniumperchlorat, en grundlæggende ingrediens i sprængstoffer og faste drivmidler til raketter og missiler..
-Perchlorsyre anvendelser i hjemmet inkluderer toilet-, metal- og afløbsrensere, rustfjernere, i batterier og som en primer til falske negle..
-Industrielle anvendelser inkluderer: metalraffinering, VVS, blegning, ætsning, galvanisering, fotografering, desinfektion, ammunition, gødningsproduktion, metalrensning og rustfjerning.
-Perchlorsyre anvendes også i begrænset omfang som et reagens til analytiske formål..
Kliniske effekter
Syrer forårsager koagulationsnekrose. Hydrogenioner udtørrer epitelceller, der forårsager ødem, erytem, udstødning af væv og nekrose med dannelse af sår og liggesår..
Ved eksponering for disse syrer via den gastrointestinale vej kan patienter udvikle grad II forbrændinger (overfladiske blærer, erosioner og sårdannelser), der er i risiko for efterfølgende dannelse af strengdannelse, især mavevejen og spiserøret..
Der kan også udvikles dybe forbrændinger og nekrose i mave-tarmslimhinden. Komplikationer inkluderer ofte perforering (esophageal, gastrisk, sjældent duodenal), fisteldannelse (tracheoesophageal, aortoesophageal) og gastrointestinal blødning..
Eksponering ved indånding kan forårsage dyspnø, pleuritisk smerte i brystet, hoste og bronkospasme, øvre luftvejsødem og forbrændinger. Øvre luftvejsødem er almindeligt og ofte livstruende.
Eksponering af øjet kan forårsage alvorlig konjunktival irritation og kemose, epitheliale hornhindedefekter, limbisk iskæmi, permanent synstab og i alvorlige tilfælde af perforering..
Mild eksponering af huden kan forårsage irritation og delvis forbrænding af tykkelsen. Længere eller høj koncentration kan medføre forbrændinger i fuld tykkelse.
Komplikationer kan omfatte cellulitis, sepsis, kontrakturer, osteomyelitis og systemisk toksicitet.
Sikkerhed og risici
Faresætninger fra det globalt harmoniserede system for klassificering og mærkning af kemikalier (GHS)
Det globalt harmoniserede system til klassificering og mærkning af kemikalier (GHS) er et internationalt aftalt system, der er oprettet af FN og designet til at erstatte de forskellige klassificerings- og mærkningsstandarder, der anvendes i forskellige lande ved hjælp af ensartede kriterier globalt..
Risikoklasserne (og deres tilsvarende GHS-kapitel), klassificerings- og mærkningsstandarder og anbefalinger for perchlorsyre er som følger (European Chemicals Agency, 2017; FN, 2015; PubChem, 2017):
GHS-faresætninger
H271: Kan forårsage brand eller eksplosion; Stærkt oxidationsmiddel [Fare Oxiderende væsker; Oxiderende faste stoffer - Kategori 1] (PubChem, 2017).
H290: Kan være ætsende for metaller [Advarsel ætsende for metaller - kategori 1] (PubChem, 2017).
H302: Farlig ved indtagelse [Advarsel Akut toksicitet, oral - kategori 4] (PubChem, 2017).
H314: Forårsager svære forbrændinger af huden og øjenskader [Fare Hudætsning / -irritation - Kategori 1A, B, C] (PubChem, 2017).
H318: Forårsager alvorlig øjenskade [Fare Alvorlig øjenskade / øjenirritation - Kategori 1] (PubChem, 2017).
H371: Kan forårsage organskader [Advarselsspecifik målorgantoksicitet, enkelt eksponering - Kategori 2] (PubChem, 2017).
Forsigtig Instruktionskoder
P210, P220, P221, P234, P260, P264, P270, P280, P283, P301 + P312, P301 + P330 + P331, P303 + P361 + P353, P304 + P340, P305 + P351 + P338, P306 + P360, P30 P311, P310, P321, P330, P363, P370 + P378, P371 + P380 + P375, P390, P404, P405 og P501 (PubChem, 2017).





Referencer
- Det Europæiske Kemikalieagentur (ECHA). (2016). Perchlorsyre. Kort profil. Hentet den 8. februar 2017 fra: echa.europa.eu.
- JSmol (2017) Perchlorsyre. [billede] Gendannet fra: chemapps.stolaf.edu.
- NASA (2008) Ares-1 lancering 02-2008 [billede] Gendannet fra: commons.wikimedia.org.
- National Center for Biotechnology Information. PubChem Compound Database. (2017). Perchlorsyre - PubChem-struktur. [billede] Bethesda, MD, EU: National Library of Medicine. Gendannet fra: pubchem.ncbi.nlm.nih.gov.
- Oelen, W. (2011) Perchlorsyre 60 procent [billede] Gendannet fra: en.wikipedia.org.
- Wikipedia. (2017). Perchlorsyre. Hentet 8. februar 2017 fra: es.wikipedia.org.
- Wikipedia. (2017). Perchlorsyre. Hentet 8. februar 2017 fra: es.wikipedia.org.


Endnu ingen kommentarer