
Glykosidiske bindingsegenskaber, typer og nomenklatur
Det glykosidbindinger De er de kovalente bindinger, der opstår mellem sukker (kulhydrater) og andre molekyler, som kan være andre monosaccharider eller andre molekyler af forskellig art. Disse forbindelser muliggør eksistensen af flere grundlæggende komponenter for livet, ikke kun i dannelsen af reservebrændstoffer og strukturelle elementer, men også af informationsbærende molekyler, der er vigtige for cellulær kommunikation..
Dannelsen af polysaccharider afhænger grundlæggende af etableringen af glykosidbindinger mellem de frie alkohol- eller hydroxylgrupper i de enkelte monosaccharidenheder..
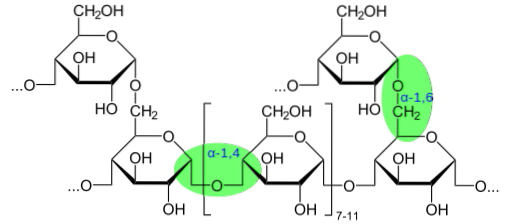
Imidlertid indeholder nogle komplekse polysaccharider modificerede sukkerarter, der er bundet til små molekyler eller grupper såsom amino, sulfat og acetyl gennem glucosidbindinger, og som ikke nødvendigvis involverer frigivelse af et vandmolekyle ved en kondensationsreaktion. Disse modifikationer er meget almindelige i glycaner til stede i den ekstracellulære matrix eller glycocalyx..
Glykosidiske bindinger forekommer i flere cellulære sammenhænge, herunder foreningen af den polære hovedgruppe af nogle sfingolipider, essentielle bestanddele i cellemembranerne i mange organismer og dannelsen af glycoproteiner og proteoglycaner..
Vigtige polysaccharider, såsom cellulose, chitin, agar, glykogen og stivelse, ville ikke være mulige uden glykosidiske bindinger. Ligeledes er proteinglycosylering, som forekommer i det endoplasmatiske retikulum og i Golgi-komplekset, af største betydning for aktiviteten af mange proteiner..
Talrige oligo- og polysaccharider fungerer som glukosereservoirer, som strukturelle komponenter eller som klæbemidler til cellefastgørelse i væv..
Forholdet mellem glycosidbindinger i oligosaccharider er analog med peptidbindinger i polypeptider og phosphodiesterbindinger i polynukleotider med den forskel, at der er større mangfoldighed i glycosidbindinger.
Artikelindeks
- 1 Funktioner
- 1.1 Dannelse af den glykosidiske binding
- 1.2 Hydrolyse af den glykosidiske binding
- 1.3 Mangfoldighed
- 2 slags
- 2.1 O-glukosidbindinger
- 2.2 N-glukosidbindinger
- 2.3 Andre typer glykosidbindinger
- 3 Nomenklatur
- 4 Referencer
Egenskaber
Glykosidbindinger er meget mere varierede end deres analoger i proteiner og nukleinsyrer, da i princippet kan to sukkermolekyler forbinde hinanden på mange måder, fordi de har flere -OH-grupper, der kan deltage i dannelsen af linket.
Yderligere giver isomererne af monosaccharider, det vil sige en af de to retninger, som hydroxylgruppen kan have i den cykliske struktur i forhold til det anomere carbon, et yderligere niveau af diversitet..
Isomerer har forskellige tredimensionelle strukturer såvel som forskellige biologiske aktiviteter. Cellulose og glykogen består af gentagne D-glukosenheder, men adskiller sig i typen af glykosidisk binding (α1-4 for glykogen og β1-4 for cellulose) og har derfor forskellige egenskaber og funktioner..
Ligesom polypeptider har en polaritet med en N- og en C-ende, og polynukleotider har 5 'og 3' ender, har oligo- eller polysaccharider en polaritet defineret af de reducerende og ikke-reducerende ender.
Den reducerende ende har et frit anomert center, der ikke danner en glykosidisk binding med et andet molekyle, hvorved den kemiske reaktivitet af aldehydet bibeholdes.
Den glykosidiske binding er den mest fleksible region af en oligo- eller polysacchariddel, da den strukturelle sadelkonformation af individuelle monosaccharider er relativt stiv..
Dannelse af den glykosidiske binding
Den glykosidiske binding kan forbinde to monosaccharidmolekyler gennem det anomere carbon i den ene og hydroxylgruppen i den anden. Det vil sige, hemiacetalgruppen i et sukker reagerer med en andens alkoholgruppe for at danne en acetal.
Generelt sker dannelsen af disse bindinger ved kondensationsreaktioner, hvor et vandmolekyle frigøres med hver binding, der dannes..
Imidlertid efterlader ilt i nogle reaktioner ikke sukkermolekylet som vand, men som en del af diphosphatgruppen i et uridindiphosphatnukleotid..
Reaktionerne, der giver anledning til de glykosidiske bindinger, katalyseres af en klasse af enzymer kendt som glycosyltransferaser. De dannes mellem et kovalent modificeret sukker ved tilsætning af en phosphatgruppe eller et nukleotid (f.eks. Glukose 6-phosphat, UDP-galactose), der binder til den voksende polymerkæde.
Hydrolyse af den glykosidiske binding
Glykosidbindinger kan let hydrolyseres i svagt sure omgivelser, men de er ret resistente over for alkaliske miljøer..
Den enzymatiske hydrolyse af de glykosidiske bindinger medieres af enzymer kendt som glycosidaser. Mange pattedyr har ikke disse enzymer til nedbrydning af cellulose, så de er ikke i stand til at udvinde energi fra dette polysaccharid på trods af at de er en væsentlig kilde til fiber.
Drøvtyggere som køer har for eksempel bakterier forbundet med deres tarme, der producerer enzymer, der er i stand til at nedbryde den cellulose, de indtager, hvilket gør dem i stand til at udnytte den energi, der er bevaret i plantevæv..
Enzymet lysozym, produceret i tårerne i øjet og af nogle bakterievira, er i stand til at ødelægge bakterier takket være dets hydrolytiske aktivitet, der bryder den glykosidiske binding mellem N-acetylglucosamin og N-acetylmuraminsyre i bakterievæggen..
Mangfoldighed
Oligosaccharider, polysaccharider eller glycaner er meget forskellige molekyler, og dette skyldes de mange måder, hvorpå monosaccharider kan binde sig sammen for at danne højere ordensstrukturer.
Denne mangfoldighed er baseret på det faktum, som nævnt ovenfor, at sukkerarter har hydroxylgrupper, der tillader forskellige bindingsregioner, og at der kan forekomme bindinger mellem de to mulige stereoisomerer med hensyn til det anomere kulstof i sukkeret (α eller β)..
Glykosidbindinger kan dannes mellem et sukker og en hvilken som helst hydroxyforbindelse, såsom alkoholer eller aminosyrer.
Derudover kan et monosaccharid danne to glycosidbindinger, så det kan tjene som et forgreningspunkt, der introducerer potentiel kompleksitet i strukturen af glycaner eller polysaccharider i celler..
Typer
For så vidt angår typer glykosidbindinger, kan to kategorier differentieres: de glykosidiske bindinger mellem monosaccharider, der udgør oligo- og polysaccharider, og de glycosidiske bindinger, der forekommer i glycoproteiner eller glycolipider, som er proteiner eller lipider med dele af kulhydrater.
O-glukosidbindinger
O-glykosidbindinger forekommer mellem monosaccharider, de dannes ved reaktionen mellem hydroxylgruppen i et sukkermolekyle og det anomere carbon i et andet.
Disaccharider er en af de mest almindelige oligosaccharider. Polysaccharider har mere end 20 monosaccharidenheder bundet sammen lineært og har undertiden flere grene..
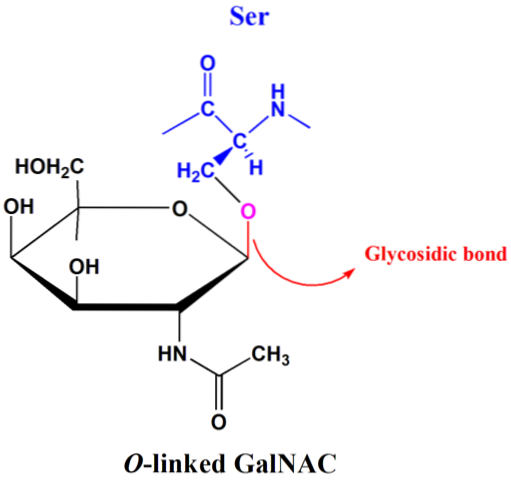
I disaccharider som maltose, lactose og saccharose er den mest almindelige glykosidiske binding den O-glukosidiske type. Disse bindinger kan forekomme mellem kulstofferne og -OH af a- eller β-isomere former..
Dannelsen af de glucosidiske bindinger i oligo- og polysaccharider vil afhænge af den stereokemiske natur af de sukkerarter, der er forbundet, såvel som af deres antal carbonatomer. Generelt forekommer lineære bindinger mellem kulstof 1 og 4 eller 1 og 6 for sukker med 6 carbonatomer.
Der er to hovedtyper af O-glycosider, der afhængigt af nomenklaturen er defineret som α og β eller 1,2-cis og 1.2-trans-glykosider.
Rester 1,2-cis glycosylerede, a-glycosider for D-glucose, D-galactose, L-fucose, D-xylose eller p-glycosider for D-mannose, L-arabinose; samt 1,2-trans (β-glycosider til D-glucose, D-galactose og α-glycosider til D-mannose osv.), er af stor betydning for mange naturlige komponenter.
O-glycosylering
En af de mest almindelige ændringer efter translation er glycosylering, som består af tilsætningen af en kulhydratdel til et voksende peptid eller protein. Muciner, sekretoriske proteiner, kan indeholde store mængder oligosaccharidkæder bundet af O-glucosidbindinger..
O-glycosyleringsprocessen forekommer i Golgi-komplekset af eukaryoter og består af binding af proteiner til kulhydratdelen gennem en glycosidisk binding mellem -OH-gruppen i en aminosyrerest af serin eller threonin og det anomere carbon af sukker..
Dannelsen af disse bindinger mellem kulhydrater og hydroxyprolin og hydroxylysinrester og med den phenoliske gruppe af tyrosinrester er også blevet observeret..
N-glykosidbindinger
N-glykosidbindinger er de mest almindelige blandt glykosylerede proteiner. N-glykosylering forekommer hovedsageligt i det endoplasmatiske retikulum af eukaryoter med efterfølgende ændringer, der kan forekomme i Golgi-komplekset.
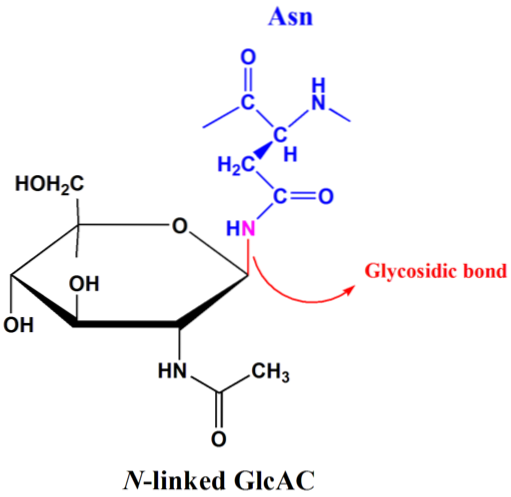
N-glycosylering afhænger af tilstedeværelsen af konsensus-sekvensen Asn-Xxx-Ser / Thr. Den glykosidiske binding opstår mellem amidnitrogen i sidekæden af asparaginresterne og det anomere carbon i sukkeret, der binder til peptidkæden..
Dannelsen af disse bindinger under glycosylering afhænger af et enzym kendt som oligosacaryltransferase, som overfører oligosacchariderne fra et dolicholphosphat til amidnitrogenet i asparaginresterne..
Andre typer glykosidbindinger
S-glukosidbindinger
De forekommer også mellem proteiner og kulhydrater, de er blevet observeret mellem peptider med N-terminale cysteiner og oligosaccharider. Peptider med denne type binding blev oprindeligt isoleret fra proteiner i human urin og erythrocytter bundet til glucoseoligosaccharider..
C-glukosidbindinger
De blev observeret for første gang som en post-translationel modifikation (glycosylering) i en tryptophanrest i RNase 2 til stede i human urin og i RNase 2 af erythrocytter. En mannose binder til carbonet i position 2 i amolens indolkerne gennem en C-glucosidbinding.
Nomenklatur
Udtrykket glycosid bruges til at beskrive ethvert sukker, hvis anomere gruppe er erstattet med en gruppe -OR (O-glycosider), -SR (thioglycosider), -SeR (selenoglycosider), -NR (N-glycosider eller glucosaminer) eller endda -CR (C-glucosider).
De kan navngives på tre forskellige måder:
(1) erstatning af terminalen "-o" for navnet på den tilsvarende cykliske form af monosaccharidet med "-ido" og inden navnet, som et andet ord, er skrevet på den substituerende R-gruppe.
(2) ved anvendelse af udtrykket "glycosyloxy" som et præfiks for monosaccharidnavnet.
(3) ved hjælp af udtrykket ELLER-glycosyl, N-glycosyl, S-glycosyl eller C-glycosyl som et præfiks for navnet på hydroxyforbindelsen.
Referencer
- Bertozzi, C. R. og Rabuka, D. (2009). Strukturel basis for glykamangfoldighed. I A. Varki, R. Cummings og J. Esko (red.), Essentials of Glycobiology (2. udgave). New York: Cold Spring Harbour Laboratory Press. Hentet fra www.ncbi.nlm.nih.gov
- Biermann, C. (1988). Hydrolyse og andre spaltninger af glykosidiske bindinger i polysaccharider. Fremskridt inden for kulhydratkemi og biokemi, 46, 251-261.
- Demchenko, A. V. (2008). Håndbog om kemisk glykosylering: Fremskridt i stereoselektivitet og terapeutisk relevans. Wiley-VCH.
- Lodish, H., Berk, A., Kaiser, C. A., Krieger, M., Bretscher, A., Ploegh, H.,… Martin, K. (2003). Molekylær cellebiologi (5. udgave). Freeman, W. H. & Company.
- Nelson, D. L. og Cox, M. M. (2009). Lehninger Principper for biokemi. Omega-udgaver (5. udgave).
- Nomenklatur for kulhydrater (anbefalinger 1996). (nitten seksoghalvfems). Hentet fra www.qmul.ac.uk
- Soderberg, T. (2010). Organisk kemi med biologisk vægt, bind I. Kemi Fakultet (Bind 1). Minnesota: University of Minnesota Morris Digital Well. Hentet fra www.digitalcommons.morris.umn.edu
- Taylor, C. M. (1998). Glykopeptider og glykoproteiner: Fokus på glykosidisk binding. Tetrahedron, 54, 11317-11362.



Endnu ingen kommentarer