
Laccase karakteristika, struktur, funktioner
Det husene, s-Diphenol: dioxygenoxidoreduktaser eller benzeniol-oxygenoxidoreduktaser, er enzymer, der hører til gruppen af oxidaseenzymer kaldet "blå kobberoxidaser".
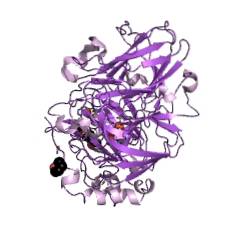
De findes i højere planter, i nogle insekter, i bakterier og i næsten alle de svampe, der er blevet undersøgt; dens karakteristiske blå farve er produktet af fire kobberatomer bundet til molekylet på dets katalytiske sted.
Disse enzymer blev beskrevet af Yoshida og samarbejdspartnere i år 1883, da man studerede træets harpiks Rhus vernicifera eller japansk "lakktræ", hvor det blev bestemt, at dets hovedfunktion var at katalysere polymerisations- og depolymerisationsreaktioner af forbindelser..
Langt senere blev det opdaget, at disse proteiner med enzymatisk aktivitet i svampe har specifikke funktioner i mekanismerne til fjernelse af giftige phenoler fra det miljø, hvor de vokser, mens de i planter er involveret i syntetiske processer såsom lignifikation.
Videnskabelige fremskridt med hensyn til undersøgelsen af disse enzymer tillod deres anvendelse på industrielt niveau, hvor deres katalytiske kapacitet er blevet brugt, især i sammenhænge med bioremediering, tekstiler, til fjernelse af farvestoffer påført tekstiler, i papirindustrien, blandt andre.
Hovedårsagerne til, at laccaser er så interessante fra et industrielt synspunkt, har at gøre med det faktum, at deres oxidationsreaktioner simpelthen involverer reduktion af molekylært ilt og produktion af vand som et sekundært element..
Artikelindeks
- 1 Funktioner
- 1.1 Distribution
- 1.2 Katalyse
- 2 Struktur
- 2.1 Isoenzymer
- 3 funktioner
- 3.1 I planter
- 3.2 I svampe
- 3.3 I industrien
- 4 Referencer
Egenskaber
Laccaseenzymer kan udskilles eller findes i det intracellulære område, men det afhænger af organismen, der undersøges. På trods af dette er de fleste af de analyserede enzymer (med undtagelse af nogle proteiner fra visse svampe og insekter) ekstracellulære proteiner..
Fordeling
Disse enzymer, som beskrevet ovenfor, findes overvejende i svampe, højere planter, bakterier og nogle arter af insekter..
Blandt de planter, hvor dets eksistens er bevist, er blandt andet æbletræer, asparges, kartofler, pærer, mango, ferskner, fyrretræer, blommer. Laccase-udtrykkende insekter hører hovedsageligt til slægterne Bombyx, Calliphora, Diploptera, Drosophila, Musca, Papilio, Rhodnius, og andre.
Svampe er de organismer, hvorfra det største antal og forskellige laccaser er blevet isoleret og undersøgt, og disse enzymer er til stede i både ascomyceter og deuteromyceter og basidiomyceter..
Katalyse
Reaktionen katalyseret af laccaser består af den monoelektroniske oxidation af et substratmolekyle, der kan høre til gruppen af phenoler, aromatiske forbindelser eller alifatiske aminer, til dets tilsvarende reaktive gruppe.
Resultatet af den katalytiske reaktion er reduktionen af et iltmolekyle til to vandmolekyler, og oxidationen på samme tid af fire substratmolekyler til dannelse af fire reaktive frie radikaler..
Mellemliggende frie radikaler kan binde og danne dimerer, oligomerer eller polymerer, hvorfor det siges, at laccaser katalyserer polymerisations- og "depolymerisations" -reaktioner..
Struktur
Laccaser er glycoproteiner, det vil sige de er proteiner, der har oligosaccharidrester kovalent bundet til polypeptidkæden, og disse repræsenterer mellem 10 og 50% af den samlede vægt af molekylet (i planteenzymer kan procentdelen være lidt højere).
Kulhydratdelen af denne type protein indeholder monosaccharider, såsom glucose, mannose, galactose, fucose, arabinose og nogle hexosaminer, og glycosylering menes at spille vigtige roller i sekretion, proteolytisk følsomhed, aktivitet, kobberretention og den termiske stabilitet af proteinet.
Generelt findes disse enzymer i naturen som monomerer eller homodimerer, og molekylvægten af hver monomer kan variere mellem 60 og 100 kDa.
Det katalytiske centrum af laccaser består af fire kobberatomer (Cu), som giver molekylet generelt en blå farve på grund af den elektroniske absorption, der finder sted i kobber-kobber (Cu-Cu) bindinger..
Plantelakser har isoelektriske punkter med værdier tæt på 9 (ganske basale), mens svampenzymer er mellem isoelektriske punkter på 3 og 7 (så de er enzymer, der fungerer under sure forhold).
Isoenzymer
Mange laccase-producerende svampe har også laccase-isoformer, som kodes af det samme gen eller af forskellige gener. Disse isoenzymer adskiller sig hovedsageligt fra hinanden med hensyn til deres stabilitet, deres optimale pH og temperatur til at katalysere og med hensyn til deres affinitet for forskellige typer substrater..
Under visse betingelser kan disse isoenzymer have forskellige fysiologiske funktioner, men det afhænger af arten eller tilstanden, hvori den lever..
Funktioner
Nogle forskere har vist, at laccaser er involveret i "sklerotisering" af neglebånd i insekter og samling af sporer, der er resistente over for ultraviolet lys i mikroorganismer i slægten. Bacillus.
I planterne
I planteorganismer deltager laccaser i dannelsen af cellevæggen i processerne med lignifikation og "delignifikation" (tab eller desintegration af lignin); og derudover har de været relateret til afgiftning af væv gennem oxidation af svampedræbende phenoler eller deaktivering af phytoalexiner.
I svampe
Lakser deltager betydeligt i denne gruppe af organismer i en række cellulære og fysiologiske processer. Blandt dem kan vi nævne beskyttelsen af tannins patogene svampe og de vegetabilske "phytoalexiner"; så det kan siges, at for enzymer er disse enzymer virulensfaktorer.
Laccaser har også funktioner i morfogenesen og differentieringen af basidiomycetes modstands- og sporestrukturer såvel som ved biologisk nedbrydning af lignin i svampe, der nedbryder væv fra træagtige plantearter..
Samtidig deltager laccaser i dannelsen af pigmenter i mycelier og frugtlegemer i mange svampe og bidrager til celle-celleadhæsionsprocesser, i dannelsen af den polyfenoliske "lim", der binder hyfer og i unddragelse af immunforsvaret. værtssystem inficeret med patogene svampe.
I branchen
Disse bestemte enzymer anvendes industrielt til forskellige formål, men de mest fremragende svarer til tekstil- og papirindustrien og til bioremediering og dekontaminering af spildevand produceret ved andre industrielle processer..
Specifikt anvendes disse enzymer ofte til oxidation af phenoler og deres derivater til stede i vand kontamineret med industriaffald, hvis katalyseprodukter er uopløselige (polymeriserede) og bundfald, hvilket gør dem let adskillelige..
I fødevareindustrien har de også en vis betydning, da fjernelse af phenolforbindelser er nødvendig for stabilisering af drikkevarer såsom vin, øl og naturlig juice..
De bruges i kosmetikindustrien, i kemisk syntese af mange forbindelser, i jordbioremediering og i nanobioteknologi.
De mest anvendte er laccase fra svampe, men for nylig er det blevet bestemt, at bakteriel laccase har mere fremtrædende karakteristika set fra et industrielt synspunkt; De er i stand til at arbejde med et større udvalg af substrater og ved meget bredere temperatur- og pH-intervaller, ud over at være meget mere stabile mod hæmmende stoffer.
Referencer
- Claus, H. (2004). Laccaser: struktur, reaktioner, fordeling. Micron, 35, 93-96.
- Couto, S. R., Luis, J., & Herrera, T. (2006). Industrielle og bioteknologiske anvendelser af laccases: En gennemgang. Bioteknologiske fremskridt, 24, 500-513.
- Madhavi, V., & Lele, S. S. (2009). Laccase: egenskaber og applikationer. Bioressourcer, 4(4), 1694-1717.
- Riva, S., Molecolare, R., & Bianco, V. M. (2006). Laccaser: blå enzymer til grøn kemi. Tendenser inden for bioteknologi, 24(5), 219-226.
- Singh, P., Bindi, C., & Arunika, G. (2017). Bakteriel laccase: nylig opdatering af produktion, ejendomme og industrielle applikationer. Biotech, 7(323), 1-20.

Endnu ingen kommentarer