
Kaliumthiocyanat (KSCN) struktur, egenskaber, anvendelser

Det kaliumthiocyanat Det er en uorganisk forbindelse dannet af grundstofferne kalium (K), svovl (S), kulstof (C) og nitrogen (N). Dens kemiske formel er KSCN. Det er et farveløst eller hvidt fast stof, der er meget opløseligt i vand. Den består af en kalium K-ion+ og en SCN-thiocyanation-. KSCN findes rigeligt i spyt.
Kaliumthiocyanat anvendes som laboratoriereagens til forskellige typer kemisk analyse. Det bruges også i blæk og maling.

KSCN er blevet brugt til at opløse dentingelatine (materiale under tandemaljen) inden påføring af tandreparationsmateriale eller harpiks. Det bruges også til forskning i vacciner, da det tillader ekstraktion af visse biokemiske grundstoffer fra bakterier.
Det bruges i form af en opløsning, hvor metaller opløses under poleringsprocessen ved hjælp af elektricitet eller elektropolering. Det er også blevet brugt til at opnå falsk blod til film og skuespil.
Det misbruges undertiden for at øge mælkens stabilitet, når den ikke opbevares nedkølet. Men det har den ulempe, at det forårsager hypothyroidisme, en sygdom, hvor skjoldbruskkirtlen ikke fungerer..
Artikelindeks
- 1 Struktur
- 2 Nomenklatur
- 3 egenskaber
- 3.1 Fysisk tilstand
- 3.2 Molekylvægt
- 3.3 Smeltepunkt
- 3.4 Nedbrydningstemperatur
- 3.5 Densitet
- 3.6 Opløselighed
- 3,7 pH
- 3.8 Andre egenskaber
- 4 Opnåelse
- 4.1 Tilstedeværelse i naturen
- 5 anvendelser
- 5.1 I forskellige applikationer
- 5.2 I tandlægeanvendelser
- 5.3 I medicinske videnskabslaboratorier
- 5.4 I metalindustrien
- 5.5 På filmsættet eller i teatret
- 5.6 Misbrug af kaliumthiocyanat
- 6 risici
- 7 Referencer
Struktur
Kaliumthiocyanat består af en kalium K-kation+ og en NCS-thiocyanatanion-. Sidstnævnte er dannet af et nitrogen (N) bundet til et carbon (C) gennem en tredobbelt binding og et svovl (S) bundet til carbon gennem en enkelt binding.
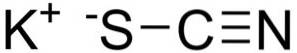
Nomenklatur
- Kaliumthiocyanat
- Kaliumsulfocyanat
- Kaliumsalt af thiocyansyre
- Kalium Rhodanat
- Kalium rhodanid
Ejendomme
Fysisk tilstand
Farveløst eller hvidt fast stof.
Molekylær vægt
97,18 g / mol
Smeltepunkt
173 ºC
Nedbrydningstemperatur
500 ºC
Massefylde
1,88 g / cm3
Opløselighed
Meget opløselig i vand: 217 g / 100 ml ved 20 ° C, 238 g / 100 ml ved 25 ° C. Opløselig i ethanol.
pH
En 5% opløsning af KSCN har en pH-værdi mellem 5,3 og 8,7.
Andre egenskaber
Rene, tørre kaliumthiocyanatprøver er stabile på ubestemt tid, når de opbevares i mørke i tæt dækkede glasbeholdere. I kontakt med direkte sollys bliver de farveløse krystaller dog hurtigt gule..
Opløsninger af rent KSCN-salt beskyttet mod lys er helt stabile.
KSCN er i stand til at hæve gelatine og kollagen. Vandige opløsninger af kaliumthiocyanat ved omsætning med mangandioxid MnOto oxiderer og danner thiocyanogen (SCN)to.
Opnåelse
Kaliumthiocyanat kan fremstilles ved at smelte kaliumcyanid (KCN) med svovl (S). Reaktionen er hurtig og kvantitativ.
KCN + S → KSCN
Det kan opnås i opløsning ved at opløse svovl (S) i benzen eller acetone og tilsætte en opløsning af kaliumcyanid (KCN) i isopropanol. Denne reaktion bruges til at analysere mængden af svovl i en opløsning.
Kaliumthiocyanat kan opnås rent ved successive omkrystallisationer fra vand eller ethanol..
Tilstedeværelse i naturen
Kaliumthiocyanat findes rigeligt i spyt (15 mg / dL), men det er fraværende i blodet.
Også mælken fra nogle pattedyr (såsom køer) har meget små mængder thiocyanat naturligt.
Ansøgninger
I forskellige applikationer
Kaliumthiocyanat er blevet anvendt i forskellige kemiske analyser. Det er blevet brugt til analyse eller titrering af sølvion, også som et reagens og indikator til andre analyser.
KSCN anvendes i farvestoffer og pigmenter. Anvendes i maling og blæk.
I fotoindustrien bruges det især til fremstilling af fotografifilm, da det tjener til at muliggøre en fast aflejring af gelatine fra plastfilm..
Koncentrationen af thiocyanat i blod er blevet brugt i medico-videnskabelige eksperimenter til at bestemme, i hvilken grad nogle mennesker ryger, da thiocyanat er et produkt afledt af hydrogencyanid (HCN) til stede i tobaksrøg..
I dental applikationer
Kaliumthiocyanat er blevet brugt til reparation af dyretænder. Det er blevet anvendt med succes på dentinoverfladen som en forbehandling inden påføring af midlet til at fylde eller tilslutte det åbne hul.
Dentin er det lag, der findes under tændernes emalje.
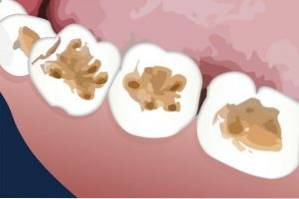
Kaliumthiocyanat favoriserer hævelse af gelatinen på dentinet, så dette lag fjernes let, og der opnås en bedre vedhæftning eller binding af det materiale, der forsegler tanden (harpiks)..
I medicinske videnskabslaboratorier
KSCN anvendes til fremstilling af vacciner eller bakterieekstrakter.
De patogene bakterier dyrkes ved inkubation i egnede laboratoriebeholdere. Derefter tilsættes en fosfat pH-regulator og KSCN til beholderen, hvor bakteriekulturen er placeret..
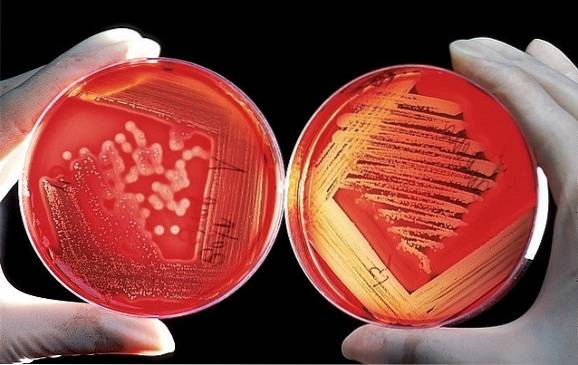
En del af dette bakteriepræparat tages og placeres i en krukke. Den omrøres i et passende tidsrum, og suspensionen centrifugeres for at separere væsken fra det faste materiale. Supernatanten (væske) opsamles og dialyseres.
Resultatet er et ekstrakt, der bruges til vaccination i videnskabelige eksperimenter med forsøgsdyr..
I metalindustrien
Kaliumthiocyanat anvendes til elektropolering af metaller. Elektropolering er en kemisk proces, der gør det muligt at behandle et metaloverflade for at reducere dets mikro ruhed, det vil sige at glatte metaloverfladen.
Dette gøres med elektricitet, hvilket får metallet til at blive glattet til at fungere som den positive pol eller anode i den elektrolytiske celle. Ruheden opløses i kaliumthiocyanatopløsningen, og metallet er således glattere.
På sæt af film eller i teatret
KSCN bruges til simulering af blod i film- og tv-film eller i skuespil.
For eksempel påføres en opløsning af kaliumthiocyanat (KSCN) på det område af kroppen, der vil "lide" snittet eller det simulerede angreb. Plastkniven eller det simulerede skæreobjekt bades i en opløsning af jernchlorid (FeCl3).
Den "skarpe" genstand, der har FeCl, passeres forsigtigt3 på hud fugtet i KSCN. Umiddelbart vil en rød stribe eller plet dannes meget lig den af blod.
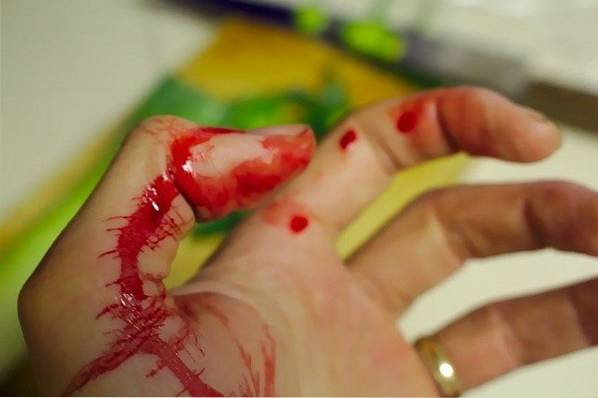
Dette skyldes dannelsen af et kompleks af jernthiocyanat og vand [Fe (NCS) (HtoELLER)5]to+ som har en intens rød farve, der minder meget om blod:
KSCN + FeCl3 + 5 timertoO → [Fe (NCS) (HtoELLER)5]to+ + 2 Cl- + KCl

Kaliumthiocyanat misbrug
Kaliumthiocyanat bruges skrupelløst for at forhindre mælk i at blive angrebet af bakterier eller svampe, mister dets egenskaber og forringes.
I tropiske lande anvendes en metode kaldet "lacto-peroxidase system" eller LP system, som øger mælkens stabilitet, når den opbevares ved høje omgivelsestemperaturer, når køling ikke er mulig..

Denne metode anvender det naturlige antibakterielle system af mælk, som aktiveres ved at øge koncentrationen af thiocyanat (allerede til stede i små mængder i mælk) og hydrogenperoxid (HtoELLERto).
Denne metode er dog ikke tilladt i mange lande af de myndigheder, der regulerer forarbejdede fødevarer..
Nogle skruppelløse mennesker tilføjer KSCN for at mælke irrationelt med eller uden HtoELLERto, hvilket udgør en fare for forbrugerens sundhed, da thiocyanater er stoffer, der forårsager skade på skjoldbruskkirtlen og kan forårsage hypothyroidisme, når de indtages i høje koncentrationer.

Risici
Indånding af kaliumthiocyanatpulver bør undgås. Det anbefales at bruge handsker og beskyttelsesbriller, når du håndterer det. Efter kort eksponering for kaliumthiocyanat kan det forårsage virkninger på nervesystemet, såsom overdreven følelse uden motiv, uro og anfald..
Efter en lang eksponering kan skjoldbruskkirtlen og centralnervesystemet blive påvirket, hvilket manifesterer sig som henholdsvis hypothyroidisme og forringelse af nogle funktioner. Ved indtagelse kan det forårsage forvirring, kvalme, opkastning, krampeanfald og svaghed..
Ved antændelse eller afbrænding af KSCN frigøres meget giftige cyanidgasser; dette sker også, når der tilsættes syrer. I laboratoriet skal det håndteres i et godt ventileret stinkskab..
Referencer
- Jarvinen, L.Z. et al. (1998). Induktion af beskyttende immunitet hos kaniner ved samtidig administration af inaktiverede Pasteurella multocida Toksin- og kaliumthiocyanatekstrakt. Infektion og immunitet, aug. 1998, s. 3788-3795. Gendannet fra ncbi.nlm.nih.gov.
- Tani, Y. og Togaya, T. (1995). Dentin overfladebehandling uden syrer. Dental Materials Journal 14 (1): 58-69, 1995. Hentet fra jstage.jst.go.jp.
- Kolthoff, I.M. og Lingane, J.J. (1935). Kaliumthiocyanat som et primært standardstof. Journal of the American Chemical Society 1935, 57, 11, 2126-2131. Gendannet fra pubs.acs.org.
- Balmasov, A.V. et al. (2005). Elektropolering af sølv i vand-organiske opløsninger af kaliumthiocyanat. Prot Met 41, 354-357 (2005). Gendannet fra link.springer.com.
- Cotton, F. Albert og Wilkinson, Geoffrey. (1980). Avanceret uorganisk kemi. Fjerde udgave. John Wiley & Sons.
- Lide, D.R. (redaktør) (2003). CRC Handbook of Chemistry and Physics. 85th CRC Tryk.
- Tyner, T. og Francis, J. (2017). Kaliumthiocyanat. ACS-reagenskemikalier. Gendannet fra pubs.acs.org.
- Kanthale, P. et al. (2015). Kvalitativ test til påvisning af fremmed thiocyanat i mælk. J Food Sci Technol (marts 2015) 52 (3): 1698-1704. Gendannet fra ncbi.nlm.nih.gov.
- Roy, D. et al. (2018) Silicon Quantum Dot-Based Fluorescent Probe: Synthese Characterization and Recognition of Thiocyanate in Human Blood. ACS Omega 2018, 3, 7, 7613-7620. Gendannet fra pubs.acs.org.
- Gammon, K. (2018). Videnskaben om falsk blod. Inside Science. Gendannet fra insidescience.org.



Endnu ingen kommentarer