
Guld (III) oxid (Au2O3) struktur, egenskaber og anvendelser
Det guld (III) oxid er en uorganisk forbindelse, hvis kemiske formel er AutoELLER3. Teoretisk kunne dets natur forventes at være af den kovalente type. Imidlertid kan tilstedeværelsen af en vis ionisk karakter i dets faste stof ikke udelukkes fuldstændigt; eller hvad er det samme, antag fraværet af Au-kationen3+ ved siden af anionen Oto-.
Det kan virke modstridende, at guld, da det er et ædelt metal, kan ruste. Under normale forhold kan stykker guld (som stjernerne på billedet nedenfor) ikke oxideres ved kontakt med ilt i atmosfæren; dog når det bestråles med ultraviolet stråling i nærværelse af ozon, OR3, panoramaet er anderledes.

Hvis guldstjerner blev udsat for disse betingelser, ville de få en rødbrun farve, der er karakteristisk for AutoELLER3.
Andre metoder til opnåelse af dette oxid ville antyde den kemiske behandling af stjernerne; for eksempel ved at konvertere massen af guld til dets respektive chlorid, AuCl3.
Så til AuCl3, og resten af de mulige guldsalte dannet, tilsættes et stærkt basismedium; og med dette opnås det hydratiserede oxid eller hydroxid, Au (OH)3. Endelig er denne sidste forbindelse termisk dehydreret for at opnå AutoELLER3.
Artikelindeks
- 1 Struktur af guld (III) oxid
- 1.1 Elektroniske aspekter
- 1.2 Hydrater
- 2 egenskaber
- 2.1 Fysisk udseende
- 2.2 Molekylær masse
- 2.3 Densitet
- 2.4 Smeltepunkt
- 2.5 Stabilitet
- 2.6 Opløselighed
- 3 Nomenklatur
- 4 anvendelser
- 4.1 Glasfarvning
- 4.2 Syntese af aurater og fulminant guld
- 4.3 Håndtering af selvmonterede monolag
- 5 Referencer
Struktur af guld (III) oxid
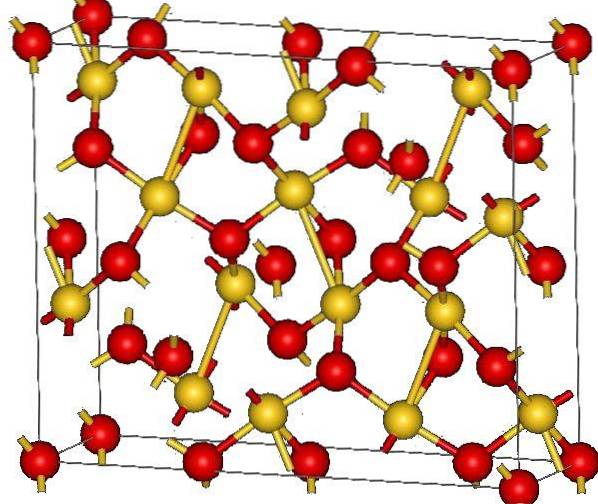
Det øverste billede viser krystalstrukturen af guld (III) oxid. Arrangementet af guld- og iltatomerne i det faste stof vises, enten når man betragter dem som neutrale atomer (kovalent fast stof) eller ioner (ionisk fast stof). Ligegyldigt er det under alle omstændigheder nok at fjerne eller placere Au-O-linkene.
Ifølge billedet antages det, at den kovalente karakter dominerer (hvilket ville være logisk). Af den grund vises atomerne og bindingerne repræsenteret med henholdsvis kugler og søjler. De gyldne kugler svarer til guldatomer (AuIII-O), og de rødlige til iltatomer.
Hvis du ser nøje, vil du se, at der er AuO-enheder4, som er forbundet med iltatomer. En anden måde at visualisere det på ville være at overveje, at hver Au3+ er omgivet af fire O'erto-; selvfølgelig fra et ionisk perspektiv.
Denne struktur er krystallinsk, fordi atomerne er arrangeret og følger det samme langtrækkende mønster. Således svarer dens enhedscelle til det rhombohedrale krystallinske system (det samme i det øverste billede). Derfor er alle AutoELLER3 kunne konstrueres, hvis alle disse sfærer i enhedscellen var fordelt i rummet.
Elektroniske aspekter
Guld er et overgangsmetal, og dets 5d-orbitaler forventes at interagere direkte med iltatets 2p-orbitaler. Denne overlapning af deres orbitaler skulle teoretisk generere ledningsbånd, som ville konvertere AutoELLER3 i en solid halvleder.
Derfor er den sande struktur af AutoELLER3 det er endnu mere komplekst med dette i tankerne.
Hydrater
Guldoxid kan tilbageholde vandmolekyler i dets rombohedriske krystaller, hvilket giver anledning til hydrater. Når sådanne hydrater dannes, bliver strukturen amorf, det vil sige uorden.
Den kemiske formel for sådanne hydrater kan være en af følgende, som faktisk ikke er fuldstændigt klarlagt: AutoELLER3∙ zHtoO (z = 1, 2, 3 osv.), Au (OH)3, eller AuxELLERY(OH)z.
Formlen Au (OH)3 repræsenterer en overforenkling af den sande sammensætning af nævnte hydrater. Dette skyldes, at inden for guld (III) hydroxidet har forskere også fundet tilstedeværelsen af AutoELLER3; og det giver derfor ingen mening at behandle det isoleret som et "simpelt" overgangsmetalhydroxid.
På den anden side fra et fast stof med formlen AuxELLERY(OH)z en amorf struktur kunne forventes; siden det afhænger af koefficienterne x, Y Y z, hvis variationer ville give anledning til alle former for struktur, der næppe kunne udvise et krystallinsk mønster.
Ejendomme
Fysisk fremtoning
Det er et rødbrunt fast stof.
Molekylær masse
441,93 g / mol.
Massefylde
11,34 g / ml.
Smeltepunkt
Smelter og nedbrydes ved 160 ° C. Derfor mangler det et kogepunkt, så dette oxid når aldrig kog..
Stabilitet
AUtoELLER3 det er termodynamisk ustabilt, fordi guld som nævnt i begyndelsen ikke har en tendens til at oxidere under normale temperaturforhold. Så det reduceres let for at blive det ædle guld igen.
Jo højere temperaturen er, jo hurtigere er reaktionen, som er kendt som termisk nedbrydning. Således AutoELLER3 ved 160 ºC nedbrydes den til at producere metallisk guld og frigive molekylært ilt:
2 AutoELLER3 => 4 Au + 3 Oto
En meget lignende reaktion kan forekomme med andre forbindelser, der fremmer reduktionen. Hvorfor reduktion? Fordi guld genvinder de elektroner, som ilt tog fra det; hvilket er det samme som at sige, at det mister bindinger med ilt.
Opløselighed
Det er et fast stof, der er uopløseligt i vand. Det er dog opløseligt i saltsyre og salpetersyre på grund af dannelsen af guldchlorider og nitrater..
Nomenklatur
Guldoxid (III) er navnet, der reguleres af aktienomenklaturen. Andre måder at nævne det på er:
-Traditionel nomenklatur: aurisk oxid, fordi 3+ valensen er den højeste for guld.
-Systematisk nomenklatur: diotrioxid.
Ansøgninger
Glasfarvning
En af de mest fremtrædende anvendelser er at tilføje en rødlig farve til visse materialer, såsom glas, ud over at give visse egenskaber, der er forbundet med guldatomer..
Syntese af aurater og fulminant guld
Hvis Au tilføjestoELLER3 til et medium, hvor det er opløseligt, og i nærvær af metaller kan aurater udfældes efter tilsætning af en stærk base; som er dannet af AuO-anioner4- i selskab med metalkationer.
Også AutoELLER3 reagerer med ammoniak til dannelse af den fulminant guldforbindelse, AutoELLER3(NH3)4. Navnet stammer fra det faktum, at det er meget eksplosivt.
Håndtering af selvmonterede monolag
Visse forbindelser, såsom dialkyldisulfider, RSSR, adsorberes ikke på samme måde på guld og dets oxid. Når denne adsorption finder sted, dannes en Au-S-binding spontant, hvor svovlatomet udviser og definerer overfladens kemiske egenskaber afhængigt af den funktionelle gruppe, hvortil det er bundet..
RSSR'er kan ikke adsorberes på AutoELLER3, men ja på metallisk guld. Derfor, hvis overfladen af guldet er modificeret og dets oxidationsgrad såvel som størrelsen af partiklerne eller lagene af AutoELLER3, en mere heterogen overflade kan designes.
Denne overflade AutoELLER3-AuSR interagerer med metaloxiderne i visse elektroniske enheder og udvikler således fremtidige smartere overflader.
Referencer
- Wikipedia. (2018). Guld (III) oxid. Gendannet fra: en.wikipedia.org
- Kemisk formulering. (2018). Guld (III) oxid. Gendannet fra: formulacionquimica.com
- D. Michaud. (2016, 24. oktober). Guldoxider. 911 Metallurg. Gendannet fra: 911metallurgist.com
- Shi, R. Asahi og C. Stampfl. (2007). Egenskaber for guldoxiderne AutoELLER3 og AutoEller: undersøgelse af de første principper. The American Physical Society.
- Cook, Kevin M. (2013). Guldoxid som maskeringslag til regioselektiv overfladekemi. Specialer og afhandlinger. Paper 1460.



Endnu ingen kommentarer