
Forgrenede alkanstrukturer, egenskaber og eksempler
Det forgrenede alkaner de er mættede kulbrinter, hvis strukturer ikke består af en lige kæde. Lige kæder alkaner adskiller sig fra deres forgrenede isomerer ved at tilføje et bogstav n forud for navnet. Således betyder n-hexan, at strukturen består af seks carbonatomer justeret i en kæde.
Grenene på en bar træhimmel (nederste billede) kunne sammenlignes med grenene på forgrenede alkaner; tykkelsen af dens kæder, hvad enten de er hoved-, sekundære eller tertiære, har imidlertid alle de samme dimensioner. Hvorfor? Fordi der er enkle CC-obligationer i dem alle.

Træer har tendens til at forgrene sig, når de vokser; det gør alkaner også. Oprethold en konstant kæde med visse methylenenheder (-CHto-) indebærer en række energiske forhold. Jo mere energi alkanerne har, jo større tendens til at forgrene sig.
Både lineære og forgrenede isomerer har de samme kemiske egenskaber, men med små forskelle i kogende, smeltende og andre fysiske egenskaber. Et eksempel på en forgrenet alkan er 2-methyl-propan, den enkleste af alle.
Artikelindeks
- 1 Kemiske strukturer
- 2 Kemiske og fysiske egenskaber
- 2.1 Kogepunkter og smeltepunkter
- 2.2 Densitet
- 3 Nomenklatur og eksempler
- 4 Referencer
Kemiske strukturer
Forgrenede og lineære alkaner har den samme generelle kemiske formel: CnH2n + 2. Det vil sige, at begge, for et givet antal carbonatomer, har det samme antal hydrogener. Derfor er de to typer forbindelser isomerer: de har den samme formel men forskellige kemiske strukturer..
Hvad observeres først i en lineær kæde? Et endeligt antal methylengrupper, -CHto-. Således er ch3CHtoCHtoCHtoCHtoCHtoCH3 er en ligekædet alkan kaldet n-heptan.
Bemærk de fem på hinanden følgende methylengrupper. Det skal også bemærkes, at disse grupper udgør alle kæderne og derfor har samme tykkelse, men med variable længder. Hvad mere kan man sige om dem? Hvilke er 2 º-carbonatomer, det vil sige carbonatomer forbundet med to andre.
For at n-heptanen skal forgrene sig, er det nødvendigt at omarrangere dets kulstoffer og hydrogener. Hvordan? Mekanismerne kan være meget komplekse og involvere migration af atomer og dannelsen af positive arter kendt som karbocationer (-C+).
Imidlertid er det på papir nok at arrangere strukturen på en sådan måde, at der er 3. og 4. kulstof; med andre ord kulhydrater bundet til tre eller fire andre. Denne nye ordre er mere stabil end de lange grupperinger af CH-grupperto. Hvorfor? Fordi 3. og 4. kulstof er energisk mere stabil.
Kemiske og fysiske egenskaber
Forgrenede og lineære alkaner med de samme atomer bevarer de samme kemiske egenskaber. Deres bindinger forbliver enkle, C-H og C-C, og med ringe forskel i elektronegativiteter, så deres molekyler er apolare. Forskellen, der er nævnt ovenfor, ligger i 3. og 4. kulstof (CHR3 og CR4).
Men når kæden forgrener sig til isomerer, ændres måden, hvorpå molekylerne interagerer med hinanden..
For eksempel er måden at forbinde to lineære grene af et træ ikke den samme som at sætte to stærkt forgrenede oven på hinanden. I den første situation er der meget overfladekontakt, mens i den anden er "hullerne" mellem grenene dominerende. Nogle grene interagerer mere med andre end med hovedgrenen.
Alt dette resulterer i lignende værdier, men ikke det samme i mange af de fysiske egenskaber.
Kogepunkter og smeltepunkter
De flydende og faste faser af alkaner er udsat for intermolekylære kræfter under specifikke betingelser for tryk og temperatur. Da molekylerne af de forgrenede og lineære alkaner ikke interagerer på samme måde, vil deres væsker eller faste stoffer heller ikke være de samme..
Smelte- og kogepunkter øges med antallet af kulhydrater. For lineære alkaner er disse proportionale med n. Men for forgrenede alkaner afhænger situationen af, hvor forgrenet hovedkæden er, og hvad substituenten eller alkylgrupperne er (R).
Hvis de lineære kæder betragtes som rækker af zigzags, så passer de perfekt oven på hinanden; men med de forgrenede interagerer hovedkæderne næppe, fordi substituenterne holder dem adskilt fra hinanden.
Som et resultat har forgrenede alkaner en mindre molekylær kontaktoverflade, og derfor har deres smelte- og kogepunkter tendens til at være lidt lavere. Jo mere forgrenet strukturen er, desto lavere vil disse værdier stadig være.
For eksempel n-pentan (CH3CHtoCHtoCHtoCH3) har en Peb på 36,1 ºC, mens 2-methyl-butan (CH3CHto(CH3CHtoCH32,2-dimethylpropan (C (CH3)4) på 27,8 og 9,5 ° C.
Massefylde
Ved hjælp af samme ræsonnement er forgrenede alkaner lidt mindre tætte på grund af det faktum, at de optager et større volumen på grund af faldet i overfladekontakt mellem hovedkæderne. Ligesom lineære alkaner er de blandbare med vand og flyder over det; de er mindre tætte.
Nomenklatur og eksempler
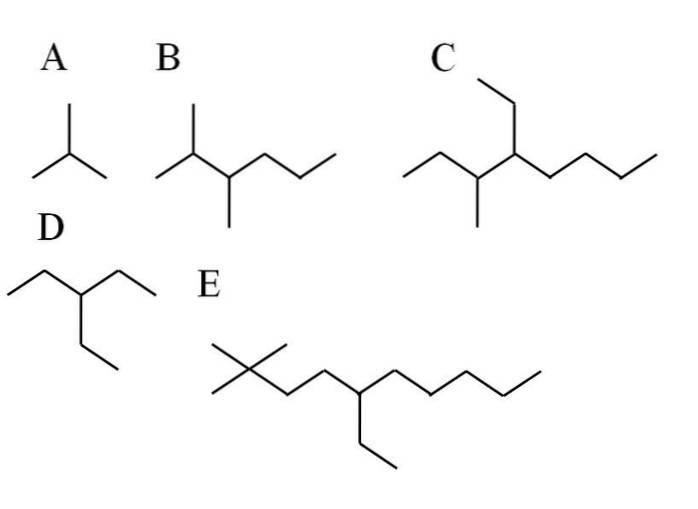
Fem eksempler på forgrenede alkaner er vist i billedet ovenfor. Bemærk, at grenene er kendetegnet ved at have 3. eller 4. kulstof. Men hvad er hovedkæden? Den med det højeste antal kulstofatomer.
-I A betyder det ikke noget, da uanset hvilken kæde der vælges, har de begge 3 C. Så deres navn er 2-methyl-propan. Det er en isomer af butan, C4H10.
-Alkane B har ved første øjekast to substituenter og en lang kæde. Til -CH grupper3 de er nummereret på en sådan måde, at de har mindst antal; derfor begynder kulstofferne at tælle fra venstre side. Således kaldes B 2,3-dimethyl-hexan.
-For C gælder det samme som for B. Hovedkæden har 8 C, og de to substituenter er en CH3 og en CHtoCH3 de er mere til venstre. Dets navn er derfor: 4-ethyl-3-methyloctan. Bemærk, at -ethylsubstituenten er nævnt før -methyl i alfabetisk rækkefølge.
-I tilfælde af D betyder det ikke noget, hvor kulstofferne i hovedkæden tælles. Dens navn er: 3-ethyl-propan.
-Og endelig for E, en lidt mere kompleks forgrenet alkan, har hovedkæden 10 C, og den begynder at tælle fra en hvilken som helst af CH-grupperne3 til venstre. Gør det på denne måde, dets navn er: 5-ethyl-2,2-dimethyl-decan.
Referencer
- Carey, F. A. (2006). Organic Chemistry Sixth Edition. Redaktionel Mc Graw Hill, side 74-81.
- John T. Moore, Chris Hren, Peter J. Mikulecky. Sådan navngives forgrenede alkaner i kemi. Gendannet fra: dummies.com
- Dr. Ian Hunt. (2014). Enkle forgrenede alkaner. Hentet fra: chem.ucalgary.ca
- Helmenstine, Anne Marie, Ph.D. (8. januar 2018). Forgrenet alkanedefinition. Gendannet fra: thoughtco.com
- Kemi LibreTexts. Forgrenede alkaner. Hentet fra: chem.libretexts.org
- Alkaner: struktur og egenskaber. Hentet fra: uam.es
- Nomenklatur: alkaner. [PDF]. Hentet fra: quimica.udea.edu.co

Endnu ingen kommentarer