
Sulfanilinsyre struktur, egenskaber, syntese, anvendelser

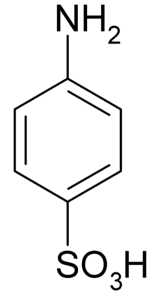
Det sulfanilsyre er en krystallinsk forbindelse, hvis molekyle er dannet af en benzenring, hvortil en basisk gruppe (-NHtoog en syregruppe (-SO3H). Dens kemiske formel er NHtoC6H4SW3H.
Det er også kendt som 4-aminobensensulfonsyre. Det fremstilles ved sulfonering af anilin i para-stilling. Dens krystaller er hvide eller gråhvide. Dens adfærd svarer mere til et salt end en organisk forbindelse med NH-grupperto bjørn3H. Derfor er det uopløseligt i de fleste organiske opløsningsmidler.
En af dens vigtigste anvendelser er i syntesen af farvestoffer, da den let danner en diazo-forbindelse, der er et råmateriale til denne anvendelse..
Både sulfanilsyre og derivater deraf er blevet anvendt som antibakterielle midler. Det bruges til syntese af mucolytiske forbindelser, da de har evnen til at nedsætte viskositeten af slim eller meget viskøse biologiske væsker..
Det bruges også i papirindustrien og i formler til graveringer eller litografier. Det er en del af harpikser, der bruges i beton- eller mørtelblandinger for at tillade dem at opretholde deres fluiditet i lang tid uden at påvirke den endelige hærdningstid.
Det er en fremmedhadsmetabolit, det betyder, at den ikke produceres naturligt af levende væsener. Det er irriterende for hud, øjne og slimhinder. Derudover kan det forurene miljøet.
Artikelindeks
- 1 Struktur
- 2 Nomenklatur
- 3 egenskaber
- 3.1 Fysisk tilstand
- 3.2 Molekylvægt
- 3.3 Smeltepunkt
- 3.4 Tæthed
- 3.5 Opløselighed
- 3.6 Kemiske egenskaber
- 3.7 Andre egenskaber
- 4 Syntese
- 5 anvendelser
- 5.1 I farvestofindustrien
- 5.2 I analytisk kemi
- 5.3 I medicin som et antibakterielt middel
- 5.4 I medicin som et mucolytisk middel
- 5.5 I bioassaylaboratorier
- 5.6 I papirindustrien
- 5.7 I udskrifter, graveringer eller litografier
- 5.8 I byggematerialer
- 6 Referencer
Struktur
Sulfanilsyre har hvide krystaller dannet af orthorhombiske eller monokliniske plader. Dets monohydrat krystalliserer i vand i form af orthorhombiske plader. Hvis krystallisationen forløber meget langsomt, krystalliserer dihydratet. Monohydratet bliver vandfrit, når det er tæt på 100 ºC.
Nomenklatur
- Sulfanilsyre.
- P-aminobenzensulfonsyre.
- 4-Aminobenzensulfonsyre.
Ejendomme
Fysisk tilstand
Hvidt eller off-white krystallinsk fast stof.
Molekylær vægt
173,19 g / mol.
Smeltepunkt
Det nedbrydes ved omkring 288 ° C uden at smelte. Det rapporteres også ved> 320 ºC.
Massefylde
1,49 g / cm3
Opløselighed
Næsten uopløselig i vand: 10,68 g / L ved 20 ºC.
Uopløselig i ethanol, benzen og ether. Let opløselig i varm methanol.
Opløselig i vandige opløsninger af baser. Uopløselig i vandige opløsninger af mineralsyrer. Opløselig i koncentreret saltsyre.
Kemiske egenskaber
Dens egenskaber adskiller sig fra egenskaberne ved andre amino- eller sulfonerede forbindelser, idet de svarer til et salts. Dette skyldes, at dens struktur faktisk indeholder -NH-grupperne3+ Også3-, hvilket giver det zwitterioniske egenskaber.
Den indeholder en syregruppe og en basisk gruppe i modsatte poler af det samme molekyle. Men hydrogenionen er bundet til nitrogen i stedet for ilt, fordi -NH-gruppento er en stærkere base end -SO-gruppen3-.
Fordi det er en zwitterion, har det et højt smeltepunkt og uopløselighed i organiske opløsningsmidler..
Sulfanilinsyre er opløselig i alkalisk opløsning, fordi hydroxidionen OH-, da den er stærkt basisk, starter den en hydrogenion (H+) af den svage basale gruppe -NHto, danner p-aminobensensulfonationen, som er opløselig i vand.
I syreopløsning ændres strukturen af sulfanilsyre ikke, derfor forbliver den uopløselig.
Andre egenskaber
Når det opvarmes til nedbrydning, udsender det giftige dampe af nitrogenoxider og svovl.
Eksponering for sulfanilsyre kan føre til symptomer som irritation af hud, øjne og slimhinder. Det er en ætsende forbindelse.
Syntese
Det fremstilles ved omsætning af anilin med svovlsyre (HtoSW4) ved høje temperaturer. Oprindeligt dannes syreaniliniumsulfatsaltet, som når det opvarmes til 180-200 ºC omorganiseres til dannelse af den substituerede ring i para-stilling, da det er det mest stabile produkt.
For at forberede det med en høj grad af renhed sulfoneres en blanding af anilin og sulfolan med HtoSW4 ved 180-190 ºC.
Ansøgninger
I farvestofindustrien
Sulfanilsyre anvendes til syntese eller fremstilling af forskellige farvestoffer, såsom methylorange og tartrazin. Til dette er det diazotiseret og genererer diazotiseret sulfanilsyre..
Det er vigtigt at bemærke, at tartrazin er blevet brugt som farvestof i mad. Men når det er indtaget, genererer det visse metabolitter i menneskekroppen, herunder sulfanilsyre, som muligvis er ansvarlige for dannelsen af reaktive iltarter. Disse kan påvirke nyre (nyrer) eller lever (lever) væv..

I analytisk kemi
Det bruges som et reagens til bestemmelse af forskellige kemiske forbindelser, herunder nitrit..
I medicin som et antibakterielt middel
Sulfanilamid, afledt af sulfanilsyre, kan anvendes i den farmaceutiske industri, da det har antibakteriel aktivitet.
I menneskekroppen forveksler bakterier det med p-aminobenzoesyre, som er en essentiel metabolit. Denne substitution betyder, at bakterierne ikke reproducerer og dør.
Et andet derivat af sulfanilsyre opnået ved kondensation med andre forbindelser har også antibakterielle egenskaber, der er baseret på dens evne til at fortrænge folsyre (et medlem af vitamin B-komplekset)..
Denne forbindelse kan tages oralt, injiceres intravenøst eller påføres eksternt i en salve..
I medicin som et mucolytisk middel
Der er anvendt et derivat af sulfanilsyre, der har mucolytisk aktivitet. Dette er, at det præsenterer flydende aktivitet af slim, for at opløse selve slim eller meget viskøse biologiske væsker.
Forbindelsen kan anvendes til at frembringe væskeformning af slim produceret af et væv på grund af patologiske tilstande. For eksempel overbelastning af åndedrætssystemet eller blandt andet fra vaginalkanalen.
Når det kommer til væskeform i slimhinderne i luftvejene, indgives produktet ved indånding, dråber i næsen, tåge, aerosoler eller forstøver. Det er en behandling, der gælder for mennesker eller pattedyr. Det er en mere kraftfuld forbindelse end dem, der er baseret på cystein.

Det bruges også i laboratoriet, når det ønskes at reducere viskositeten af biologiske væsker for at lette analytiske bestemmelser..
I bioanalyselaboratorier
Diazotiseret sulfanilsyre (et derivat fremstillet ved omsætning af sulfanilsyre med natriumnitrit) anvendes til bestemmelse af bilirubin.
Bilirubin er et gult pigment, der findes i galden. Overskydende bilirubin i blodet er en konsekvens af leversygdomme, hæmatologiske (eller blod) lidelser eller lidelser i galdevejen.
For at måle mængden af bilirubin i blodet omsættes diazo afledt af sulfanilsyre med bilirubin til dannelse af azobilirubinkomplekset, hvis intensitet måles med et kolorimeter eller spektrofotometer. På denne måde bestemmes bilirubinindholdet i blodserum..
I papirindustrien
Sulfanilsyre gør det muligt at syntetisere en papirpolish, det vil sige en forbindelse, der giver den en optisk glans eller et hvidt udseende, da det neutraliserer den gule farve af naturligt eller ubehandlet papir..

Det har fordelen i forhold til andre forbindelser, idet det kan anvendes i relativt høje koncentrationer til behandling af papirmasse under lave pH-betingelser uden at øge papirets gulhed..
Resultatet er tydeligt, når papiret observeres med UV (ultraviolet) lys, under hvilket det fluorescerer meget mere, end når andre forbindelser anvendes, og med synligt lys observeres det, at graden af gulhed er meget lav.
Det er meget opløseligt i vand, hvilket gør det muligt at bruge det i mere koncentrerede opløsninger. Kan bruges på alle typer papir, inklusive papir fremstillet af formalet træmasse, sulfitmasse eller enhver anden proces.
I udskrifter, graveringer eller litografier
Sulfanilic syre fungerer som en syrningsmiddel i koncentrerede opløsninger til litografi uden at præsentere problemerne med andre syrer såsom fosforsyre, er mindre giftige og mindre forurenende end sidstnævnte..
I byggematerialer
Sulfanilsyre-modificerede vandige melamin-formaldehyd-harpiksopløsninger er blevet testet i beton (beton), mørtel eller cementpasta. Formålet har været at reducere vandindholdet og forhindre et fald i blandingens fluiditet over tid uden at reducere indstillingstiden..
Beton eller mørtel fremstillet med disse opløsninger er meget effektiv om sommeren, når faldet i fluiditet over tid er et problem..
Hvis mørtel eller beton er klargjort med disse opløsninger og af en eller anden grund skal hvile, kan cementsammensætningen let hældes i forme eller lignende, da den ikke har mistet fluiditet over tid..

Referencer
- Windholz, M. et al. (redaktører) (1983). Merck-indekset. En encyklopædi med kemikalier, lægemidler og biologiske stoffer. Tiende udgave. Merck & CO., Inc..
- Kirk-Othmer (1994). Encyclopedia of Chemical Technology. Bind 2. fjerde udgave. John Wiley & Sons.
- National Library of Medicine. (2019). Sulfanilsyre. Gendannet fra: pubchem.ncbi.nlm.nih.gov
- Urist, H. og Martin, G.J. (1950). Sulfanilsyrederivater. US patent nr. 2.504.471. Overdragere til The National Drug Company. 18. april 1950.
- Villaume, Frederick G. (1964). Blødgøringssammensætning til papir afledt af methanil- og sulfanilinsyrer. US patent nr. 3.132.106. 5. maj 1964.
- Martin, Tellis A. og Comer, William T. (1979). Benzoesyrederivat og benzensulfonsyre mucolytisk proces. US patent nr. 4.132.802. 2. januar 1979.
- Druker, L.J. og Kincaid, R.B. (1979). Litografisk springvandskoncentrat. US patent nr. 4.150.996. 24. april 1979.
- Shull, Bruce C. (1983). Bilirubin-analyse. US patent nr. 4.404.286. 13. september 1983.
- Uchida, J. et al. (2001). Fremgangsmåde til fremstilling af en vandig opløsning af sulfanilsyremodificeret melamin-formaldehydharpiks og en cementsammensætning. US patent nr. 6,214,965 B1. 10. april 2001.
- Corradini, M.G. (2019). Bind 1. I Encyclopedia of Food Chemistry. Gendannet fra sciencedirect.com.



Endnu ingen kommentarer