
Hexan (C6H14) fysiske og kemiske egenskaber, struktur, anvendelser, toksicitet
Det hexan er et carbonhydrid, der er karakteriseret ved at være en organisk forbindelse, hvis kondenserede kemiske formel er C6H14. Det er en farveløs, gennemsigtig væske, der ikke kan blandes med vand. Den har fem isomerer, hvor den lineære er en af de vigtigste paraffiniske kulbrinter i industrien og forskningen.
Hexan opnås ved fraktioneret destillation af råolie. Ligeledes er det naturligt til stede i citrusfrugter og i flygtige fraktioner af forskellige planter eller frugter såsom æble, guava, ristede hasselnødder, sød kartoffel og salvie..
Det er en meget brandfarlig flygtig væske, der findes i benzin, hurtigtørrende lim og gummicement. Hexan bruges som opløsningsmiddel i ekstraktionsprocessen af vegetabilske olier såvel som lipider og fedtstoffer til stede i forurenet vand og jord.
Mennesker, der er professionelt udsat for hexan, kan opleve perifere nervesystemskader, der manifesteres ved prikken og kramper i ben og arme; ud over generaliseret muskelsvaghed og i svære tilfælde skeletmuskulaturrofi.
Artikelindeks
- 1 Fysiske og kemiske egenskaber af hexaner
- 1.1 Fysisk udseende
- 1.2 Molær masse
- 1.3 Lugt
- 1.4 Lugttærskel
- 1,5 Massefylde
- 1.6 Smeltepunkt
- 1.7 Kogepunkt
- 1.8 Flammepunkt
- 1.9 Opløselighed i vand
- 1.10 Opløselighed i opløsningsmidler
- 1.11 Relativ damptæthed med luft
- 1.12 Octanol / vand fordelingskoefficient
- 1.13 Damptryk
- 1.14 Bølgelængde med maksimal optisk tæthed
- 1.15 Brydningsindeks
- 1.16 Viskositet
- 1.17 Kalorikapacitet
- 1.18 Forbrændingsvarme
- 1.19 Fordampningsvarme
- 1.20 Overfladespænding
- 1.21 Ioniseringspotentiale
- 1.22 Stabilitet
- 1.23 Reaktivitet
- 2 Struktur af hexan
- 2.1 Intermolekylære interaktioner
- 2.2 Isomerer
- 3 anvendelser
- 4 Toksicitet
- 4.1 Indånding og kontakt
- 4.2 Sikker dosis
- 5 Referencer
Fysiske og kemiske egenskaber af hexaner
Fysisk fremtoning
Farveløs, gennemsigtig og meget flygtig væske.
Molar masse
86,178 g / mol
Lugt
Svarende til benzin
Lugtgrænse
1,5 ppm
Massefylde
0,6606 g / ml
Smeltepunkt
-96 til -94 ºC
Kogepunkt
68,5 til 69,1 ºC
antændelsespunkt
-22 ºC (lukket kop).
Vandopløselighed
9,5 mg / L (praktisk talt blandbar med vand)
Opløselighed i opløsningsmidler
Meget opløselig i ethanol, opløselig i ethylether og chloroform. Blandbar med alkohol, chloroform og ether.
Relativ damptæthed med luft
2,97 (luft = 1)
Fordelingskoefficient for oktanol / vand
Log P = 3.764
Damptryk
17,60 kPa ved 20 ºC
Bølgelængde med maksimal optisk tæthed
200 nm
Brydningsindeks
1.375
Viskositet
0,3 mPa s
Kalorikapacitet
265.2 JK-1Muldvarp-1
Forbrændingsvarme
4.163,2 kJ mol-1
Fordampningsvarme
31,56 kJ mol-1
Overfladespænding
17,89 mN / m ved 25 ºC
Ioniseringspotentiale
10,18 eV
Stabilitet
Stabil. Uforenelig med oxidationsmidler, klor, fluor, magnesiumperchlorat. Danner en eksplosiv blanding med luft.
Reaktivitet
Hexan kan reagere kraftigt med oxiderende materialer, som kan omfatte flydende chlor, koncentreret ilt, natriumhypochlorit og calciumhypochlorit. Det er også uforeneligt med dinitrogentetroxid. Hexan kan angribe nogle former for plast, gummi og belægninger.
Struktur af hexan
Intermolekylære interaktioner
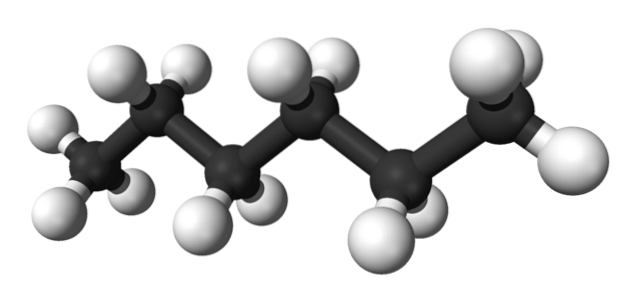
Det første billede viser molekylet af n-hexan repræsenteret af en kugle-og-stick-model. De sorte kugler svarer til kulstofatomer, der udgør det zigzaggende kulstofskelet, mens de hvide kugler er hydrogenatomer. Det n-Hexan er derfor et kulbrinte, lineært og meget dynamisk.
Fordi alle dets CH-bindinger har lav polaritet, mangler molekylet et dipolmoment. Dermed er deres intermolekylære interaktioner ikke af dipol-dipol-typen, men afhænger udelukkende af molekylær masse og Londons dispersive kræfter..
Hvert molekyle af n-Hexan "passer" på hinanden ved meget lave temperaturer, som man antager i dens krystallinske struktur. På den anden side, i væsken, bøjer deres skeletter og roterer deres CH-bindinger, hvilket får væsken til at være flygtig og koge ved 68,7 ºC..
Isomerer
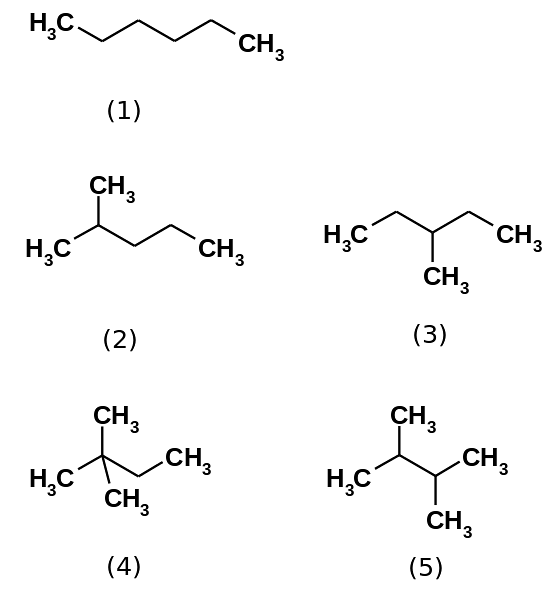
Hydrocarbonhexanen består faktisk af fem isomerer, idet de er n-hexan mindst forgrenet, (1). De andre fire isomerer er i stigende rækkefølge:
2-methylpropan (2)
3-methylpropan (3)
2,2-dimethylbutan (4)
2,3-dimethylbutan (5)
Bemærk også, at strukturerne bliver mere forgrenede fra (1) til (5). Da de er mere forgrenede, falder de dispersive kræfter, da der ikke længere er lineære dele, der kiler effektivt. Dette fører til et fald og variation i isomerernes kogepunkter; skønt der observeres nogle acceptable afvigelser.
Både 2-methylpropan (kp = 60,3 ° C) og 3-methylpropan (kp = 63,3 ° C) er lige forgrenede, men deres kogepunkter er forskellige. Derefter efterfølges det af 2,3-dimethylbutan (peb = 58 ºC) for endelig at lokalisere 2,2-dimethylbutan som den mest flygtige væske (peb = 49,7 ºC).
Ansøgninger
Hexan blandes med lignende kemikalier for at producere opløsningsmidler. Blandt navnene på disse opløsningsmidler er kommerciel hexan, blandede hexaner osv. De bruges som rengøringsmidler i tekstil-, møbel- og dybtrykindustrien..
Hexan er en ingrediens i lim, der bruges til tagtætning, fodtøj og læder. Det bruges også til at binde bøger, til støbning af piller og tabletter, konservering, fremstilling af dæk og baseball..
Hexan anvendes til bestemmelse af brydningsindekset for mineraler og fyldningsvæske til termometre i stedet for kviksølv; normalt med en rød eller blå nuance. Det bruges også til ekstraktion af fedt og olie fra vand til analyse af dets forurenende stoffer..
Hexan bruges som opløsningsmiddel ved ekstraktion af olie fra vegetabilske frø, såsom sojabønner, raps eller brombær. Derudover bruges det til affedtning af dele af forskellig oprindelse. Det bruges til denaturering af alkohol, i HPLC-analysemetoden og i spektrofotometri.
Toksicitet
Indånding og kontakt
Den akutte toksicitet af hexan er relativt lav, skønt det er en mild bedøvelsesmiddel. Akut eksponering for høje koncentrationer af hexan kan ved indånding fremkalde mild centralnervesystemdepression (manifesteret ved svimmelhed, svimmelhed, mild kvalme og hovedpine)..
Det kan også forårsage dermatitis og irritation af øjne og hals. Kronisk indånding af hexan, relateret til arbejdsaktivitet, kan forårsage skade på det perifere nervesystem (sensorimotorisk polyneuropati).
De første symptomer er prikken og kramper i ben og arme efterfulgt af muskelsvaghed. I alvorlige tilfælde kan skeletmuskelatrofi forekomme sammen med tab af koordination og synsproblemer.
Hexantoksicitet er relateret til dannelsen af hexan-2,5-dionmetabolitten. Det reagerer med aminosyren lysin i en proteinsidekæde og forårsager tab af proteinfunktion..
Sikker dosis
Miljøstyrelsen (EPA) beregnede en referencekoncentration (RfC) for hexan på 0,2 mg / m3, og en referencedosis (RfD) på 0,06 mg / kg legemsvægt / dag.
I 1960'erne og 1970'erne havde en gruppe arbejdere i skomagerindustrien i Japan tilstedeværelse af nervesygdomme. Årsagen var, at de åndede en hexanatmosfære på 500 - 2.500 ppm i 8-14 timer om dagen.
Arbejdstagerne udviste de kendte symptomer på kronisk inhalation af hexan og opdagede lægerne, at nerverne, der styrede musklerne i arme og ben, blev beskadiget..
Referencer
- Danielle Reid. (2019). Hexan: struktur, formel og egenskaber. Undersøgelse. Gendannet fra: study.com
- National Center for Biotechnology Information. (2019). Hexan. PubChem-database. CID = 8058. Gendannet fra: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2019). Hexan. Gendannet fra: en.wikipedia.org
- World of Molecules. (s.f.). Hexanmolekyle. Gendannet fra: worldofmolecules.com
- Kemikaliebog. (2017). Hexan. Gendannet fra: chemicalbook.com
- Australiens Commonwealth. (s.f.). n-hexan: Emissionskilder. Gendannet fra: npi.gov.au
- EPA. (2000). Hexan. [PDF]. Gendannet fra: epa.gov
- Agentur for toksiske stoffer og sygdomsregistrering. (1999). Erklæring om folkesundhed for n-hexan. Gendannet fra: atsdr.cdc.gov



Endnu ingen kommentarer