
Steroidhormonstruktur, syntese, virkningsmekanisme
Det steroidhormoner De er stoffer fremstillet af kirtler med intern sekretion, og som dumpes direkte i kredsløbets strøm, hvilket fører dem til vævene, hvor de udøver deres fysiologiske virkning. Dets generiske navn stammer fra det faktum, at det har en steroidkerne i sin grundlæggende struktur..
Kolesterol er det foregående stof, hvorfra alle steroidhormoner syntetiseres, som er grupperet i gestagener (f.eks. Progesteron), østrogener (estron), androgener (testosteron), glukokortikoider (kortisol), mineralokortikoider (aldosteron) og D-vitamin.
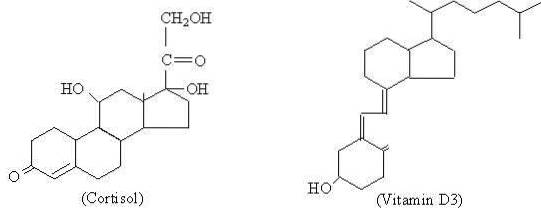
Selvom de forskellige steroidhormoner præsenterer molekylære forskelle mellem dem, hvilket er hvad der giver dem deres forskellige funktionelle egenskaber, kan det siges, at de har en grundlæggende struktur, der er fælles for dem, og som er repræsenteret af cyclopentaneperhydrophenanthren med 17 carbonatomer..
Artikelindeks
- 1 Struktur af steroider
- 1.1 C21
- 1.2 C19
- 1.3 C18
- 2 Syntese
- 2.1 - Syntese på niveauet af binyrebarken
- 2.2 - Androgensyntese
- 2.3 - Syntese af mandlige kønssteroider i testiklerne
- 2.4 - Syntese af kvindelige kønssteroider i æggestokkene
- 3 Handlingsmekanisme
- 4 Aldosteron som et eksempel
- 5 Referencer
Struktur af steroider
Steroider er organiske forbindelser af meget forskelligartet natur, der har det til fælles, hvad der kan betragtes som en moderkerne, der består af fusion af tre ringe med seks carbonatomer (cyclohexaner) og et af fem carbonatomer (cyclopentan).
Denne struktur er også kendt som "cyclopentaneperhydrophenanthrene". Da ringene er indbyrdes forbundne, er det samlede antal kulstofatomer, der udgør den, 17; Imidlertid har de fleste naturlige steroider methylgrupper i carbon 13 og 10, som repræsenterer henholdsvis carbon 18 og 19..

Mange af de naturlige steroidforbindelser har også en eller flere grupper med alkoholisk funktion i ringstrukturen og kaldes derfor steroler. Blandt dem er kolesterol, som har en alkoholfunktion ved carbon 3 og en carbonhydrid-sidekæde med 8 carbonatomer bundet til carbon 17; atomer, der er nummereret fra 20 til 27.
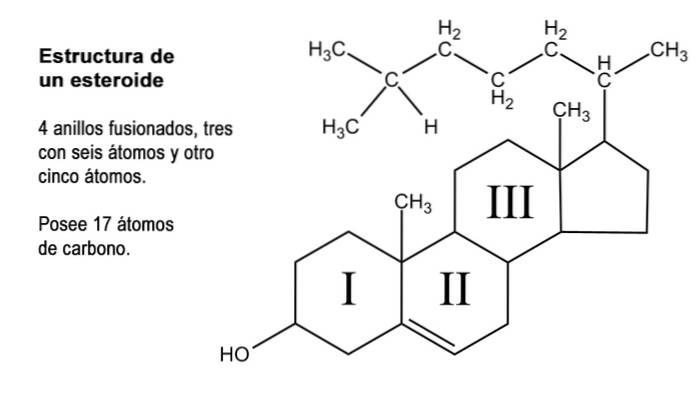
Ud over disse 17 carbonatomer kan steroidhormoner have 1, 2 eller 4 flere af disse atomer i deres struktur, for hvilke der er genkendt tre typer steroider, nemlig: C21, C19 og C18.
C21
C21'erne, som progesteron og binyrebarksteroider (glukokortikoider og mineralokortikoider), stammer fra "gravidan". Den har 21 kulstofatomer, fordi der tilsættes 17 af den basiske ring de to af methylgrupperne i carbon 13 og 10 og to carbonatomer i sidekæden fastgjort til C17, der oprindeligt i kolesterol var 8 carbonatomer.
C19
C19'erne svarer til kønshormoner med androgen aktivitet og stammer fra "androstan" (19 carbonatomer), som er strukturen, der forbliver, når gravidan mister de to carbonatomer i C17-sidekæden, som erstattes af en hydroxyl- eller en ketongruppe.
C18
C18-steroider er kvindelige hormoner eller østrogener, der hovedsageligt syntetiseres i de kvindelige kønskirtler, og hvis fremragende karakteristika i forhold til de to andre typer steroider er fraværet af den methyl, der er til stede i sidstnævnte, bundet til carbonet i position 10.
Under syntesen fra cholesterol produceres enzymatiske modifikationer, der ændrer antallet af carbonatomer og fremmer dehydrogeneringer og hydroxyleringer af specifikke carbonatomer i strukturen..
Syntese
Cellerne, der producerer steroidhormoner, er hovedsageligt placeret i cortex i binyrerne, hvor der produceres glukokortikoider såsom kortisol, mineralokortikoider såsom aldosteron og mandlige kønshormoner såsom dehydroepiandrosteron og androstenedion..
Mandlige kønskirtler er ansvarlige for produktionen af androgener, herunder de førnævnte hormoner og testosteron, mens de modne ovariefollikler producerer progesteron og østrogener..
Syntesen af alle steroidhormoner starter fra kolesterol. Dette molekyle kan syntetiseres af celler, der producerer steroidhormoner, men for det meste opnås det af disse celler fra lipoproteiner med lav densitet (LDL) til stede i cirkulerende plasma..
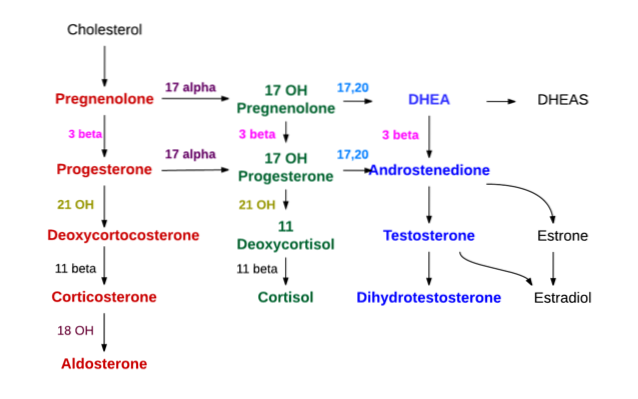
- Syntese på niveauet af binyrebarken
Tre lag skelnes i binyrebarken, kendt udefra i henholdsvis de glomerulære, fascikulære og retikulære zoner..
I det glomerulære syntetiseres mineralokortikoider (aldosteron) hovedsageligt i de fascikulære glukokortikoider såsom kortikosteron og cortisol og i retikulære androgener såsom dehydroepiandrosteron og androstenedion.
Glukokortikoid syntese
Det første trin i syntesen forekommer i mitokondrierne og består af virkningen af et enzym kaldet cholesterol desmolase, der hører til cytokrom P450 superfamilien og også kendt som "P450scc" eller "CYP11A1", hvilket fremmer eliminering af 6 af carbonatomer af sidekæden fastgjort til C17.
Med virkningen af desmolase omdannes kolesterol (med 27 kulstofatomer) til pregnenolon, som er en forbindelse med 21 kulstofatomer og repræsenterer den første af C21-typen steroider.
Pregnenolon bevæger sig til det glatte endoplasmatiske retikulum, hvorved virkningen af enzymet 3β-hydroxysteroid dehydrogenase gennemgår dehydrogenering i hydroxylen af alkoholgruppen af carbon 3 og bliver progesteron.
På grund af virkningen af 21β-hydroxylase, også kaldet “P450C21” eller “CYP21A2”, hydroxyleres progesteron ved carbon 21 og omdannes til 11-deoxycorticosteron, som vender tilbage til mitokondrierne, og hvortil enzymet 11β-hydroxylase (“P450C11 ”Eller“ CYP11B1 ”) konverterer til kortikosteron.
En anden syntese i den fascikulære zone, der ikke ender i kortikosteron, men i cortisol, opstår, når pregnenolon eller progesteron hydroxyleres i position 17 af 17a-hydroxylase ("P450C17" eller "CYP17") og omdannes 17-hydroxypregnolon eller 17-hydroxyprogesteron.
Det samme enzym, der allerede er nævnt, 3β-hydroxysteroid dehydrogenase, der omdanner pregnenolon til progesteron, omdanner også 17-hydroxypregnolon til 17-hydroxyprogesteron.
Sidstnævnte bæres successivt af de to sidste enzymer på vejen, der producerer corticosteron (21β-hydroxylase og 11β-hydroxylase) til henholdsvis deoxycortisol og cortisol..
Glukokortikoid handlinger
De vigtigste glukokortikoider produceret i zona fascicular i binyrebarken er corticosteron og cortisol. Begge stoffer, men især cortisol, udviser et bredt spektrum af handlinger, der påvirker stofskifte, blod, forsvar og sårhelingsreaktioner, knoglemineralisering, fordøjelseskanalen, kredsløbssystemet og lungerne..
Med hensyn til stofskifte stimulerer cortisol lipolyse og frigivelse af fedtsyrer, der kan bruges i leveren til dannelse af ketonlegemer og proteiner med lav densitet (LDL); nedsætter glukoseoptagelse og lipogenese i fedtvæv og glukoseoptagelse og anvendelse i muskler.
Det fremmer også proteinkatabolisme i periferien: i bindevæv, muskel og knoglematrix og frigiver derved aminosyrer, der kan bruges i leveren til syntese af plasmaproteiner og til glukoneogenese. Det stimulerer desuden absorptionen af tarmglukose ved at øge produktionen af SGLT1-transportører..
Accelereret tarmglucoseoptagelse, øget leverproduktion og nedsat udnyttelse af dette kulhydrat i muskel- og fedtvæv favoriserer en forhøjelse af plasmaglucoseniveauer..
Hvad angår blodet favoriserer cortisol koagulationsprocessen, stimulerer dannelsen af neutrofile granulocytter og hæmmer eosinofiler, basofiler, monocytter og T-lymfocytter. Det hæmmer også frigivelsen af inflammatoriske mediatorer såsom prostaglandiner, interleukiner, lymfokiner, histamin og serotonin.
Generelt kan det siges, at glukokortikoider interfererer med immunresponset, af hvilken grund de kan anvendes terapeutisk i de tilfælde, hvor dette respons er overdrevet eller upassende, såsom i tilfælde af autoimmune sygdomme eller i organtransplantationer for at reducere afvisning.
- Androgensyntese
Androgensyntese på niveauet af binyrebarken forekommer hovedsageligt på niveau med retikulær zone og fra 17-hydroxypregnolon og 17-hydroxyprogesteron.
Det samme 17a-hydroxylaseenzym, der producerer de to netop nævnte stoffer, har også 17,20 lyase-aktivitet, som fjerner de to carbonatomer i C17-sidekæden og erstatter dem med en ketogruppe (= O).
Denne sidste handling reducerer kulstofantalet med to og producerer C19-steroider. Hvis handlingen er på 17-hydroxypregnolon, er resultatet dehydroepiandrosteron; hvis det berørte stof tværtimod er hydroxyprogesteron, vil produktet være androstenedion.
Begge forbindelser er en del af de såkaldte 17-ketosteroider, da de har en ketongruppe ved kulstof 17.
3β-hydroxysteroid dehydrogenase omdanner også dehydroepiandrosteron til androstenedion, men det mest almindelige er, at førstnævnte omdannes til dehydroepiandrosteronsulfat af en sulfokinase, der næsten udelukkende er til stede i retikulær zone.
Syntese af mineralokortikoider (aldosteron)
Zona glomerularis mangler 17a-hydroxylase-enzymet og kan ikke syntetisere 17-hydroxysteroidforløberne til cortisol og kønshormoner. Det har heller ikke 11β-hydroxylase, men det har et enzym kaldet aldosteronsyntetase, der sekventielt kan producere kortikosteron, 18-hydroxycorticosteron og mineralokortikoid aldosteron..
Handlinger af mineralokortikoider
Det vigtigste mineralokortikoid er aldosteron syntetiseret i zona glomerularis i binyrebarken, men glukokortikoider viser også mineralokortikoid aktivitet.
Aldosteronets mineralokortikoidaktivitet udvikler sig på niveauet af den distale nefrons rørformede epitel, hvor det fremmer sekretion af natriumreabsorption (Na +) og kalium (K +) og bidrager således til bevarelsen af niveauerne af disse ioner i kropsvæsker.
- Syntese af mandlige kønssteroider i testiklerne
Testikulær androgensyntese forekommer på niveauet med Leydig-celler. Testosteron er det vigtigste androgenhormon, der produceres i testiklerne. Dens syntese involverer den indledende produktion af androstenedion som tidligere beskrevet til syntesen af androgener på niveauet af binyrebarken..
Androstenedion omdannes til testosteron ved virkningen af enzymet 17β-hydroxysteroid dehydrogenase, der erstatter ketongruppen i carbon 17 med en hydroxylgruppe (OH).
I nogle væv, der tjener som et mål for testosteron, reduceres det med en 5a-reduktase til dihydrotestosteron med større androgen styrke.
- Syntese af kvindelige kønssteroider i æggestokkene
Denne syntese sker cyklisk, der ledsager de ændringer, der opstår under den kvindelige seksuelle cyklus. Syntesen sker i folliklen, der i løbet af hver cyklus modnes for at frigive et æg og derefter producere det tilsvarende corpus luteum.
Østrogener syntetiseres i de granulære celler i den modne follikel. Den modne follikel har celler i sin theca, der producerer androgener som androstenedion og testosteron..
Disse hormoner diffunderer i nærliggende granulosa-celler, som har aromataseenzymet, der omdanner dem til estron (E1) og 17β-østradiol (E2). Fra begge syntetiseres estriol.
Handlinger af kønssteroider
Androgener og østrogener har som hovedfunktion udviklingen af henholdsvis mandlige og kvindelige seksuelle egenskaber. Androgener har anabolske virkninger, der fremmer syntesen af strukturelle proteiner, mens østrogener favoriserer ossifikationsprocessen.
Østrogenerne og progesteronet, der frigives under den kvindelige seksuelle cyklus, er beregnet til at forberede kvindens krop til en eventuel graviditet som et resultat af befrugtning af det modne æg, der frigives under ægløsning..
Handlingsmekanisme
Hvis du har brug for at opdatere din hukommelse om hormonernes virkningsmekanisme, anbefales det at se følgende video, før du fortsætter med at læse.
Virkningsmekanismen for steroidhormoner er ret ens i dem alle. I tilfælde af lipofile forbindelser opløses de uden problemer i lipidmembranen og trænger ind i cytoplasmaet i deres målceller, som har specifikke cytoplasmatiske receptorer for det hormon, som de skal reagere på..
Når hormonreceptorkomplekset er dannet, krydser det kernemembranen og binder sig i genomet på en måde som en transkriptionsfaktor med et hormonresponselement (HRE) eller primært responsgen, som igen kan undertiden regulere andre gener kaldes sekundært svar.
Slutresultatet er fremme af transkription og syntese af messenger-RNA'er, der oversættes i ribosomerne i det grove endoplasmatiske retikulum, der ender med at syntetisere proteinerne induceret af hormonet..
Aldosteron som et eksempel
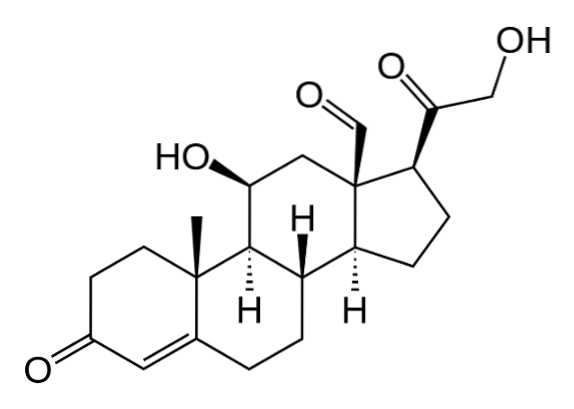
Aldosteronets virkning udøves hovedsageligt i niveauet med den sidste del af det distale rør og i opsamlingskanalerne, hvor hormonet fremmer Na + reabsorption og K-sekretion+.
I den luminale membran af de vigtigste rørformede celler i denne region er der epiteliale Na + kanaler og K + kanaler af "ROMK" typen. Renal ydre medullær kaliumkanal).
Den basolaterale membran har Na + / K + ATPase-pumper, der kontinuerligt trækker Na + fra cellen ind i det basolaterale interstitielle rum og introducerer K + i cellen. Denne aktivitet holder den intracellulære koncentration af Na + meget lav og favoriserer skabelsen af en koncentrationsgradient for denne ion mellem tubulens lumen og cellen..
Denne gradient gør det muligt for Na + at bevæge sig mod cellen gennem epitelkanalen, og da Na + passerer alene, forbliver der for hver ion, der bevæger sig, en ukompenseret negativ ladning, der får tubulens lumen til at blive negativ med hensyn til interstitiet. Det vil sige, at der skabes en transepitelial forskel med det negative lys.
Denne negativitet af lyset favoriserer udgangen af K +, der bevæges af dens højere koncentration i cellen, og lysets negativitet udskilles mod tubulens lumen for endelig at blive udskilt. Det er denne Na + reabsorption og K + sekretionsaktivitet, der reguleres af virkningen af aldosteron..
Aldosteron til stede i blodet og frigivet fra zona glomerularis som reaktion på virkningen af angiotensin II eller til hyperkalæmi, trænger ind i hovedcellerne og binder med sin intracytoplasmiske receptor.
Dette kompleks når kernen og fremmer transkriptionen af gener, hvis ekspression vil ende med at øge syntesen og aktiviteten af Na + / K + pumper, epiteliale Na + kanaler og ROMK K + kanaler såvel som andre proteiner. Respons, der vil have den samlede effekt af tilbageholdelsen af Na + i kroppen og stigningen i urin K-udskillelse+.
Referencer
- Ganong WF: Adrenal Medulla & Adrenal Cortex, 25. udgave. New York, McGraw-Hill Uddannelse, 2016.
- Guyton AC, Hall JE: Adrenokortikale hormoner, i Lærebog i medicinsk fysiologi , 13. udgave, AC Guyton, JE Hall (red.). Philadelphia, Elsevier Inc., 2016.
- Lang F, Verrey F: Hormon, i Physiologie des Menschen mit Pathophysiologie, 31. udgave, RF Schmidt et al (red.). Heidelberg, Springer Medizin Verlag, 2010.
- Voigt K: Endokrines System, I: Physiologie, 6. udgave; R Klinke et al. (Red.). Stuttgart, Georg Thieme Verlag, 2010.
- Widmaier EP, Raph H og Strang KT: Kvindelig reproduktiv fysiologi, i Vander's Human Physiology: The Mechanisms of Body Function, 13. udgave; EP Widmaier et al. (Red.). New York, McGraw-Hill, 2014.



Endnu ingen kommentarer