
Isomerisme
Hvad er isomerisme??
Isomerisme er et kemisk fænomen, der er kendetegnet ved, at molekyler med det samme antal atomer har forskellige kemiske eller fysiske egenskaber. Således forekommer det i isomerer, som igen er molekyler, hvis kemiske formler er de samme, men deres strukturer eller rumlige arrangementer adskiller sig væsentligt fra hinanden..
Vi har forfatningsmæssig eller strukturel isomerisme og rumlig isomerisme, som koncentrerer stor opmærksomhed om stereokemi. Rutediagrammet i billedet nedenfor viser, at isomerer hovedsageligt er opdelt i de to netop nævnte typer isomerisme: forfatningsmæssige og stereoisomerer..
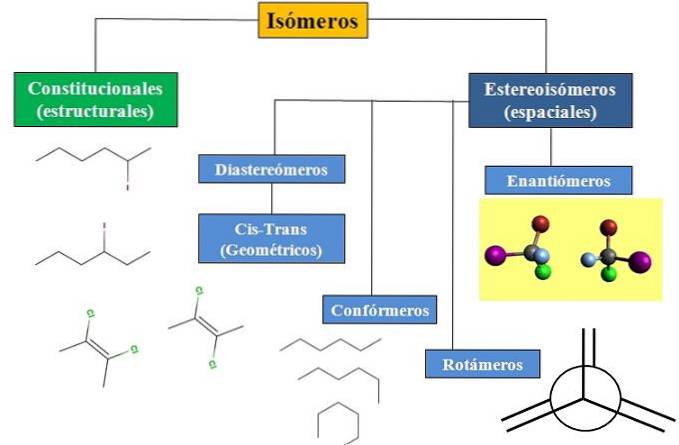
Alle isomerer, for en bestemt forbindelse, har den samme kemiske formel. Men de strukturer, som disse atomer kan bygge, og deres proportioner er unikke for hvert molekyle eller isomer. Selvom selve strukturen er den samme, kan atomerne eller grupperne også indtage forskellige rumlige positioner..
Flowdiagrammet viser nogle eksempler på isomerer, der vil blive diskuteret i de næste afsnit..
Typer af isomerer
Forfatningsmæssig
Forfatningsmæssige eller strukturelle isomerer er dem, der adskiller sig i rækkefølgen af den molekylære rygrad. Det vil sige, deres atomer er ikke forbundet på samme måde, så strukturen eller de pågældende funktionelle grupper kan blive meget forskellige..
For eksempel for den samme kemiske formel C7H10Eller der kan være flere molekyler, der opfylder det antal atomer; de vil alle have et enkelt iltatom, men det strukturelle arrangement af de andre atomer vil være unikt for hver isomer.
Og dermed de kemiske og fysiske egenskaber af alle konstitutionelle isomerer for formel C7H10Eller de vil også adskille sig meget fra hinanden.
På den anden side kan konstitutionelle isomerer være meget enkle og kun variere i den relative position af et enkelt atom eller en gruppe. I det næste afsnit vil du se et eksempel på dette og ovenstående sagde.
Stereoisomerer
Stereoisomerer er dem, der har den samme strukturelle rækkefølge, men adskiller sig i deres atomer eller gruppers position og rumlige orientering..
For at deres eksistens skal være mulig, skal molekyler indeholde stereogene centre, hvor de mest berømte inden for organisk kemi er asymmetriske eller chirale carbonatomer; det vil sige med fire forskellige substituenter.
Ud over asymmetriske carbonatomer skal det betragtede molekyle mangle elementer af symmetri. Ellers er det umuligt for den rumlige orden at blive stereoisomerisme..
Enantiomerer
Enantiomerer er stereoisomerer, der består af ikke-overlappende spejlbilleder. For eksempel overlapper de højre og venstre hænder ikke, ligesom sko eller handsker. Det næste afsnit behandler det klassiske eksempel på enantiomerisme: bromochloromethan: CBrClI.
Diastereomerer
Diastereomerer er derimod også stereoisomerer, men de er ikke spejlbilleder. Det vil sige, at at placere den ene foran den anden er ikke afspejling af sig selv. Af de mest kendte diastereomerer har vi cis-trans-isomerismen, også kaldet geometrisk isomerisme, især når den anvendes på alkener.
Conformers
Conformere, selvom de er inden for stereoisomerismens spektrum, er faktisk ikke isomerer. De er rumlige konfigurationer, som et molekyle i et bestemt øjeblik eller en energitilstand erhverver gennem rotation af flere af dets bindinger. Vi vil i næste afsnit se eksemplet på overensstemmelse med n-hexan.
Rotamer
Endelig har vi rotamerer, der ligner konformere i den forstand, at de er afhængige af rotation af kovalente bindinger..
Imidlertid tages en enkeltbinding mellem to carbonatomer som reference, og de relative positioner, uanset om de er overskygget eller vekslet, af substituenterne for begge carbonatomer sammenlignes. Senere vil vi se eksemplet på propylenrotamere.
Eksempler på isomerer
Hexanjod
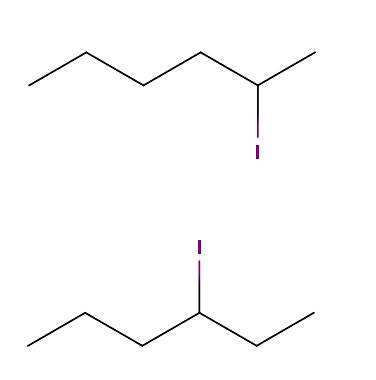
Ovenfor har vi to molekyler, hvis kemiske formler er C6H13I. I den første har vi 2-iodohexan, mens i den anden 3-iodohexan. De er konstitutionelle isomerer af positionstype, da skeletet er det samme, med den forskel at positionen af jodatomet varierer fra et kulstof til et andet..
C3H8ELLER
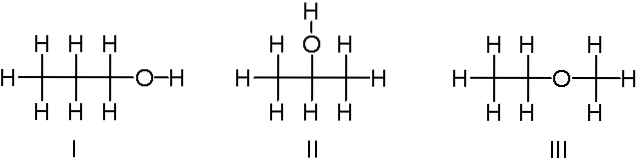
Ovenfor har vi et andet eksempel på konstitutionelle isomerer til den kemiske formel C3H8O. Molekyler I og II er henholdsvis 1-propanol og 2-propanol. De er begge alkoholer. I stedet handler molekyle III om ethyl-methylether.
Derfor taler vi om en anden funktionel gruppe. Bemærk, at de tre molekyler har det samme antal atomer, men deres strukturer er forskellige..
2,3-dichlor-2-buten
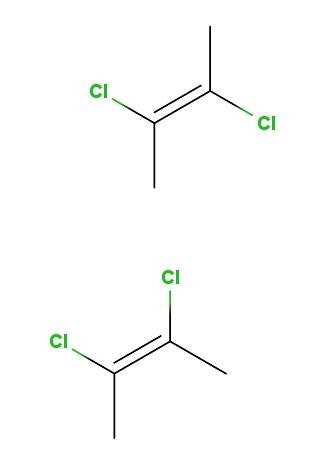
Ovenfor har vi trans-2,3-dichlor-2-buten-isomeren, og nedenfor har vi cis-2,3-dichlor-2-buten-isomeren. I den første er kloratomerne i modsatte positioner med hensyn til dobbeltbindingen, mens de i den anden ligger på samme side af dobbeltbindingen..
Rygraden for begge molekyler er den samme, men de adskiller sig i kloratomernes rumlige position; derfor er de stereoisomerer, og da de ikke er spejlbilleder, bliver de diastereomerer.
3-fluor-2-methylcyclohexan
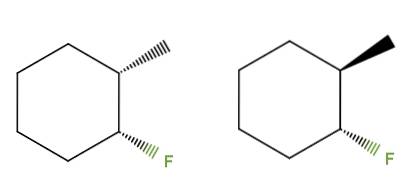
Denne gang har vi i stedet for en dobbeltbinding en cyclohexanring til forbindelsen 3-fluor-2-methylcyclohexan. I venstre isomer grupperer CH3 og F er under ringens plan; mens den i højre side CH3 er op og F er nede.
Derfor svarer den til venstre til cis-isomeren, og den til højre er trans-isomeren. De er derfor diastereomerer, fordi de igen ikke er spejlbilleder.
Overholdere af n-hexan
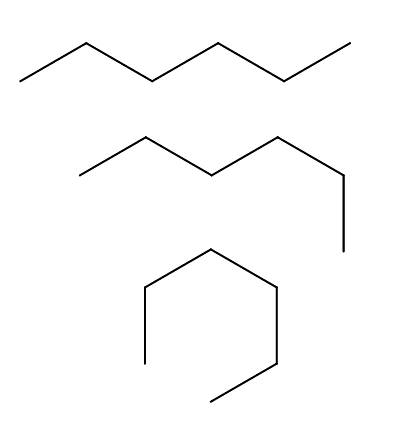
Vi har over tre overensstemmelse med n-hexan, som skyldes rotation og "bøjninger" af carbonkæden i forskellige retninger. De svarer alle til det samme molekyle af n-hexan med forskellige foldningsniveauer, som afhænger af miljøet og den indre energi i hvert molekyle.
3-brom-2-pentanol
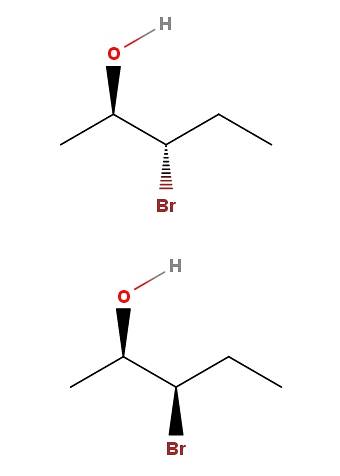
I 3-brom-2-pentanol har vi et andet eksempel på et par diastereomerer. Bemærk, at vi endnu en gang i isomeren ovenfor har OH og Br, der peger i den modsatte retning af skeletplanet; mens i den lavere isomer peger begge grupper mod læsernes retning.
1-brom-3-chlor-5-ethylcyclohexan
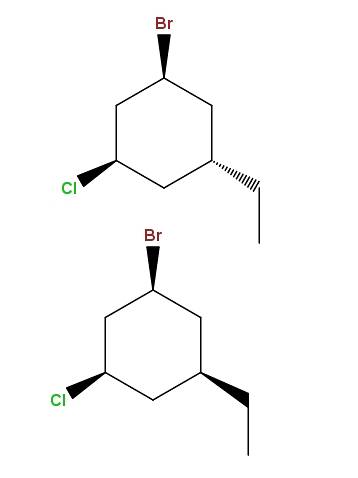
Og endnu en gang har vi endnu et par diastereomerer med den forskel, at forskellen nu ligger i en enkelt gruppes rumlige position: ethylen, -CHtoCH3.
Denne type isomerer har et meget specifikt navn: epimerer, som er diastereomerer, hvis variation kun observeres i den rumlige konfiguration af et enkelt asymmetrisk kulstof; i dette tilfælde er den bundet til -CHtoCH3.
Bromchlorooyodomethan
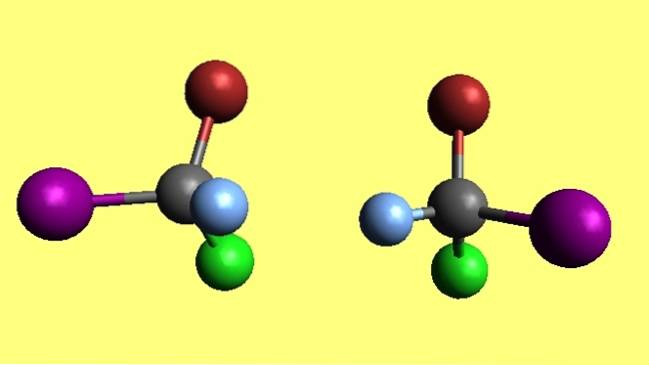
Bemærk, at de to bromchloriodmethanmolekyler, CBrClI, er enantiomerer, fordi den ene er den ikke-overlejelige refleksion af den anden. Uanset hvor hårdt du prøver, vil de fire atomer aldrig matche. De siges at have modsatte rumlige konfigurationer.
2-brom-4-ethylcyclohexan
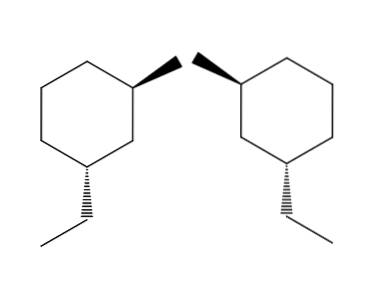
I eksemplet med 2-brom-4-ethylcyclohexan-paret af molekyler er enantiomerismen endnu mere tydelig. Hvis vi forsøger at vende molekylet til højre, vil vi se, at -CH-gruppentoCH3 det vil ikke være placeret under ringen, men over.
Tilsvarende CH3 Det peger ikke op på ringen, men under den. Rumlige konfigurationer er omvendte, de er modsatte. Dette er en anden af de vigtigste egenskaber ved enatiomerisme..
Propylen rotamerer
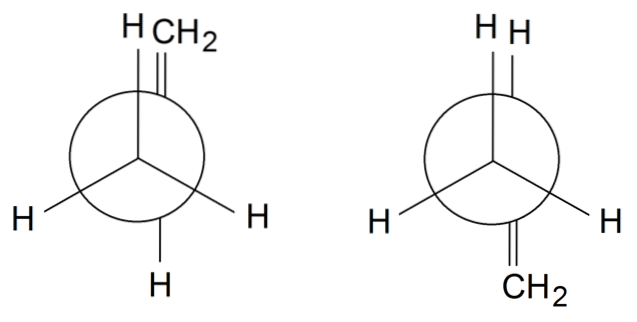
For at afslutte roterer vi i propylen-rotamerer enkeltbindingen mellem C1 og Cto: H3C-CH = CHto. Gruppen = CHto er i en formørket position med en af H'erne i CH-gruppen3 foran på rotameteret til venstre. I mellemtiden er = CHto og H er i alternative positioner på højre rotamer.
Afhængigt af gruppens formørkelse eller ej, vil vi have sterisk hindring, som vil destabilisere rotameren. Derfor er rotameren til højre mere stabil end den til venstre..
Referencer
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. (10th udgave.). Wiley plus.
- Carey F. (2008). Organisk kemi. (Sjette udgave). Mc Graw Hill.
- Morrison og Boyd. (1987). Organisk kemi. (Femte udgave). Addison-Wesley Iberoamericana.
- Dr. S. Gevorg. (2020). Enantiomerer, diastereomerer, identiske eller forfatningsmæssige isomerer. Kemiske trin. Gendannet fra: chemistrysteps.com
- Wikipedia. (2020). Isomer. Gendannet fra: en.wikipedia.org
- Allison Soult. (13. august 2020). Isomerer. Kemi LibreTexts. Gendannet fra: chem.libretexts.org
- James Ashenhurst. (2020). Stereokemi og chiralitet. Gendannet fra: masterorganicchemistry.com


Endnu ingen kommentarer