
Hvad er diatomiske elementer? (Eksempler)
Det diatomiske elementer, Også kaldet homonukleære diatomiske molekyler, de består af kun to atomer med de samme kemiske grundstoffer. Nogle elementer kan ikke eksistere alene, selv når de er isoleret fra andre atomtyper.
Elementer af denne art kombineres med atomer af det samme element for at være stabile. Med andre ord, brint, et diatomisk element, kan ikke være af sig selv. Det kan ikke bare eksistere H.
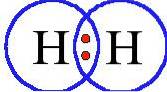
Brint er så reaktivt, at når det isoleres fra alt andet end brint, vil det kombinere sig i et diatomisk (to-atom) molekyle. Derfor findes brintgas, som undertiden bruges som brændstof, som Hto.
Diatomiske molekyler
Diatomiske molekyler indeholder to atomer, der er kemisk bundet. Hvis de to atomer er identiske, såsom iltmolekylet (Oto), udgør et homonukleært diatomisk molekyle, mens hvis atomerne er forskellige, som i carbonmonoxid (CO) -molekylet, danner det et heteronukleært diatomisk molekyle.
Molekyler, der indeholder mere end to atomer, kaldes polyatomiske molekyler, for eksempel kuldioxid (COto) og vand (HtoELLER). Polymermolekyler kan indeholde mange tusinder af komponentatomer.
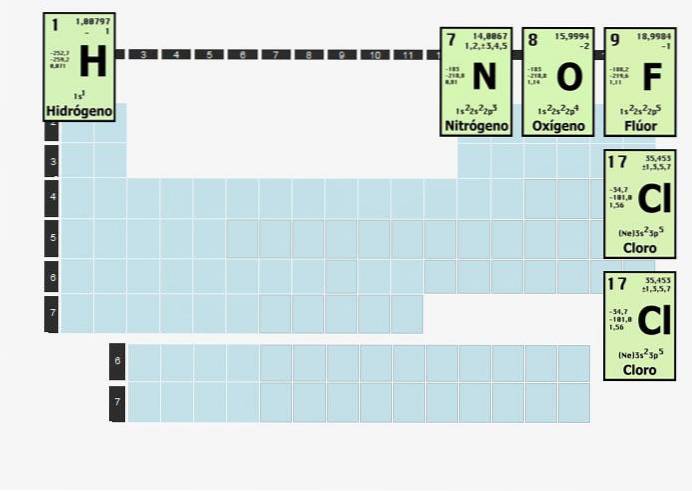
Der er syv elementer, der udgør diatomiske molekyler. Følgende 5 elementgasser findes som diatomiske molekyler ved stuetemperatur og tryk:
-Brint - Hto
-Kvælstof - Nto
-Oxygen - Oto
-Fluor - Fto
-Klor - Clto
Brom og iod findes almindeligvis i flydende form, men også som diatomiske gasser ved lidt højere temperaturer, hvilket giver i alt 7 diatomiske elementer..
-Brom - Brto
-Jod - jegto
Diatomiske elementer er halogener (fluor, chlor, brom, iod) og grundstoffer med en -gen-slutning (hydrogen, ilt, nitrogen). Astatin er et andet halogen, men dets adfærd er ukendt..
Egenskaber ved diatomiske elementer
Alle diatomiske molekyler er lineære, hvilket er det enkleste rumlige arrangement af atomer.
Det er praktisk og almindeligt at repræsentere et diatomisk molekyle som to punktmasser (de to atomer) forbundet med en masseløs fjeder..
Energierne involveret i molekylets bevægelser kan opdeles i tre kategorier:
- De translationelle energier (molekylet, der bevæger sig fra punkt A til punkt B)
- Rotationsenergier (molekylet roterer omkring sin akse)
- Vibrationsenergier (molekyler, der vibrerer på forskellige måder)
Alle diatomære elementer er gasser ved stuetemperatur med undtagelse af brom og iod, som er flydende (iod kan endda være i fast tilstand), og alle med undtagelse af ilt og nitrogen er forbundet med en enkelt binding..
Oxygenmolekylet har sine to atomer forbundet med en dobbeltbinding og nitrogenmolekylet med en tredobbelt binding.
Nogle diatomiske elementer
Brint
Brint (Hto), med et atomnummer på 1, er en farveløs gas, der ikke formelt blev opdaget som et element af Henry Cavendish indtil 1766, men ved et uheld blev fundet omkring hundrede år tidligere af Robert Boyle.
Det er en farveløs, lugtfri, giftfri gas, der findes naturligt i vores univers. At være det første element i det periodiske system, er brint det letteste og mest rigelige af alle de kemiske grundstoffer i universet, da det udgør 75% af dets masse..
Kvælstof
Kvælstof (Nto) har et atomnummer på syv og udgør ca. 78,05% af Jordens atmosfære i volumen.
Det er en lugtfri, farveløs og for det meste inert gas, og den forbliver farveløs og lugtfri i flydende tilstand..

Ilt
Oxygen (Oto) har et atomnummer på otte. Denne farveløse, lugtfri gas har otte protoner i sin kerne og er lyseblå i dens flydende og faste tilstand..
En femtedel af jordens atmosfære består af ilt, og det er det tredje mest forekommende element i universet efter masse..
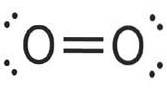
Oxygen er det mest forekommende massemasse i Jordens biosfære. Den høje iltkoncentration i atmosfæren er resultatet af jordens iltcyklus, der overvejende er drevet af fotosyntese i planter..
Fluor
Fluor (Fto) har et atomnummer på ni og er den mest reaktive og elektronegative af alle elementerne. Dette ikke-metalliske element er en lysegul gas, der er medlem af halogengruppen.
George Gore var tilsyneladende den første videnskabsmand, der isolerede fluor, men hans eksperiment eksploderede, da fluoren, der blev produceret, reagerede med brint..
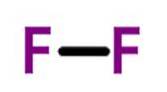
I 1906 blev Ferdinand Frederic Henri Moissan tildelt Nobelprisen i kemi for sit arbejde med isolering af fluor i 1886. Det er det mest elektronegative element i det periodiske system..
Klor
Klor (Clto) er medlem af halogengruppen med et atomnummer på sytten. En af dens former, NaCl, har været i brug siden oldtiden.

Klor har været i brug i tusinder af år i mange andre former, men det blev først navngivet før 1810 af Sir Humphry Davy..
Klor i sin rene form er gulgrøn, men dens almindelige forbindelser er typisk farveløse..
Brom
Brom (Brto) har et atomnummer på femogtredive. Det er en tung mørkebrun væske, det eneste ikke-metalliske element, der er en væske.

Brom blev opdaget af Antoine J. Balard i 1826. Den blev brugt til vigtige formål længe før den blev formelt opdaget..
Jod
Jod (Ito) har et atomnummer på treoghalvtreds med treoghalvtreds protoner i kernen af et atom. Det er et blå-sort ikke-metal, der spiller en meget vigtig rolle i organisk kemi..
Jod blev opdaget i 1811 af Barnard Courtois. Han kaldte det jod fra det græske ord "ioder", hvilket betyder violet. Det er en solid blå-sort.
Jod spiller en meget vigtig rolle i biologien for alle levende organismer, da dens mangel fører til sygdomme som hyperthyroidisme og hypothyroidisme.
Referencer
- (S.F.). Homonukleære diatomiske molekyler. Gendannet fra boundless.com.
- Klorfakta. (S.F.). Gendannet fra softschools.com.
- Diatomiske elementer. (S.F.). Gendannet fra ths.talawanda.org.
- Encyclopædia Britannica. (2016, 14. september). Molekyle. Gendannet fra britannica.com.
- Helmenstine, A. (2014, 28. september). Diatomiske elementer. Gendannet fra sciencenotes.org.
- Helmenstine, A. M. (2017, 29. marts). Hvad er de syv diatomiske elementer? Gendannet fra thoughtco.com.
- Oxygen Fakta. (S.F.). Gendannet fra softschools.com.
- Royal Society of Chemistry. (2015). molekylært iod. Gendannet fra chemspider.com.



Endnu ingen kommentarer