
Benedikts reagens, hvad det er til, komponenter, forberedelse
Det Benedikts reagens er en blålig opløsning af kobber, der bruges til at detektere tilstedeværelsen af reducerende sukkerarter: aldehyder, alfa-hydroxy-ketoner og hemicetaler. Det blev udviklet af Stanley R. Benedict (1884-1936).
Alfa-hydroxy-ketonsukker er kendetegnet ved at have en hydroxylgruppe i nærheden af ketonen. I mellemtiden er en hemiketal en forbindelse, der skyldes tilsætningen af en alkohol til et aldehyd eller keton. Benedikts reagens reagerer uden forskel på alle disse reducerende sukkerarter.
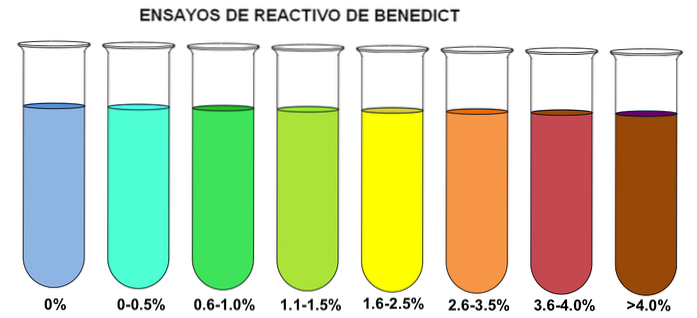
Benedikts metode er baseret på den reducerende virkning af sukker på Cuto+, af blå farve, som omdanner den til Cu+. CU+ danner et murstenrødt bundfald af kobberoxid. Afhængig af koncentrationen af sukker vises der et spektrum af farver (øverste billede).
Bemærk, at hvis Benedict's reagens sættes til et reagensglas uden at reducere sukker (0%), gennemgår det ikke nogen ændring i dets blålig farve. Således, når koncentrationen er højere end 4%, farves reagensglas brun..
Artikelindeks
- 1 Historie
- 2 Hvad er Benedict's reagens til?
- 2.1 Påvisning af glukose i urinen
- 2.2 Farvning af opløsningen
- 2.3 Påvisning af forskellige monosaccharider og disaccharider
- 3 komponenter
- 4 Fremgangsmåde til brug
- 5 Benedikts testreaktion
- 6 Klargøring af Benedict's reagens
- 7 Referencer
Historie
Reagenset blev oprettet af den amerikanske kemiker Stanley Rossiter Benedict i 1909, der offentliggjorde sin videnskabelige artikel Et reagens til påvisning af reducerende sukker, i tidsskriftet J. Biol. Chem.
Desuden offentliggjorde Lewis og Benedict (1915) en metode til bestemmelse af reduktion af sukker i blod ved anvendelse af picrat som en indikator; men stoppede med at blive brugt på grund af manglende specificitet.
Benedikts reagens ligner meget Fehlings. De adskiller sig ved, at Benedict bruger citrationen og natriumcarbonatsaltet; mens Fehling bruger tartrationen og natriumhydroxidet.
Benedict-testen er kvalitativ, dvs. det registrerer kun tilstedeværelsen af reducerende sukker. Imidlertid kan Benedict's reagens være kvantitativ, hvis den har kaliumthiocyanat i opløsning, som danner et hvidt bundfald af kobberthiocyanat, der kan titreres ved hjælp af glukosestandarder..
Hvad er Benedikts reagens til?
Påvisning af glukose i urinen
Benedict-reagenset bruges stadig til at detektere tilstedeværelsen af glukose i urinen og er en indikation af diabetes sygdom hos patienten, hvis urin udsættes for Benedict test eller test. Selvom det ikke kan udelukkes, at glucosuri har en anden oprindelse.
For eksempel findes øget glykosuri under tilstande som: graviditet, primær renal glykosuri, renal tubulær acidose, primær eller sekundær Fanconi syndrom, hyperaldosteronisme og akut pancreatitis eller kræft i bugspytkirtlen..
Benedikts reagens er blå på grund af tilstedeværelsen af Cuto+, som er reduceret til Cu+ ved at reducere sukker i dette tilfælde glukose, der danner et murstenrødt kobber (I) oxidfældning.
Opløsningsfarvning
Farven og dannelsen af bundfaldet i Benedict-testen anvendt på urin varierer afhængigt af koncentrationen af det reducerende sukker. Hvis glukosekoncentrationen i urinen er mindre end 500 mg / dL, bliver opløsningen grøn, og der dannes ikke noget bundfald.
En uringlukosekoncentration på 500 - 1.000 mg / dL forårsager et grønt bundfald i Benedict-testen. Ved en koncentration større end 1.000 til 1.500 mg / dL forårsager det dannelsen af et gult bundfald.
Hvis glukosekoncentrationen er 1.500 - 2.000 mg / dL, ses et orange bundfald. Endelig er en koncentration af glukose i urinen større end 2.000 mg / dL, det vil forårsage dannelsen af et murstenrødt bundfald..
Dette indikerer, at Benedict-testen har en semi-kvantitativ karakter, og at resultatet rapporteres ved hjælp af kryds. Således svarer for eksempel dannelsen af et grønt bundfald til et kryds (+); og dannelsen af et murstenrødt bundfald svarer til fire kryds (++++).
Påvisning af forskellige monosaccharider og disaccharider
Benedikts reagens detekterer tilstedeværelsen af reducerende sukkerarter, der har en fri funktionel gruppe eller en fri keton-funktionel gruppe, som en del af deres molekylære struktur. Dette er tilfældet med glucose, galactose, mannose og fructose (monosaccharider) samt lactose og maltose (disaccharider).
Saccharose og stivelse reagerer ikke med Benedict's reagens, fordi de har gratis reducerende grupper. Derudover er der forbindelser, der interfererer med Benedict-testen i urinen, hvilket giver falsk positivitet; sådan er tilfældet med salicylat, penicillin, streptomycin, levodopa, nalidixinsyre og isoniazid.
Der er kemikalier til stede i urinen, der kan reducere Benedict-reaktionen; for eksempel: kreatinin, urat og ascorbinsyre.
Komponenter (rediger)
Komponenterne i Benedict's reagens er som følger: kobbersulfatpentahydrat, natriumcarbonat, trinatriumcitrat og destilleret vand..
Kobbersulfat pentahydrat, CuSO45HtoO, indeholder Cuto+: er den forbindelse, der giver Benedikts reagens sin blå farve. Reducerende sukker virker på Cuto+, producerer sin reduktion til Cu+ og dannelsen af et bundfald af kobberoxid (CutoO) mursten rød.
Natriumcarbonat genererer et alkalisk medium, der er nødvendigt for, at reduktionen af kobber kan finde sted. Natriumcarbonat reagerer med vand og genererer natriumbicarbonat og hydroxylionen, OH-, ansvarlig for det alkaliske medium, der er nødvendigt for, at den reduktive proces finder sted.
Natriumcitrat danner et kompleks med kobber (II), der forhindrer det i at blive reduceret til Cu (I) under opbevaring.
Procedure for anvendelse
5 ml Benedict's reagens anbringes i et reagensglas på 20 x 160 mm, og der tilsættes 8 dråber urin til det. Reagensglasset rystes forsigtigt og anbringes i en beholder med kogende vand i 5-10 minutter..
Efter denne tid fjernes røret fra varmtvandsbadet, og overfladen afkøles med rindende vand for endelig at aflæse det opnåede resultat, når man udfører Benedict-testen (farverne).
Benedikts testreaktion
Reduktionen af Cu (II) under Benedict-testen kan skitseres som følger:
RCHO + 2 Cuto+ (i kompleks) + 5 OH- => RCOO- + CutoO + 3 HtoELLER
RCHO = aldehyd; RCOO- = (carboxylation); CutoO = kobberoxid, et murstenrødt bundfald.
Forberedelse af Benedict's reagens
173 gram natriumcitrat og 100 gram natriumcarbonat afvejes og opløses sammen i 800 ml varmt destilleret vand. Hvis der observeres spor af uopløste stoffer, skal opløsningen filtreres.
På den anden side opløses 17,3 gram kobbersulfatpentahydrat i 100 ml destilleret vand..
Derefter blandes de to vandige opløsninger forsigtigt og fortsættes under permanent omrøring, hvorved der fyldes op til 1.000 ml med destilleret vand..
Referencer
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kemi. Aminer. (10th udgave.). Wiley plus.
- Clark J. (2015). Oxidation af aldehyder og ketoner. Gendannet fra: chemguide.co.uk
- Wikipedia. (2020). Benedikts reagens. Gendannet fra: en.wikipedia.org
- Redaktionelt hold. (9. januar 2019). Benedict's Test: Princip, forberedelse af reagenser, procedure og fortolkning. Gendannet fra: laboratoriuminfo.com
- Dr. Whitson. (s.f.). Benedikts reagens: En test til reduktion af sukker. Gendannet fra: nku.edu



Endnu ingen kommentarer