
Jodidperoxidasekarakteristika, struktur, funktioner
Det iodidperoxidase o skjoldbruskkirtelperoxidase (TPO) er et hæm-glycoprotein, der hører til familien af pattedyrsperoxidaser (såsom myeloperoxidase, lactoperoxidase og andre), der deltager i syntesen af skjoldbruskkirtelhormon.
Dets vigtigste funktion er "iodering" af tyrosinrester i thyroglobulin og dannelsen af 3-3'-5-triiodothyronin (T3) og thyroxin (T4) gennem en "koblings" -reaktion. Intramolekylær af ioderede tyrosiner.
Triiodothyronin og thyroxin er to hormoner produceret af skjoldbruskkirtlen, der har væsentlige funktioner i pattedyrsudvikling, differentiering og metabolisme. Dens virkningsmekanisme afhænger af interaktionen mellem dens nukleare receptorer og specifikke gensekvenser af dens målgener..
Eksistensen af enzymet iodidperoxidase blev bekræftet i 1960'erne af forskellige forfattere, og der er nu gjort betydelige fremskridt med at bestemme dets struktur, dets funktioner og karakteristika for det gen, der koder det i forskellige organismer..
I meget af litteraturen relateret til dette enzym er det kendt som det mikrosomale "autoantigen" og er relateret til nogle autoimmune skjoldbruskkirtelsygdomme..
Takket være dets immunogene egenskaber er dette enzym et mål- eller målmolekyle for de antistoffer, der findes i serum hos mange patienter med skjoldbruskkirtelpatologier, og dets defekter kan føre til hormonelle mangler, der kan være vigtige patofysiologisk set.
Artikelindeks
- 1 Funktioner
- 1.1 Regulering af udtryk
- 2 Struktur
- 3 funktioner
- 3.1 Hvad er syntesen af skjoldbruskkirtelhormon?
- 4 Relaterede sygdomme
- 5 Referencer
Egenskaber
Iodidperoxidase kodes af et gen placeret på kromosom 2 hos mennesker, som måler mere end 150 kbp og består af 17 exoner og 16 introner..
Dette transmembranprotein, med et enkelt segment nedsænket i membranen, er tæt beslægtet med myeloperoxidase, med hvem det deler mere end 40% aminosyresekvenslighed.
Dens syntese forekommer i polyribosomer (et sæt ribosomer, der er ansvarlig for translationen af det samme protein) og indsættes derefter i membranen i det endoplasmatiske retikulum, hvor det gennemgår en proces med glykosylering.
Når den først er syntetiseret og glykosyleret, transporteres iodidperoxidase til den apikale pol af thyrocytter (skjoldbruskkirtelceller eller skjoldbruskkirtelceller), hvor den er i stand til at udsætte sit katalytiske centrum for skjoldbruskkirtlens follikulære lumen..
Regulering af udtryk
Ekspression af genet, der koder thyroidperoxidase eller iodidperoxidase, styres af skjoldbruskkirtelspecifikke transkriptionsfaktorer såsom TTF-1, TTF-2 og Pax-8.
De genetiske elementer, der tillader forøgelse eller forbedring af ekspressionen af dette gen hos mennesker, er blevet beskrevet i de regioner, der flankerer 5'-enden af det, sædvanligvis mellem de første 140 basepar i denne "flankerende" region..
Der er også elementer, der undertrykker eller formindsker ekspressionen af dette protein, men i modsætning til "enhancerne" er disse blevet beskrevet nedstrøms for gensekvensen..
Meget af reguleringen af den genetiske ekspression af iodidperoxidase sker på en vævsspecifik måde, og dette afhænger af virkningen af DNA-bindende elementer, der virker på cis, såsom TTF-1 transkriptionsfaktorer og andre.
Struktur
Dette protein med enzymatisk aktivitet har omkring 933 aminosyrerester og en ekstracellulær C-terminal ende på 197 aminosyrer, der kommer fra ekspressionen af andre genmoduler, der koder for andre glykoproteiner..
Dens molekylvægt er omkring 110 kDa og er en del af gruppen af type 1 glykosylerede transmembrane proteiner, da den har et glykosyleret transmembransegment og en hæmgruppe på sit aktive sted..
Strukturen af dette protein har mindst en disulfidbro i det ekstracellulære område, der danner en karakteristisk lukket sløjfe, der udsættes for overfladen af thyrocytter..
Funktioner
Den vigtigste fysiologiske funktion af iodidperoxidase er relateret til dets deltagelse i syntesen af skjoldbruskkirtelhormon, hvor det katalyserer "iodering" af tyrosinrester af monoiodotyrosin (MIT) og diiodotyrosin (DIT), ud over koblingen af iodotyrosinresterne i thyroglobulin.
Hvad er syntesen af skjoldbruskkirtelhormon?
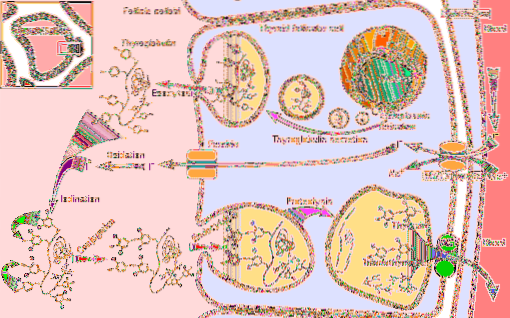
For at forstå funktionen af skjoldbruskkirtelperoxidaseenzymet er det nødvendigt at overveje trinene til hormonsyntese, hvor det deltager:
1-Det begynder med transport af iodid til skjoldbruskkirtlen og fortsætter med
2-Dannelsen af et oxidationsmiddel såsom hydrogenperoxid (H2O2)
3-Efterfølgende syntetiseres et receptorprotein, thyroglobulin
4-Jodidet oxideres til en højere valenstilstand og derefter
5-Iodid binder til tyrosinrester, der findes i thyroglobulin
6-I thyroglobulin dannes iodothyroniner (en type skjoldbruskkirtelhormoner) ved kobling af rester af iodotyrosin
7-Thyroglobulin opbevares og spaltes derefter
8-Jod fjernes fra de frie iodotyrosiner og til sidst,
9-Thyroxin og triiodothyronin frigives i blodet; Disse hormoner udøver deres virkning ved at interagere med deres specifikke receptorer, som er placeret på kernemembranen, og som er i stand til at interagere med mål-DNA-sekvenser, der fungerer som transkriptionsfaktorer..
Som det kunne udledes af kendskabet til funktionerne i de to hormoner, i hvis syntese det deltager (T3 og T4), har iodidperoxidase vigtige implikationer på det fysiologiske niveau..
Manglen på begge hormoner under menneskelig udvikling producerer defekter i vækst og mental retardation samt metaboliske ubalancer i voksenlivet.
Relaterede sygdomme
Iodidperoxidase er en af de største skjoldbruskkirtel autoantigener hos mennesker og er forbundet med komplement system-medieret cytotoksicitet. Dens funktion som et autoantigen fremhæves hos patienter med autoimmune skjoldbruskkirtelsygdomme.
Gigt sygdom, for eksempel, skyldes en mangel på jodindholdet under hormonsyntese i skjoldbruskkirtlen, hvilket igen har været relateret til en mangel på iodering af thyroglobulin som et resultat af visse defekter i iodidperoxidase..
Nogle carcinomer er kendetegnet ved at have ændrede iodidperoxidasefunktioner, dvs. aktivitetsniveauerne for dette enzym er signifikant lavere end hos ikke-kræftpatienter..
Undersøgelser har imidlertid bekræftet, at det er en meget variabel karakteristik, som ikke kun afhænger af patienten, men også af typen af kræft og de berørte regioner..
Referencer
- Degroot, L. J. og Niepomniszcze, H. (1977). Biosyntese af skjoldbruskkirtelhormon: Grundlæggende og kliniske aspekter. Fremskridt inden for endokrinologi og metabolisme, 26(6), 665-718.
- Fragu, P., & Nataf, B. M. (1976). Human skjoldbruskkirtelperoxidaseaktivitet ved godartede og ondartede skjoldbruskkirtelforstyrrelser. Det endokrine samfund, Fire. Fem(5), 1089-1096.
- Kimura, S. og Ikeda-saito, M. (1988). Human myeloperoxidase og skjoldbruskkirtelperoxidase, to enzymer med separate og forskellige fysiologiske funktioner, er evolutionært beslægtede medlemmer af samme genfamilie. Proteiner: Struktur, funktion og bioinformatik, 3, 113-120.
- Nagasaka, A., Hidaka, H., & Ishizuki, Y. (1975). Undersøgelser af human iodidperoxidase: dets aktivitet i forskellige skjoldbruskkirtelforstyrrelser. Chimica Acta Clinic, 62, 1-4.
- Ruf, J., & Carayon, P. (2006). Strukturelle og funktionelle aspekter af skjoldbruskkirtelperoxidase. Arkiv for biokemi og biofysik, 445, 269-277.
- Ruf, J., Toubert, M., Czarnocka, B., Durand-gorde, M., Ferrand, M., & Carayon, P. (2015). Forholdet mellem immunologisk struktur og biokemiske egenskaber af human skjoldbruskkirtelperoxidase. Endokrine anmeldelser, 125(3), 1211-1218.
- Taurog, A. (1999). Molekylær udvikling af skjoldbruskkirtelperoxidase. Biochimie, 81, 557-562.
- Zhang, J. og Lazar, M. A. (2000). Virkningsmekanismen for skjoldbruskkirtelhormoner. Annu. Præsten Physiol., 62(1), 439-466.



Endnu ingen kommentarer